基于胺基功能化磁性纳米粒子改进QuEChERS方法结合GC-MS/MS检测果蔬中7 种农药残留
连玉晶,周一冉,孙 欣,陈佳楠,郑振佳,王明林
(山东农业大学食品科学与工程学院,山东 泰安 271018)
为了增加产量并改善质量,需要在农作物上喷洒农药以控制病虫害和杂草。但是,长时间的使用或滥用农药会引起农药残留问题。在传统的农药残留分析方法中,样品预处理复杂,存在试剂用量大、操作复杂、费时、易污染且难自动化的问题,一直以来是分析检测的热点及难点[1]。因此有必要开发简单、经济、高效的农药残留分析前处理方法。
QuEChERS(quick, easy, cheap, effective, rugged and safe)方法因其简单、经济、高效等特性而被广泛用做食品基质中农药多残留分析的预处理方法[2],它主要包括目标物的提取及在溶剂中的分配、共萃物的净化及离心分离。在净化过程中,一些传统的净化材料包括N-丙基乙二胺吸附剂(primary secondary amine,PSA)[3-4]、石墨化碳黑(graphitized carbon black,GCB)[5]和C18[6-7]等,以及一些新材料包括多壁碳纳米管(multi-walled carbon nanotubes,MWCNTs)[8]、氧化石墨烯(graphene oxide,GO)[9]和二氧化锆基吸附剂(Z-Sep)[10]等的应用,提高了分析方法的灵敏度和选择性。这些材料可以在预处理过程中单独或组合使用,以分析各种类型基质中的不同目标分析物[11-14]。近年来,磁性纳米粒子(magnetic nanoparticles,MNPs)在样品前处理中显现了它的优势。替代分离过程中的离心操作,通过外部磁场即可实现吸附材料与萃取介质的分离,简化了操作步骤并节省了分析时间;此外,纳米材料比表面积大、吸附容量增加;磁性材料表面可接枝不同的功能基团如Fe3O4-MWCNTs[15]、Fe3O4/GO[16]和Fe3O4-PSA[17]等,提高了吸附的选择性。
以胺基为功能基团接枝的磁性材料可作为有机酸的吸附剂。姜飞虹等[18]制备的Fe3O4/壳聚糖磁性微球对苹果汁中有机酸具有良好的吸附性能。另外,胺基修饰的MNPs也可作为不同基质的净化剂。Wang Jun等[19]以磁性超支化聚酰胺为QuEChERS方法净化剂,建立橙汁中有机磷农药的检测方法。Liu Zhenzhen等[17]用Fe3O4-PSA和C18移除谷物基质中的脂肪酸和非极性干扰物。并通过液相色谱-串联质谱(liquid chromatography-tandem mass spectrometry,LC-MS/MS)法同时测定了水稻中50 种农药和8 种相关代谢物残留。与以非磁性材料作为净化吸附剂的传统QuEChERS方法相比,新方法可以节省30%的预处理时间。Qi Peipei等[20]用3-(N,N-二乙氨基)丙基三甲氧基硅烷改性的Fe3O4MNPs为吸附剂,开发了磁性QuEChERS方法,结合LC-MS/MS可测定苹果、奇异果、橙子和梨中的56 种农药残留。检测目标物的线性范围在2~200 ng/mL之间,相关系数(r)在0.943 4~0.999 3之间;添加回收率在60.2%~130%范围内,定量限为10 ng/kg。
果蔬基质中极性干扰物较多,为了达到更好的净化目的,提高方法的灵敏度及选择性,本研究将3-[2-(2-氨基乙基氨基)乙基氨基]丙基(3-[2-(2-aminoethylamino)ethylamino] propyltrimethoxy,PAAA)接枝到磁性材料表面,可以提供较大的极性基团,增强对基质中极性干扰物的吸附。研究制备了不同胺基含量接枝的MNPs并与商品PSA净化性能进行比较,优化净化参数。开发以胺基功能化MNPs为净化剂的QuEChERS方法,并与气相色谱-串联质谱(gas chromatography-tandem mass spectrometry,GC-MS/MS)结合用于分析果蔬中7 种农药残留。
1 材料与方法
1.1 材料与试剂
农药标准品猛杀威(99.0%)、二嗪磷(97.5%)、百菌清(99.5%)、甲基溴硫磷(99.5%)、喹硫磷(98.5%)、硫丹(99.7%)、咯菌腈(98.0%) 英国LGC Promochem公司;氯化亚铁(FeCl2g 4H2O)(分析纯) 天津大茂化学试剂厂;氨水(NH3g H2O)(分析纯) 北京化工厂;正硅酸乙酯(tetraethyl orthosilioate,TEOS)(分析纯) 天津科密欧化学试剂有限公司;乙腈、正己烷(均为色谱纯),无水乙醇、六水合三氯化铁(III)(FeCl3g 6H2O)、无水硫酸镁、氯化钠(NaCl)(均为分析纯) 天津凯通化学试剂有限公司;PSA(40 μm) 天津博纳艾杰尔科技有限公司;3-[2-(2-氨基乙基氨基)乙基氨基]丙基三甲氧基硅烷(3-[2-(2-aminoethylamino) ethylamino] propyltrimethoxysilane,AAAPTMS)(纯度90%)、N-(2-氨基乙基)-3-氨基丙基三甲氧基硅烷(N-[3-(trimethoxysilyl)propyl] ethylenediamine,AAPTMS)(纯度90%)、(3-氨基丙基)三乙氧基硅烷((3-a m i n o p r o p y l)triethoxysilane,APTES)(纯度95%) 上海谱振生物科技有限公司。
1.2 仪器与设备
JEM 2010透射电子显微镜(transmission electron microscope,TEM) 日本电子株式会社;Nicolet iN10傅里叶变换红外光谱(Fourier transform infrared spectroscopy,FT-IR)仪、Escalab 250xi X射线光电子能谱(X-ray photoelectron spectroscopy,XPS)仪 美国Thermo Fisher Scientific公司;MPMS SQUID VSM磁学测量系统 美国Quantum Design公司;Zetasizer Nano ZS90 Zeta电位分析仪 英国Malvern Panalytical公司;T18 digital Ultra Turrax匀浆器 德国IKA-Werke GmbH & Co.KG公司;TGL-20bR离心机 上海安亭科学仪器厂;QL-861涡旋振荡器 江苏其林贝尔仪器制造有限公司;KD200氮吹仪 杭州奥盛有限公司;CASCADA IIII-10实验室净水系统 颇尔(中国)有限公司;GC-2010 Plu-GCMS-TQ 8030 GC-MS联用仪(配备有电子电离源)日本岛津株式会社。
1.3 方法
1.3.1 混合标准溶液的配制
称取一定质量的单个农药标准品溶于甲苯或正己烷中制备100 μg/mL单个标准贮备液。吸取不同体积的单个农药标准贮备溶液于正己烷中稀释至所需浓度,配制7 种农药的混合标准溶液。
1.3.2 Fe3O4纳米粒子的合成
参考Li Yanfei等[5]的方法合成Fe3O4。将FeCl3g 6H2O(5.40 g)置于含100 mL去离子水的500 mL三颈圆底烧瓶中搅拌溶解,迅速将FeCl2g 4H2O(2.00 g)转移到上述三颈圆底烧瓶中,在氮气保护下搅拌,并逐滴加入110 mL氨水,滴定速度保持恒定,在30 min内滴定结束;随后在70 ℃的油浴中快速搅拌3 h,待反应结束后将产物分别用去离子水和无水乙醇各洗涤3 次,置于60 ℃真空干燥箱中干燥24 h。
1.3.3 二氧化硅包覆Fe3O4纳米粒子(Fe3O4@SiO2)的合成
参考Lu Yu等[21]的方法合成Fe3O4@SiO2纳米粒子,并作适当修改。将0.20 g Fe3O4加入到内有200 mL异丙醇和40 mL去离子水的500 mL三颈圆底烧瓶中。在连续搅拌下,向混合物中加入1 mL氨水溶液和130 μL TEOS,继续搅拌反应3 h;待反应结束后,通过磁铁收集Fe3O4@SiO2,然后分别用去离子水和无水乙醇各洗涤3 次,最后在真空干燥箱中60 ℃干燥24 h。
1.3.4 胺基功能化Fe3O4@SiO2纳米粒子的合成
参考Liu Yue等[22]的方法合成胺基功能化Fe3O4@SiO2纳米粒子,并作适当修改。将0.50 g Fe3O4@SiO2超声分散于50 mL去离子水和50 mL无水乙醇混合溶液中,边搅拌边将2 mL硅烷偶联剂(APTES、AAPTMS或AAAPTMS)逐滴加入到混合物中。在连续搅拌下,70 ℃反应24 h;反应结束后自然冷却至室温,通过磁铁收集不同胺基功能化的Fe3O4@SiO2,将产物用去离子水和无水乙醇各洗涤3 次,最后置于真空干燥箱中60 ℃干燥24 h。上述3 种硅烷偶联剂接枝的磁性材料分别表示为Fe3O4@SiO2-NH2、Fe3O4@SiO2-PSA和Fe3O4@SiO2-PAAA(图1)。
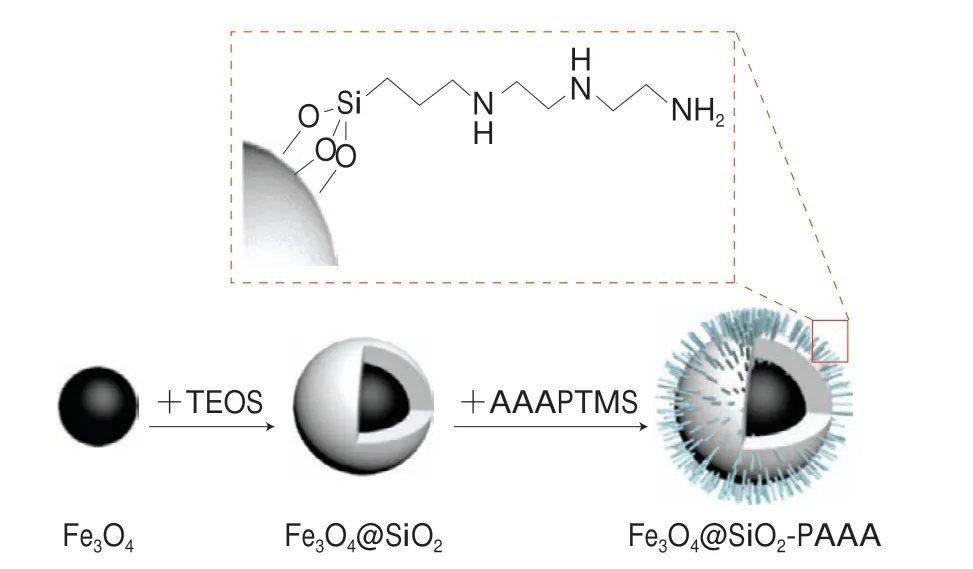
图1 Fe3O4@SiO2-PAAA的合成示意图Fig.1 Schematic illustration of the synthesis process of Fe3O4@SiO2-PAAA
1.3.5 样品的制备
称取10.00 g均质的样品(番茄、黄瓜或苹果)于50 mL离心管中,向离心管中加入10 mL体积分数为1%的乙酸-乙腈溶液,然后用均质器均质30 s,再向离心管中依次加入1.0 g氯化钠和4.0 g无水硫酸镁,并立即涡旋混合1 min,然后5 000 r/min离心5 min;将1 mL上层溶液转移到另一个2 mL装有一定质量的净化材料和100 mg无水硫酸镁的微量离心管中;涡旋一定时间后,通过磁铁将净化材料与提取液分离。吸取上清液过0.22 μm微孔滤膜,于GC-MS/MS进样分析。样品的制备过程如图2所示。
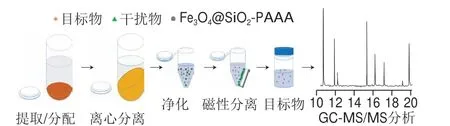
图2 样品制备过程示意图Fig.2 Schematic illustration of sample preparation process
1.3.6 GC条件
H P-5 M S 石英毛细管柱(3 0 m h 0.2 5 0 m m,0.25 μm);进样口温度290 ℃;升温程序:柱温75 ℃保持3 min,然后以30 ℃/min速率升温至230 ℃,以6 ℃/min速率升温至280 ℃并保持3 min。氦气流速1.2 mL/min;进样量1 μL;不分流进样。
1.3.7 MS条件
电离能量70 eV;离子源温度230 ℃;GC-MS/MS接口温度280 ℃;监控模式多反应监测(multiple reaction monitoring,MRM)。目标物的化学结构、分类、保留时间及质谱参数见表1。
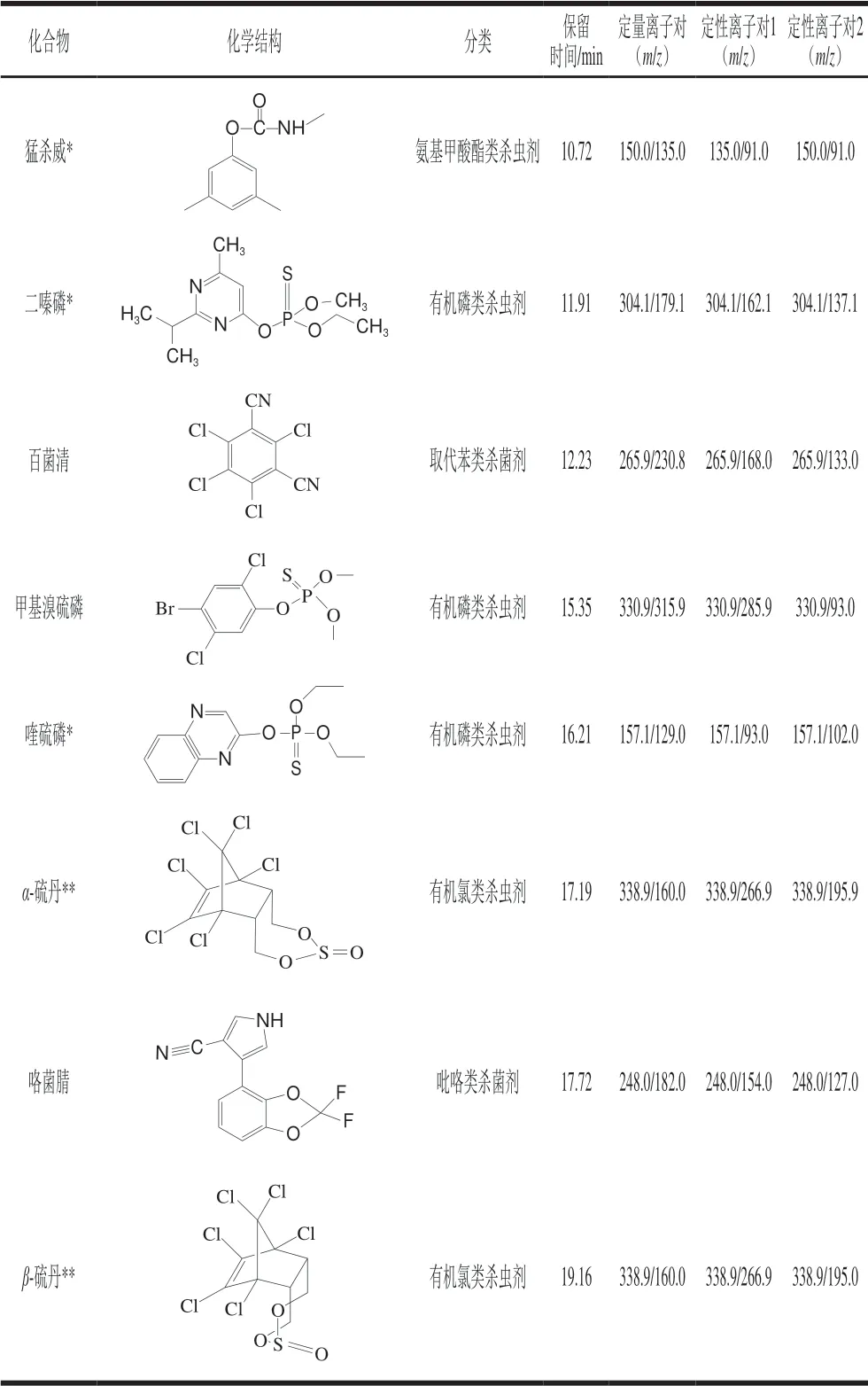
表1 7 种农药的化学结构、分类、保留时间及质谱参数Table 1 Chemical structures, assignment, retention times and MS parameters of 7 pesticides
2 结果与分析
2.1 MNPs的表征
2.1.1 形貌分析

图3 Fe3O4(a)和Fe3O4@SiO2-PAAA(b)的TEM图Fig.3 TEM images of Fe3O4 (a) and Fe3O4@SiO2-PAAA (b)
由图3a可以看出,球形Fe3O4的平均直径约为10 nm左右。图3b显示,功能基团包覆在Fe3O4表面并呈现核壳结构。
2.1.2 磁化分析
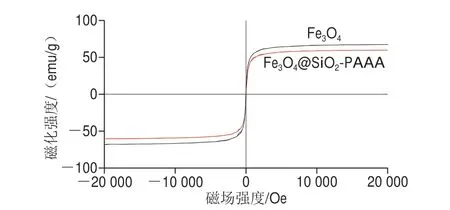
图4 Fe3O4和Fe3O4@SiO2-PAAA的磁滞回线Fig.4 Hysteresis loops of Fe3O4 and Fe3O4@SiO2-PAAA
采用振动样品磁强计测定MNPs的磁化强度,见图4。Fe3O4和Fe3O4@SiO2-PAAA的饱和磁化强度分别为67.59 emu/g和60.07 emu/g,表明包覆的功能基团对Fe3O4的磁性影响较小。2 个材料均可被磁铁快速吸附。
2.1.3 FT-IR和XPS分析
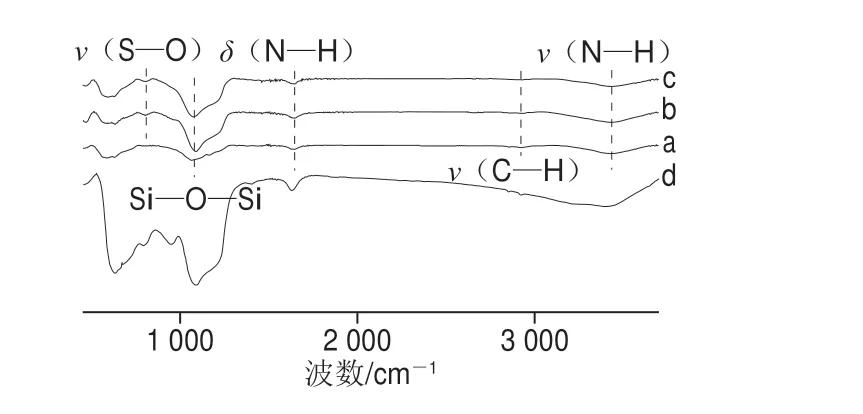
图5 MNPs的FT-IR分析图谱Fig.5 FT-IR spectra of MNPs
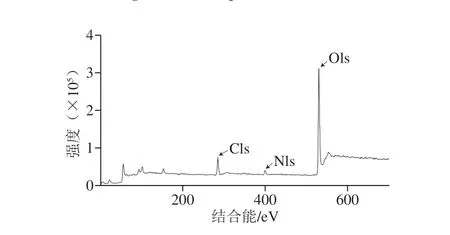
图6 Fe3O4@SiO2-PAAA的XPS全谱分析Fig.6 XPS survey spectrum of Fe3O4@SiO2-PAAA
通过FT-IR和XPS可验证MNPs表面接枝的官能团。从图5可以观察到,胺基功能化MNPs在1 062 cm-1和794 cm-1处有吸收峰,表明存在Siü Oü Si(不对称)和Siü O伸缩振动[23],由此可确定SiO2成功包覆到Fe3O4表面。在1 636 cm-1处的吸收峰为Nü H的弯曲振动,2 922 cm-1的吸收峰代表Cü H的伸缩振动以及在3 422 cm-1处检测到Nü H的伸缩振动[24],表明胺基已经接枝到MNPs表面。在对Fe3O4@SiO2-PAAA进行的XPS全谱分析中,O1s、C1s和N1s均有吸收峰(图6),进一步证实了功能基团已接枝到Fe3O4MNPs上。
2.1.4 Zeta电位分析
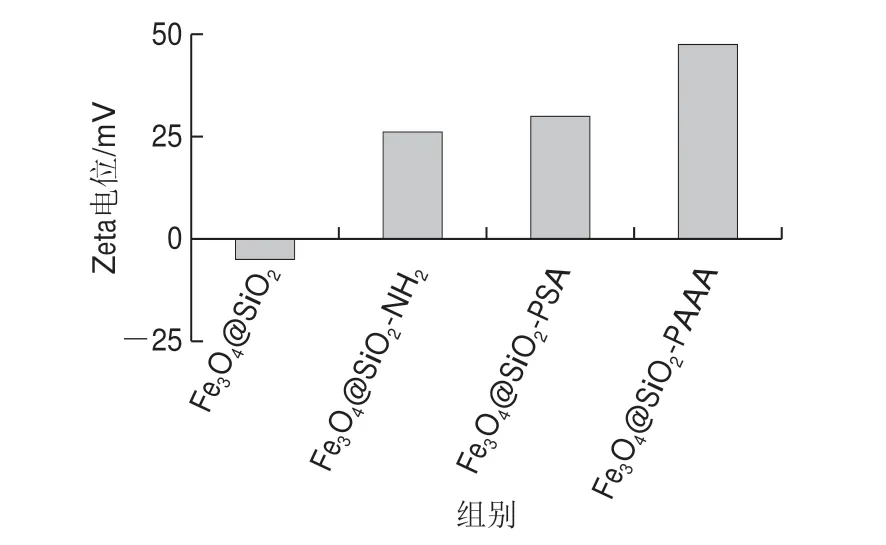
图7 MNPs的Zeta电位值Fig.7 Zeta potential of MNPs
胶体粒子的Zeta电位与其表面电荷有关。Zeta电位与胺基表面密度的对数之间具有良好的相关性。该关系由Zeta电位=38.7+21.6lgσ表示,其中σ定义为每1 nm2的ü NH2基团数[25]。实验中测量分散在含1 mmol/L NaNO3的0.1 mol/L HCl中功能化MNPs的Zeta电位值。图7显示未改性的Fe3O4@SiO2具有负的Zeta电位,而氨基功能化MNPs Zeta电位为正值。Fe3O4@SiO2-NH2、Fe3O4@SiO2-PSA和Fe3O4@SiO2-PAAA的Zeta电位值分别为26.27、30.04 mV和47.65 mV。因此,计算得到不同氨基功能化MNPs的表面氨基基团数分别为0.27、0.40 个/nm2和2.60 个/nm2。表明在Fe3O4@SiO2-PAAA表面的氨基含量明显高于其他2 种胺基接枝的MNPs。
2.2 提取溶剂及盐的选择
在果蔬基质的多种农药残留分析中,应用较多的提取试剂有乙腈、丙酮和乙酸乙酯。对于混合果蔬基质,乙腈与丙酮和乙酸乙酯比较,在GC-MS(全扫描模式)监测时,干扰物质最少[3]。因此,本研究选择的提取试剂为乙腈。目标物百菌清和硫丹是不稳定农药,在酸性乙腈中比乙腈中稳定性好。方法选择提取剂为含有体积分数为1%乙酸的乙腈溶液[26]。
在分配过程中加入NaCl、MgSO4等盐的目的是增加极性农药在有机相中的分配,从而提高这些农药的回收率。MgSO4比NaCl的吸水性好,但是在吸收水分过程中易形成团块,并且硫酸镁吸水是个放热过程,加入太多不但使后面涡旋操作更困难,同时可能影响热敏感目标物的稳定性。水相中盐的浓度不仅影响农药在有机相中分配,同时也影响基质中极性组分在有机相中的含量。Anastassiades等[3]发现在加入一定量的NaCl进行分配平衡时,可以减少有机相中极性组分(糖)的含量。因此本研究选择MgSO4和NaCl的组合方式吸收分配过程中的水分,在减少有机相中极性干扰物的同时提高目标物的回收率。实验基于Li Yanfei等[5]的研究,选择MgSO4和NaCl的添加量为每10 g样品分别添加4.0 g和1.0 g。
2.3 不同胺基功能化MNPs净化效果比较
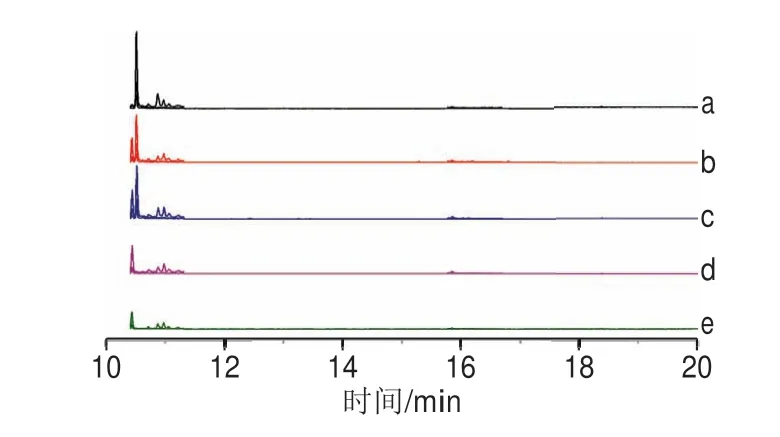
图8 不同净化材料处理番茄空白基质的总离子流图Fig.8 TIC chromatograms of tomato blank matrix by purification with different sorbents
为了评估功能化MNPs的净化能力,研究以不同氨基功能化MNPs及PSA为净化剂,对番茄空白样品进行前处理实验。从图8可以看出,保留时间在10~12 min的谱图中存在较多干扰峰;不同的吸附材料对样品有不同程度的净化效果,表现在干扰峰信号的强弱不同。经过Fe3O4@SiO2-PAAA净化的样品干扰峰最弱,这是因为—NH2和PSA是弱离子交换基团,可与化合物中的极性基团通过氢键结合,移除基质中的脂肪酸、有机酸、糖和花青素等杂质。与—NH2比较,由于仲胺的存在,PSA可移除更多的基质共萃物[3],而Fe3O4@SiO2-PAAA比PSA在结构上还要多1 个氨基,因此对共萃物的吸附能力会更强。

图9 4 种不同吸附剂对加标回收率的影响Fig.9 Effects of four different sorbents on spiked recoveries
在添加水平为0.5 mg/kg的番茄样品中,以不同材料为吸附剂得到的回收率结果见图9。可以看出,以3 种功能化MNPs为净化剂处理的样品中7 种农药(其中硫丹有α和β同分异构体)的添加回收率均高于商品PSA。并且,随着接枝氨基数量的增加,百菌清回收率也从44.6%提高到90.0%以上。Fe3O4@SiO2-PSA和Fe3O4@SiO2-PAAA处理的样品中农药的回收率无太大差别,7 种农药添加回收率集中在84.0%~95.5%之间,但后者处理的样品相对标准偏差(relative standard deviation,RSD)相对较低。结合考虑总离子流图中干扰情况,最后确定Fe3O4@SiO2-PAAA为最优的净化材料。在后续的实验中,选择Fe3O4@SiO2-PAAA为净化吸附剂。
2.4 净化条件的优化
对于果蔬基质的净化,GCB和PSA是最优的净化组合。GCB可去除基质中具有平面结构的物质(叶绿素、固醇等),但也会保留平面结构的农药(如百菌清),并且Anastassiades等[3]在研究中发现叶绿素在GC-MS上并未显示出干扰峰。因此,方法中仅选择Fe3O4@SiO2-PAAA作为净化剂。
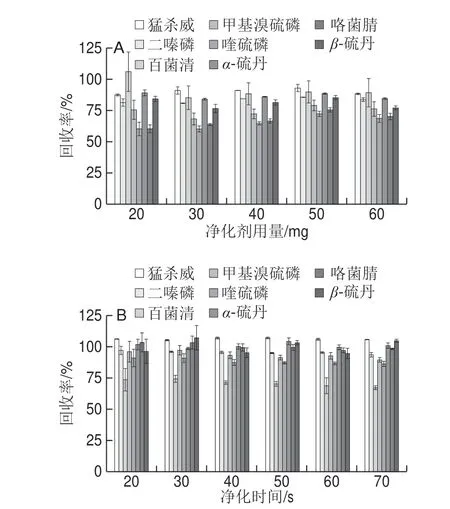
图10 净化剂用量(A)和净化时间(B)对目标农药提取效率的影响Fig.10 Effects of sorbent dosage (A) and clean-up time (B) on the extraction efficiency of the target pesticides
研究比较了Fe3O4@SiO2-PAAA不同用量对目标物添加回收率的影响。番茄样品中添加0.5 mg/kg农药混合标准溶液,然后按照样品的制备方法处理样品,其中净化剂用量分别为20、30、40、50 mg和60 mg。从图10A可以看出,50 mg添加量处理的样品获得最好的添加回收率,在72.2%~93.0%范围内。其中溴硫磷、喹硫磷和咯菌腈的回收率随净化剂用量的改变,变化较大。因此方法确定净化剂添加量为50 mg。
在最佳实验条件下,对净化时间进行优化。净化时间分别为20、30、40、50、60 s和70 s。从图10B可以看到,净化时间在20~70 s内,回收率差别不大。原因可能是在较短的时间内净化剂对干扰物的吸附就已经达到了平衡,从效率及添加回收率考虑,方法的净化时间确定为20 s。
2.5 方法学验证
2.5.1 线性方程、检出限和定量限结果
向空白基质中加入不同浓度的混合标准溶液,绘制标准曲线。分析物的含量最高不超过1 mg/kg。确定最佳的检测范围及相关系数。方法检出限(limit of detection,LOD)是信噪比(RSN)为3时检测目标物的含量;定量限(limits of quantitation,LOQ)为RSN为10时检测目标物的含量。如表2所示,每种目标物均表现出良好的线性,线性范围在0.007~1.000 mg/kg之间;线性相关系数(R2)高于0.994;方法LOD范围在0.002~0.005 mg/kg之间;LOQ在0.007~0.017 mg/kg之间。
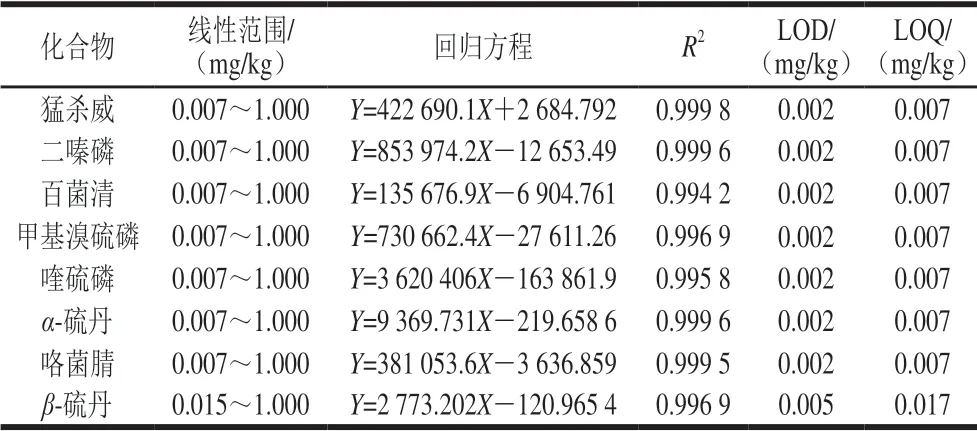
表2 7 种农药的校准曲线、回归数据、检出限和定量限Table 2 Calibration curve equations, LODs, and LOQs of seven pesticides (n= 3)
2.5.2 基质效应
以不分流方式进样的GC进样口以及分离柱中存在各种活性位点,这些活性位点不可逆吸附和/或催化(热)分解一些敏感分析物。除了玻璃内衬表面中可能存在的游离硅烷醇基和金属之外,其他活性位点也可能来自前部的非挥发性共萃取物[27]。产生基质诱导色谱增强或抑制作用的化合物通常是热不稳定的或者是极性的、易于发生氢键键合的化合物。影响基质增强效应的因素有分析物的化学结构及浓度,通常分析物浓度越低基质增强效应越明显;另一个重要因素是基质的组成。基质效应用试剂标准和基质标准制作的校准曲线斜率表示[28]。
基质效应值为正数表明基质对信号有增强作用。相反,为负数则表明基质对信号有抑制作用。从图11可以看出,新建方法处理的番茄、苹果和黄瓜样品中不同农药的基质效应不同。与黄瓜比较,番茄和苹果中7 种农药的基质效应较低。参照Zhang Zihao等[6]的分类方法,基质效应绝对值≤20%,基质无影响;20%<基质效应绝对值≤50%,中等强度基质效应;基质效应绝对值>50%,强的基质效应。以这个分类标准可以判断,新建的分析方法中番茄和苹果无基质效应。黄瓜基质中猛杀威和二嗪磷无基质效应,百菌清表现为强基质抑制效应,其他农药均显示中等强度基质增强效应。由图11可以看出,与其他农药比较,百菌清和甲基溴硫磷2 种农药受基质影响较大。
2.5.3 回收率和精密度结果
实验对番茄、苹果和黄瓜3 种基质分别进行了LOQ、2 倍LOQ和10 倍LOQ三个水平的添加回收率实验,每个样品设置5 个平行,回收率在70%~110%之间,RSD低于20%认为可接受。由表3可知,方法添加回收率在75.2%~105.4%范围内,RSD在3.7%~15.7%之间。结果表明以Fe3O4@SiO2-PAAA为磁性吸附剂改进的QuEChERS方法,结合GC-MS/MS分析果蔬中7 种农药残留,检测方法具有较好的准确度和精密度。
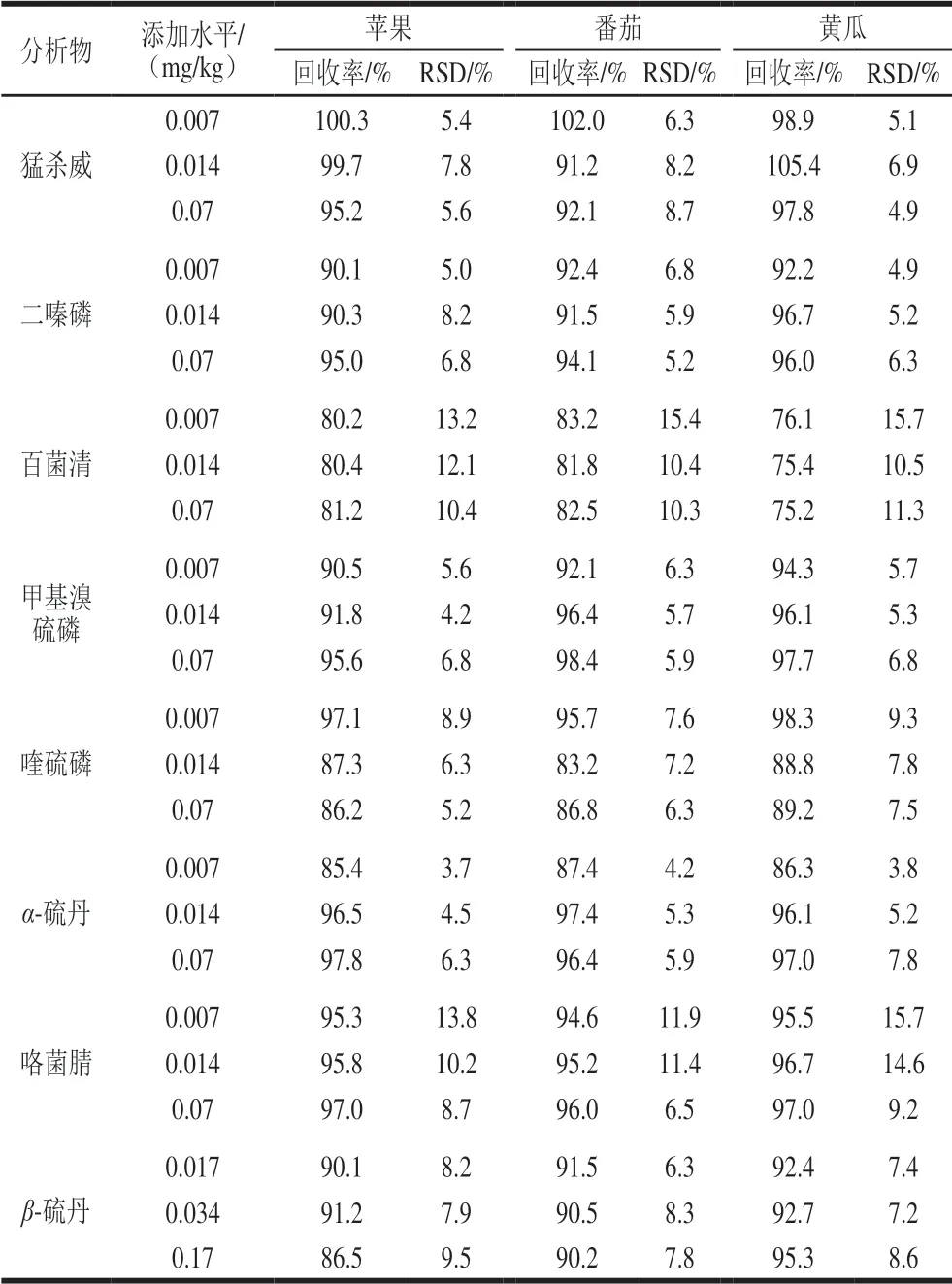
表3 苹果、番茄和黄瓜中7 种农药的添加回收率及RSDTable 3 Recoveries and RSDs of 7 pesticides in spiked apples,tomatoes and cucumbers (n= 5)
2.6 实际样品分析
为了明确方法的适用性,分别从超市及农贸市场购买番茄、苹果和黄瓜各2 组不同品种的样品,每组5 份共30 份。按照新开发的方法检测其中的农药残留。其中1 组番茄样品中检测到了百菌清,含量为0.027 mg/kg。可能的原因是农户在未过农药安全间隔期即进行了采收。
3 结 论
研究制备了具有高磁化强度的Fe3O4@SiO2-PAAA纳米粒子。开发了以Fe3O4@SiO2-PAAA为吸附剂的改进的QuEChERS方法,结合GC-MS/MS可同时测定果蔬中的7 种农药残留。建立的方法操作简单、快速;线性范围宽、检出限低、准确度高。Fe3O4@SiO2-PAAA可作为替代PSA的净化剂。本研究对新材料在农药多残留分析中的应用具有一定的指导意义。

