RuPt双金属在催化加氢反应中的性能研究
刘曼君,王柳枫,王梁炳
(1. 中南大学 材料科学与工程学院,长沙 410083;2. 浙江新和成股份有限公司,浙江 绍兴 312500)
苯乙烯是聚苯乙烯或橡胶工业中非常重要的有机化工原料,是按体积成本计算的最便宜的热塑性聚合物之一[1]。苯乙烯主要由乙苯脱氢制得,但在实际的脱氢过程中,脱氢副产物苯乙炔会导致脱氢催化剂失活[2-3],与此同时,生成的苯乙炔会降低苯乙烯的纯度,从而影响产品品质[4]。以苯乙炔为原料通过半氢化是制备高品质苯乙烯的另一种有效途径,在苯乙炔加氢制苯乙烯过程中,提高目标产物苯乙烯的选择性是至关重要的一步。
4-硝基酚催化加氢生成4-氨基酚也是一个具有重要意义的催化反应。4-硝基酚是一种含硝基的芳香族酚类化合物,是纺织、医药、塑料和染料制造等工业过程和农化产品中的一种有毒性的中间体[5]。作为一种工业污染物,释放到环境中的4-硝基酚容易对生态产生恶劣的影响,且微量的4-硝基酚就能损害人体的中枢神经系统、血液、肝脏和肾脏。4-硝基酚在工业废水中具有高度的稳定性,难以通过自然降解去除。然而,通过催化加氢[6]可以将环境致癌物4-硝基酚转化为具有药用价值的4-氨基酚。因此,研发一种高效的4-硝基酚加氢催化剂具有显著的经济和生态价值。
目前,金属催化剂在催化加氢中的应用十分广泛[7]。VIII 族金属如Rh、Ru、Pt 和Ir 是众所周知的优良加氢催化剂。有研究[8]发现,在苯乙炔加氢中,Pt 基单金属催化剂展现了高的苯乙炔加氢活性,而Ru 纳米颗粒催化剂具有较高的苯乙烯选择性(≈98%),但它的活性非常低。由于单金属催化剂通常伴随活性高但选择性低或选择性高但活性低的问题,可以通过掺杂第二金属对其进行修饰来弥补这些缺陷。与单金属催化剂相比,双金属体系具有独特的活性中心;由于电子效应和几何效应的存在,双金属催化剂可使目标产物的产率更高,并且表现出更稳定的性能[9-10]。已有研究证明,在相同的条件下,双金属纳米颗粒比单金属纳米颗粒具有更强的催化活性,该现象被称为“协同效应”[11]。Stucchi等[12]通过浸渍和溶胶固定化制备了活性炭负载的单金属Mo 和Pt;以Na2PtCl4为前驱体,PVA 和NaBH4为还原剂,以Pt 浸渍Mo-AC 催化剂制备了Pt/Mo 双金属。在糠醛的加氢中,Pt/Mo 双金属催化剂展现了比Pt 或Mo 单金属催化剂更高的活性,其中糠醛转化率为92%,糠醇和糠醚的选择性分别为20%和80%。单金属Mo/AC 催化剂尽管初始活性较低,但对糠醚表现出完全的选择性。
虽然Pt 在大多加氢反应中表现了高的催化活性,但因其昂贵的价格限制了Pt 催化剂的应用,因此,设计一种低成本同时又具备高活性的催化剂具有十分重要的工业意义。与金属Pt 相比,Ru 是一种更便宜的贵金属[13],且在催化加氢中也有着广泛的应用。在大量的Ru 中引入少量的Pt,通过RuPt双金属之间的协同作用实现更为优异的催化性能是一条可取的途径。
本文采用甲醇、乙醇作为还原溶剂的溶剂热法将Ru、Pt 负载在活性炭上,制备Ru/C、Pt/C 单金属催化剂和RuPt/C 双金属催化剂。对催化剂的成分分布进行表征分析,并研究其在苯乙炔选择性加氢为苯乙烯和4-硝基酚加氢为4-氨基酚反应中的催化性能,以探究双金属的协同作用对催化加氢的影响。
1 实验
1.1 试剂及仪器
活性炭粉末,分析纯,国药集团化学试剂有限公司;氯铂酸钾,纯度(质量分数)≥99%,北京华威锐科化工有限公司;三氯化钌水合物,ω(Ru)≥37%,上海麦克林生化科技有限公司;硼氢化钠(98%)、苯乙炔(97%)、无水乙醇、甲醇、乙腈和4-硝基酚等均为市售分析纯试剂。
气相色谱仪,日本岛津2014C 型;双光束紫外分光光度计,北京普析通用仪器有限责任公司TU-1901 型。
1.2 催化剂制备
将200 mg 氯铂酸钾粉末加入20 mL 超纯水中,在80℃下保温30 min,使其充分溶解,得到浓度为10 mg/mL的氯铂酸钾水溶液。将0.254 mL 10 mg/mL的氯铂酸钾水溶液、1.27 mL 20 mg/mL 三氯化钌水溶液和211.5 mg 活性炭粉末混合于反应釜内衬中,随后加入20 mL 无水乙醇和20 mL 甲醇。将混合悬浊液放置在220℃的水热箱中保温150 min,冷却后将悬浊液抽滤洗涤,将洗净的固体在60℃的真空干燥箱中干燥6 h后即得到负载量为5%的Ru95Pt5/C。用上述方法同样制得负载量为5%的Pt/C 和Ru/C,用于比对实验。
1.3 苯乙炔的催化加氢实验
在100 mL 反应器中加入10 mL 乙腈、20 μL 苯乙炔和10 mg 催化剂。向反应器中充入0.3 MPa H2,充3 次以排除空气,然后再充入0.3 MPa H2。在室温条件下反应,隔一段时间取出50 μL 反应液离心,用配备FID 检测器和WondaCap 5 毛细管柱的岛津2014C 气相色谱检测上清液中的成分。反应物的转化率为反应物的消耗量除以引入的总量,产物的选择性为产物的生成量除以反应物消耗的量。
1.4 4-硝基酚的催化加氢实验
在250 mL 反应器中加入20 mL 0.42 mol/L 硼氢化钠水溶液、20 mL 1.4 mmol/L 4-硝基酚水溶液、140 mL 超纯水和2 mg 催化剂,在20℃下搅拌反应80 min,隔一段时间取出3 mL 反应液,用紫外分光光度计测定400 nm 处的吸光度。在不同温度下的反应方法与上述类似,40℃、60℃、80℃下的反应均在恒温油浴锅中进行。为了检测催化剂的稳定性,还进行了循环试验。催化反应在20℃下反应80 min,循环一次后,对上清液进行检测,并用水将催化剂冲洗抽滤,将收集的催化剂重新分散至上述反应液中,进行下一轮催化反应。
2 结果与讨论
2.1 形貌及成分表征
用扫描透射电子显微镜(STEM)和能量色散X射线能谱(EDX)对5%Ru95Pt5/C 进行了分析,如图1所示。图 1(a)中的高角度环形暗场透射电镜(HAADF-STEM)图像显示样品中形成了纳米颗粒,且比较均匀地分布在活性炭上;Ru 和Pt 以及这2种元素叠加的EDX 面扫元素分布如图1(b)~(d)所示,证实了在单个纳米颗粒内,Ru 和Pt 均匀分布,没有出现明显的偏聚现象。综合图1 结果可以证实合成的产物为双金属纳米颗粒。

图1 5%Ru95Pt5/C 的形貌表征图Fig.1 Morphology characterization of Ru95Pt5/C
2.2 催化剂的苯乙炔加氢性能
图2 为负载量为5%的Ru95Pt5/C、Pt/C 和Ru/C催化剂在室温下苯乙炔加氢产物随时间的变化曲线。在该催化反应中,苯乙炔加氢的产物包括苯乙烯和乙苯。
如图2(b)所示,5%Pt/C 对苯乙炔加氢具有很高的催化活性。当反应时间为8 min 时,苯乙炔的转化率达到100%,此时苯乙烯的选择性为80%;随着反应时间的增加,苯乙炔的转化率保持在100%,而苯乙烯可进一步加氢转化为乙苯,因此苯乙烯选择性持续降低,乙苯的选择性逐渐增加;反应进行60 min 以后,苯乙烯几乎全部转化为乙苯,苯乙烯的最终选择性接近于零。与5%Pt/C 不同,5%Ru/C的催化活性很低(图2(c)),反应时间为90 min 时,苯乙炔转化率仅为6%,而苯乙烯选择性高达91%。
5%Ru95Pt5/C 在苯乙炔加氢中表现出相对优异的催化性能,如图2(a)所示。在反应100 min 后,苯乙炔转化率接近100%,此时苯乙烯选择性接近90%,随着反应的进一步进行,苯乙炔全部反应,苯乙烯的选择性略有下降,但由于下降速率十分缓慢,出现了一个平台期,当反应时间持续到200 min时,苯乙烯仍有77%的选择性。由上述结果可以得出,与5%Ru/C 相比,5%Ru95Pt5/C 催化剂由于有Pt的加入表现出更高的活性,Pt 是催化的活性中心。此外,相比于5%Pt/C,5%Ru95Pt5/C 催化剂具有更高的苯乙烯选择性,这来源于Ru 对催化选择性的调控。因此,5%Ru95Pt5/C 由于Ru 和Pt 双金属的协同效应,在苯乙炔加氢反应中同时具有优异的活性和选择性。

图2 不同催化剂的苯乙炔加氢反应曲线Fig.2 Reaction curve of hydrogenation of phenylacetylene over different catalysts
2.3 催化剂的4-硝基酚加氢性能
在4-硝基酚加氢反应中,以硼氢化钠作为氢源,4-硝基酚中苯环上的-NO2被-NH2取代。反应前,4-硝基酚溶液为黄色,而加氢后的产物4-氨基酚溶液呈无色,因此可以用紫外分光光度法来评价该加氢反应的程度。图3为5%Ru95Pt5/C、5%Pt/C和5%Ru/C三种催化剂在20℃下的加氢动力学曲线。
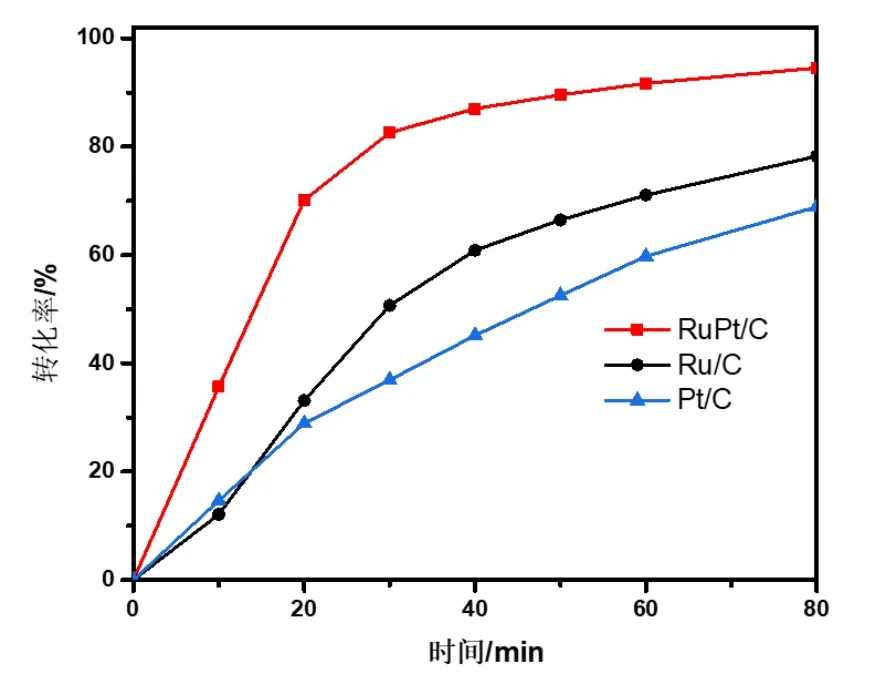
图3 4-硝基酚在5%Ru95Pt5/C、5%Pt/C、5%Ru/C 催化下的时间-转化率曲线Fig.3 Time-conversion curves of 4-nitrophenol catalyzed by 5%Ru95Pt5/C, 5%Pt/C and 5%Ru/C
由图3 可见,5%Pt/C 和5%Ru/C 作为催化剂时,在反应进行20 min 后,4-硝基酚的转化率约为30%,80 min 时,转化率仍低于80%。而5%Ru95Pt5/C在催化反应20 min 后,4-硝基酚的转化率约为70%,比单金属催化剂的转化率提高了一倍以上。随着时间的延长,转化率继续提高,但速度逐渐变缓。到80 min 时,其转化率达到95%以上。对比可以发现,与单金属负载的催化剂相比,双金属负载的催化剂催化加氢活性明显增加。
进一步研究了5%Ru95Pt5/C 在不同温度下的对4-硝基酚加氢具有不同催化活性,如图4 所示。随着温度的增加,反应速率明显增加,在80 min 时,不同温度下的转化率均达到95%以上。

图4 不同温度下5%Ru95Pt5/C 催化剂 对4-硝基酚的加氢转化率曲线Fig.4 Conversion curves of 4- nitrophenol hydrogenation over 5%Ru95Pt5/C catalyst at different temperatures
根据图4 催化剂在不同温度下的反应速率(k)和温度(T)计算拟合可以得到lnk和1/T的关系曲线,即Arrhenius 曲线,如图5 所示。
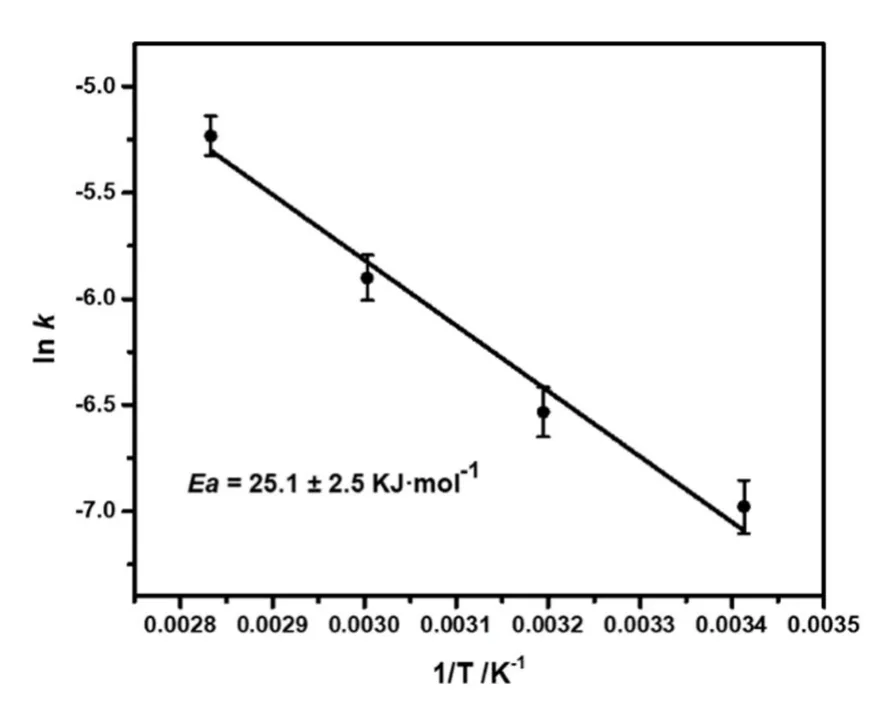
图5 4-硝基酚催化加氢反应的的Arrhenius 曲线Fig.5 Arrhenius curves for catalytic hydrogenation of 4-nitrophenol
由图5 可见,该曲线呈线性,表明该催化系统满足准一级动力学。根据Arrhenius 公式:

计算得到该反应活化能Ea=25.1±2.5 kJ/mol。
此外,进一步对5%Ru95Pt5/C 催化剂进行了重复使用性能测试,如图5 所示。经过5 次循环实验后,催化剂依旧具有很高的活性,4-硝基酚的转化率仍然有95%,没有明显下降。因此,该双金属催化剂除了显著的高活性外还具有良好的稳定性。这一高活性和稳定性的特点使其在化工和环保方面有较强的应用潜力。

图6 5%Ru95Pt5/C 催化剂的重复使用性能Fig.6 Reusability of 5%Ru95Pt5/C catalyst
3 结论
本文采用将甲醇和乙醇作为还原剂的溶剂热法,制备了活性炭上负载金属量为5%的Ru、Pt 及Ru-Pt 双金属催化剂。在苯乙炔的加氢中,单金属的Ru/C 的催化活性低;Pt/C 催化活性高,但是对苯乙炔的过度氢化导致了苯乙烯选择性过低;由于双金属的协同作用,Ru95Pt5/C 的活性和选择性都很高,既弥补了Ru/C 单金属催化剂活性低的缺陷,又改善了Pt/C 选择性低的问题。
在4-硝基酚的加氢实验中,Ru95Pt5/C 表现出比单金属更优异的催化活性。拟合计算得到的Ru95Pt5/C 加氢反应的活化能Ea=25.1±2.5 kJ/mol,此外,Ru95Pt5/C 还具有优异的稳定性能,催化剂在经过5 次重复使用后,仍保留了大于99%的初始活性。因此,Ru95Pt5/C 是一种兼备高活性、选择性和稳定性的加氢催化剂。有较强的应用潜力。

