双歧杆菌四联活菌片联合多烯磷脂酰胆碱治疗非酒精性脂肪性肝病34例*
周萍,张志勇,王佐兵,刘黎明
[1.鄂东医疗集团黄石市中心医院(湖北理工学院附属医院)感染科,黄石 435000;2.湖北省第三人民医院肝病科,武汉 430030]
非酒精性脂肪性肝病(non-alcoholic fatty liver disease,NAFLD)是指除酒料和其他明确的损伤肝因素外所致的肝细胞内脂肪过度沉积为主要特征的临床病理综合征,与胰岛素抵抗和遗传易感性密切相关的、获得性代谢肝损伤,其疾病谱包括非酒精性单纯性脂肪肝(SFL)、非酒精性脂肪性肝炎(nonalcoholic steatohepatitis,NASH)及其相关肝硬化和肝癌。随着生活方式的改变,NAFLD的发病率逐年上升,已成为当今发达国家和中国富裕地区慢性肝病的首要病因[1]。据流行病学数据显示,全球人群中NAFLD的发病率20%~30%,且15%~25%的NASH患者经10~15年最终可发展为肝硬化[2]。其发病机制尚未十分明确,但近年来,有研究表明NAFLD与肠道菌群失调有密切关系,从肠道菌群失衡出发治疗NAFLD具有重要临床意义[3]。目前益生菌联合护肝药治疗NAFLD的临床研究虽多,但其结论不一,临床疗效仍存在争议,且多数研究中益生菌选用双歧杆菌三联活菌胶囊。双歧杆菌四联活菌片能提供更合理肠道菌群,更有利于肠道黏膜屏障修复,促进毒素排出体外,更利于NAFLD患者及早恢复健康。多烯磷脂酰胆碱胶囊可提供大剂量容易吸收利用的高能多烯磷脂酰胆碱、维生素B等,多烯磷脂酰胆碱进入体内,可迅速与细胞器膜、肝细胞膜结合,成为生物膜的重要组成成分,提高生物膜的流动性、完整性及稳定性,从而提高肝细胞的自护能力[4]。本研究主要观察双歧杆菌四联活菌片联合多烯磷脂酰胆碱胶囊治疗NAFLD患者的临床疗效。
1 资料与方法
1.1临床资料 选取2018年1—12月在鄂东医疗集团黄石市中心医院门诊NAFLD患者64例,通过抛硬币法随机分为对照组30例及治疗组34例。对照组患者男21例,女9例;年龄22~66岁,平均年龄(43.50±11.86)岁;平均体质量指数(23.15±2.87) kg·(m2)-1;并发症:高血压9例,糖耐量异常4例,糖尿病4例;治疗组患者男24例,女10例;年龄23~68岁,平均年龄(43.97±11.89)岁;平均体质量指数(23.08±2.70) kg·(m2)-1;并发症:高血压8例,糖耐量异常5例,糖尿病3例。两组患者性别、年龄、体质量指数、并发症比较,均差异无统计学意义,具有可比性。
1.2纳入标准及排除标准 本研究通过鄂东医疗集团黄石市中心医院医学伦理委员会批准,患者及家属签署知情同意书。纳入标准:符合中华医学会肝病分会脂肪肝和酒精性肝病学组2010年修订的《非酒精性脂肪性肝病诊疗指南》的诊断标准[5];肝功能异常。排除标准:年龄<18岁;病毒性肝炎、酒精性肝病;自身免疫性肝病、药物性肝炎、肝豆状核变性等其他肝病及肝硬化或肝癌者;由肾脏疾病、自身免疫性疾病引起的高脂血症、脂肪肝者;合并心脑肺系统严重疾病者;合并恶性肿瘤者;合并精神异常或癫者;妊娠期及哺乳期妇女;对治疗药物过敏者;观察期服用其他药物者。
1.3方法 给予两组患者合理膳食指导,配合有氧运动。在此基础上,对照组予以多烯磷脂酰胆碱胶囊[赛诺菲(北京)制药有限公司,批准文号:国药准字H20059010,规格:每粒228 mg],口服,每次1粒,tid。治疗组在对照组基础上加双歧杆菌四联活菌片(杭州远大生物制药有限公司,批准文号:国药准字S20060010,规格:每片0.5 g),口服,每次3片,tid。疗程均为4周。
1.4观察指标 检测两组患者治疗前后肝功能[丙氨酸氨基转移酶(ALT)]、天冬氨酸氨基转移酶(AST)、谷胺酰转移酶(GGT)]及血脂[三酰甘油(TG)、总胆固醇(TC)]。肝功能及血脂采用西门子ADVIA2400型全自动生化分析仪及宁波瑞源生物科技有限公司生产的肝功能试剂(批号:2017121601)及血脂试剂(批号:2017122001)进行测定。
1.5疗效评价标准 显效:患者临床症状、体征消失,肝功能恢复正常;有效:患者临床症状、体征及肝功能指标均较前改善;无效:患者临床症状、体征无改善甚至加重,肝功能指标无改善甚至恶化。总有效率(%)=(显效+有效)/总例数×100%。
2 结果
2.1临床疗效比较 治疗后,治疗组总有效率为 91.18%,明显优于对照组(70.00%),差异有统计学意义(χ2=4.691,P=0.030);治疗组临床疗效以显效为主,有效次之,而对照组以有效为主,显效次之,两组患者疗效分布差异有统计学意义(U=-2.133,P=0.033)。 见表1。
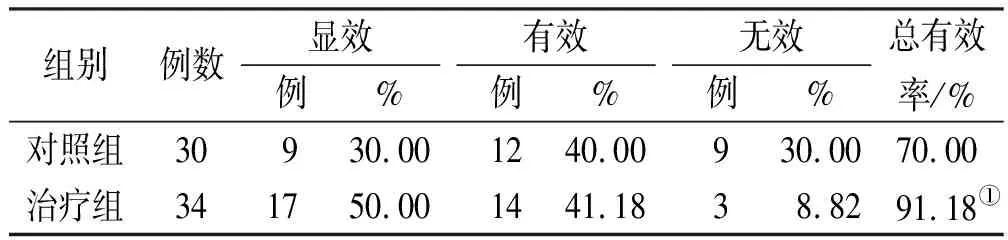
表1 两组患者临床疗效比较
2.2肝功能指标比较 治疗后,两组患者ALT、AST、GGT均较治疗前明显改善,治疗组患者治疗后ALT、AST、GGT改善明显优于对照组,均差异有统计学意义(均P<0.05)。见表2。
2.3血脂指标比较 治疗前两组患者TG、TC差异无统计学意义,治疗后两组患者TG、TC比较,差异无统计学意义(P>0.05)。见表3。
3 讨论
随着生活条件的改善,脂肪肝和代谢综合征患者越来越多,且发病年龄日趋年轻化。NAFLD已成为我国第一大慢性肝病和肝酶异常的首要原因,并且越来越多的慢性乙型肝炎患者合并NAFLD,严重危害生命健康[6-7]。NAFLD的发病机制复杂,临床护肝药物单用治疗效果欠佳,近年来不断有学者提出肠道益生菌的辅助治疗方案。肠道菌群因“肠-肝”轴与肝脏紧密相连,“肠-肝”轴这一概念指出肝脏与肠道之间存在多个相互作用方面,共同为对方的免疫完整性和固有性提供条件[8]。肠道黏膜屏障损伤是导致NAFLD的重要原因之一,刘涛等[9]对NAFLD大鼠进行研究,指出肠道黏膜屏障损伤后的大鼠体内内毒素、脂多糖等物质吸收增加,从而导致血中浓度增加,进一步激活炎症反应,促进并加重NAFLD大鼠的肝脏炎症和脂肪变性。益生菌可改善肠道黏膜生物屏障功能,利用益生菌改善肠道菌群结构有利于慢性肝病患者减少肝细胞脂肪沉积及减轻炎症反应。肠道微生态失衡致NAFLD的发病机制研究已成为一个新的热点,王伟等[10]对国内外相关文献报道进行总结,指出其发病机制可能包括干扰代谢、促进胰岛素抵抗、产生毒性代谢产物、增加肠壁通透性、激活肠道免疫、激活肝脏氧化应激及炎症等。有学者对SD大鼠进行研究,指出乳杆菌联合甘露寡糖能明显改善由高脂饮食引起的大鼠肝损伤和肝脏脂肪性病变[11]。何周桃等[12]研究指出,肠道菌群中双歧杆菌、乳杆菌等益生菌的菌落增多,可以有效缓解NAFLD患者的临床症状,改善肝功能及血脂水平。ALISI等[13]对48例NAFLD患者予以嗜酸乳杆菌口服4个月后,患者肝功能、血脂、BMI、胰岛素抵抗及肝脏影像学表现均明显改善。双歧杆菌四联活菌片为复方制剂,主要成分包括婴儿双歧杆菌、嗜酸乳杆菌、粪肠球菌、蜡样芽孢杆菌。人体正常肠道内的微生物有500多种,其中双歧杆菌、嗜酸乳杆菌、粪链球菌占绝对优势地位,因而双歧杆菌四联活菌片能提供更合理的肠道菌群,促进肠道微生态平衡,更有利于肠道黏膜屏障的修复。
表2 两组患者治疗前后肝功能变化
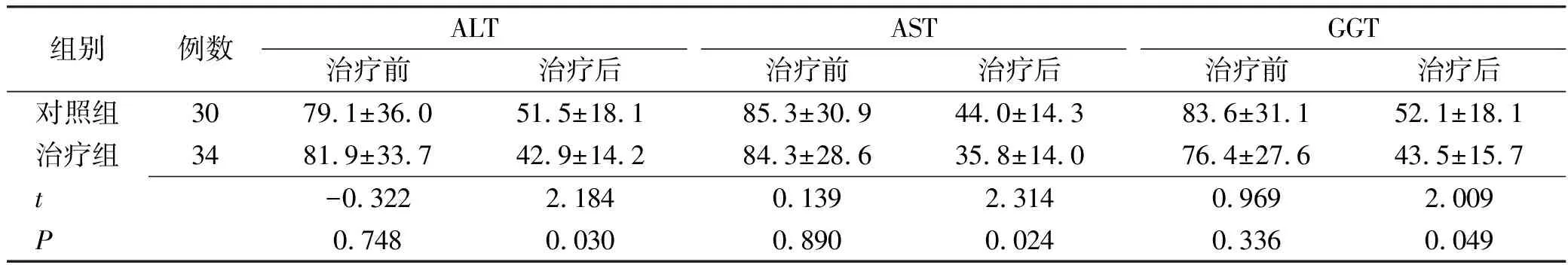
表2 两组患者治疗前后肝功能变化
组别例数ALT治疗前治疗后AST治疗前治疗后GGT治疗前治疗后对照组3079.1±36.051.5±18.185.3±30.944.0±14.383.6±31.152.1±18.1治疗组3481.9±33.742.9±14.284.3±28.635.8±14.076.4±27.643.5±15.7t-0.3222.1840.1392.3140.9692.009P0.7480.0300.8900.0240.3360.049
表3 两组患者治疗前后的血脂变化

表3 两组患者治疗前后的血脂变化
组别例数TG治疗前治疗后TC治疗前治疗后对照组302.51±0.952.19±0.755.46±0.885.20±0.97治疗组342.40±0.932.07±0.725.41±0.895.05±0.90t0.4910.6180.2160.608P0.6250.5390.8300.545
本研究中两组患者治疗后肝功能均明显改善,而血脂指标改善却不明显,考虑可能与疗程短,代谢状态的调整需要更长时间有关。此结论虽与上述学者研究不一致,但与林达等[14]研究结论类似,其研究指出,益生菌联合双环醇治疗脂肪肝,患者肝功能明显改善,但血脂、BMI未见明显改善。此外,赵庆卫等[15]对NAFLD患者进行长达6个月益生菌治疗后发现,患者BMI、腰围、TC等均明显改善,但仍有部分患者肝功能指标未完全恢复。郑丹等[16]对100例NAFLD患者进行研究,对照组仅予以低脂饮食加有氧运动,治疗组在此基础上予以双歧杆菌三联活菌胶囊口服,用药疗程为3个月,结果显示治疗组患者血脂(TC、TG)改善明显,而肝功能指标(ALT、AST、GGT)、肝脏硬度等改善不明显,此结论与本研究有所出入,考虑可能与益生菌的种类、疗程长短及是否联用护肝药物等有关。
综上所述,益生菌联合护肝药对NAFLD具有显著的临床疗效,能有效改善临床症状、体征及肝功能指标,值得临床推广,同时可进一步研究长疗程益生菌治疗对NAFLD患者血脂的影响,及肠道微生态在NAFLD中的更多应用。

