粗茎秦艽多糖GCP-1的分离纯化、结构表征及抗炎活性评价
于少朋,曾 锐,韩 珍,曾元莲,杨 玲,瞿 燕,秦旭华*
1.成都中医药大学药学院,四川 成都 611137
2.西南民族大学药学院,四川 成都 610041
秦艽为龙胆科龙胆属Gentiana(Tourn.) L.秦艽组(Sect.Cruciata Gaudin)多年生草本植物的干燥根,《中国药典》2020年版规定其法定来源为植物秦艽Gentiana m acrophyllaPall.、麻花秦艽G.stramineaMaxim.、粗茎秦艽G.crassicaulisDuthie ex Burk.或小秦艽G.dahuricaFisch.。其中粗茎秦艽主要分布于四川、贵州、云南、西藏等海拔2700~3800 m 的高山草甸、山坡草地、灌丛及林缘中,为中国西南地区秦艽的代表品种,也是人工种植和市场流通规模较大的品种[1]。秦艽始载于《神农本草经》列为中品,至今已有2000 多年的药用历史。秦艽是重要的中药,也是藏、蒙和彝等多民族用药,具有祛风湿、清湿热、止痹痛、退虚热的功效,中医用于治疗风湿痹痛、中风半身不遂、筋脉拘挛,黄疸等证[2]。目前认为秦艽的抗炎、抗风湿活性成分主要集中在其环烯醚萜类、黄酮类及三萜类等成分,其他成分研究较少。近年来,多项研究表明中药多糖同样具有生物活性,如抗凝血、抗氧化、免疫活性[3-5]等。目前秦艽多糖的研究甚少,主要有陈克克等[6]使用HPLC 测定了秦艽多糖的单糖组成,本课题组前期对粗茎秦艽多糖的提取优化进行了研究,本研究从粗茎秦艽中分离纯化制备多糖,运用光谱、色谱以及核磁共振等方法对其结构进行分析,并使用小鼠单核巨噬细胞RAW 264.7模型评价其抗炎活性,为粗茎秦艽多糖的进一步研究奠定基础。
1 材料与仪器
1.1 材料
粗茎秦艽采自四川阿坝州黑水县,经西南民族大学刘圆教授鉴定为粗茎秦艽G.crassicaulisDuthie ex Burk.的根。对照品D-甘露糖(批号140651-201502,质量分数99.4%)、L-鼠李糖(批号111683-201505,质量分数99.8%)、D-葡萄糖醛酸(批号140648-201505,质量分数99.8%)、D-半乳糖醛酸(批号111646-201506,质量分数99.8%)、D-无水葡萄糖(批号110833-201506,质量分数99.9%)、D-半乳糖(批号100226-201506,质量分数99.9%)、L-阿拉伯糖(批号150624-201507,质量分数 99.8%)、葡聚糖标准品(批号 140639-201203),均购自中国食品药品检定研究院;CCK-8检测试剂盒、肿瘤坏死因子-α(TNF-α)检测试剂盒和白细胞介素-1β(IL-1β)检测试剂盒(南京建成生物工程研究所);一氧化氮(NO)检测试剂盒(上海碧云天生物技术有限公司);碘甲烷(分析纯,北京化学试剂公司);DEAE-52 阴离子树脂、SephadexG-100 凝胶(上海源叶生物化学试剂有限公司);其他试剂均为分析纯级别。
1.2 仪器
GC-MS-QP2010 型气质联用仪(日本Shimadzu公司);EQUINOX 55 型傅里叶红外光谱仪(德国Bruker 公司);Waters 515 液相色谱仪(配置Waters 2410 示差检测器,Waters 公司);Agilent1260 型高效液相色谱仪(安捷伦科技有限公司);水相凝胶色谱柱TSK-GelG4000PWXL(300 mm×7.5 mm,10 μm,日本TOSOH公司);Bruker AVIII-600 NMR光谱仪(美国Bruker 公司);Elx808 型酶标仪(Bio-Tek 公司)。
2 方法
2.1 GCP-1 的分离和纯化
取干燥粗茎秦艽药材500 g,切段并打粉,过三号筛,加入10 倍量石油醚脱脂(30~60 ℃,6 h)。干燥后残留物加 14 倍量水超声辅助热水浸提(25 ℃超声20 min,80 ℃,1.5 h,2 次),提取液经脱脂棉滤过后,合并滤液,55 ℃真空浓缩至总体积的1/3;按4 倍体积加20% Sevage 试剂[二氯甲烷-正丁醇(4∶1)]除去蛋白质,重复几次,直至无明显蛋白质为止。浓缩,加入4 倍体积无水乙醇沉淀,4 ℃冷藏12 h,再进行离心(2000 r/min、15 min),然后用丙酮、乙醚洗涤,挥干,即得粗茎秦艽粗多糖。然后将粗多糖过DEAE-52 柱依次用蒸馏水和0.5、1 mol/L NaCl 溶液梯度洗脱,隔管检测吸光度(A)值(硫酸-苯酚法),收集洗脱的各组分,洗脱得到2 个多糖组分,即水洗脱组分和0.5 mol/L NaCl 溶液洗脱组分。0.5 mol/L NaCl 溶液洗脱组分经SephadexG-100 凝胶色谱柱纯化,用0.1 mol/L NaCl 溶液等度洗脱,透析后冷冻干燥得均一多糖GCP-1。
2.2 GCP-1 的总糖含量测定
通过改良的硫酸-苯酚法对总糖含量进行测定。以0.5 mg/mL 葡萄糖溶液为标准液,然后分别量取标准液0、10、20、30、40、50 μL 加双蒸水补足至100 μL 工作液,向工作液中加6%苯酚溶液200 μL,快速加入浓硫酸1.5 mL,混合均匀。于100 ℃的水浴锅中加热10 min,取出冷却,然后量取200 μL 加入96 孔板中,于490 nm 波长下检测A值,以对照品葡萄糖质量浓度为横坐标,A值为纵坐标绘制标准曲线。
2.3 GCP-1 的纯度和相对分子质量测定
色谱条件:TSK-GelG4000PWXL 凝胶色谱柱(300 mm×7.5 mm,10 μm),流动相为0.1 mol/L NaNO3溶液,进样量20 μL,体积流量0.6 mL/min,柱温与检测器温度均为40 ℃。
先将不同相对分子质量的葡聚糖标准品(5.0×104、8.0×104、1.5×105、2.7×105、6.7×105、1.4×106、2×106、5.3×106)配成2 mg/mL 的水溶液,用微孔滤膜(直径50 mm、孔径0.45 mL)滤过后进样,然后将样品配成2 mg/mL 的水溶液,过微孔滤膜(直径50 mm、孔径0.45 mL)后进样,测定样品的保留时间,以相对分子质量对数为纵坐标,以对保留时间为横坐标绘制标准曲线,根据线性回归方程计算样品相对分子质量。
2.4 GCP-1 的单糖组成分析
取2 mg GCP-1,加入3 mL 2 mol/L 三氟乙酸(TFA),密封,110 ℃水解6 h。加等体积的甲醇于水解产物中,并在减压情况下旋转蒸发干燥,重复上述过程几次以除去过量的TFA。取全水解液100µL,碱性条件下进行PMP 衍生化,衍生后除去多余的PMP,进行HPLC 分析。
色谱条件:采用Agilent Eclipse XDB-C18(150 mm×4.6 mm,5 μm)色谱柱;检测器为紫外检测器;进样量为10 μL;在245 nm 检测波长下,检测温度为35 ℃,以0.1 mol/L 磷酸盐缓冲液(pH 6.7)-乙腈(83∶17)为流动相,按体积流量1 mL/min 进行检测。
服务器:云服务器,Windows2008Server 服务器系统和Apache为平台,MYSQL数据库系统。
2.5 GCP-1 的红外光谱(IR)分析
称取干燥的GCP-1 样品约3.0 mg,与适量干燥的KBr 粉末置于玛瑙研钵中研磨均匀,压片,在4000~400 cm-1的范围内进行IR 扫描。
2.6 GCP-1 的甲基化分析
2.6.1 甲基化实验 称取GCP-1 样品约10 mg,通过碳二亚胺方法[7]将GCP-1 羧基还原,通过IR 确定羧基还原程度;根据文献方法[8],完全还原后的GCP-1 进行甲基化,通过IR 确定甲基化程度,甲基化完成后,进行酸水解和乙酰化衍生,采用气相色谱-质谱联用仪(GC-MS)进行分析。
2.6.2 质谱条件 连接处温度250 ℃;EI 离子源,电子能量70 eV,离子温度230 ℃;DB-5 石英毛细管柱(30 m×0.25 mm,0.25 μm),体积流量1 mL/min;升温程序为120 ℃保持3 min,然后在8 ℃/min 至250 ℃的温度下保持10 min;进样量1 μL。
2.7 GCP-1 的核磁分析
GCP-1(30 mg)溶解在1 mL D2O 中,并在25 ℃的Bruker AVIII-600 NMR 光谱仪上进行1H-NMR、13C-NMR、1H-13C HSQC 分析。
2.8 GCP-1 对小鼠单核巨噬细胞RAW264.7 的抗炎活性的影响
2.8.1 小鼠单核巨噬细胞RAW264.7 的增殖实验将指数生长期的小鼠单核巨噬细胞RAW 264.7 以4.8×105个/孔的密度接种在96 孔板中。加入不同质量浓度(10、50、100、200 μg/mL)GCP-1,每个样品质量浓度设置3 个平行组。参考文献方法[9],进行CCK-8 实验,通过酶标仪在570 nm 的波长下测量每组的A值,以细胞培养液处理细胞作为对照组,按公式计算细胞活力。
细胞活力=A570实验/A570对照
2.8.2 ELISA 法检测IL-1β、NO 和TNF-α 的水平将小鼠单核巨噬细胞RAW 264.7(1×105个/孔)接种到24 孔板中,用脂多糖(LPS)1 μg/mL 处理1 h后,加入不同质量浓度(10、50、100、200 μg/mL)的GCP-1。24 h 后,收集培养上清液。每个样品质量浓度设置3 个平行组,同时以细胞培养液处理细胞作为对照组。根据试剂盒说明书操作,用酶标仪在540 nm 的波长下测量每组的A值。根据A值,通过测定得到的标准曲线计算细胞培养上清液中抗炎因子TNF-α、IL-1β 和NO 水平。
2.8.3 统计学处理 实验结果以±s表示,应用SPSS 21.0 进行数据处理,数据的差异统计分析均采用单因素方差分析(one-way ANOVA)。
3 结果与分析
3.1 粗茎秦艽多糖的分离纯化
通过超声辅助热水浸提法提取,进行脱蛋白,浓缩,无水乙醇沉淀,然后用丙酮、乙醚洗涤,挥干,得粗茎秦艽粗多糖,得率为4.32%;粗多糖经DEAE-cellulose 柱色谱分离得到2 个组分:水洗脱组分、0.5 mol/L NaCl 洗脱组分,见图1。因水洗脱组分含量相对较少,故将0.5 mol/L NaCl 洗脱组分通过SephadexG-100 柱进一步纯化,得GCP-1,得率为3.48%。硫酸-苯酚法测得GCP-1 总糖质量分数为84.38%。如图2 所示,凝胶色谱法测定GCP-1 相对分子质量为6.87×104。GCP-1 的峰单一且对称,表明其纯度高且结构均匀,可用于后续的结构分析。

图1 粗茎秦艽粗多糖经DEAE-cellulose 柱的分离图Fig.1 Elution cruve of G.crassicaulis crude polysaccharide on DEAE-cellulose column
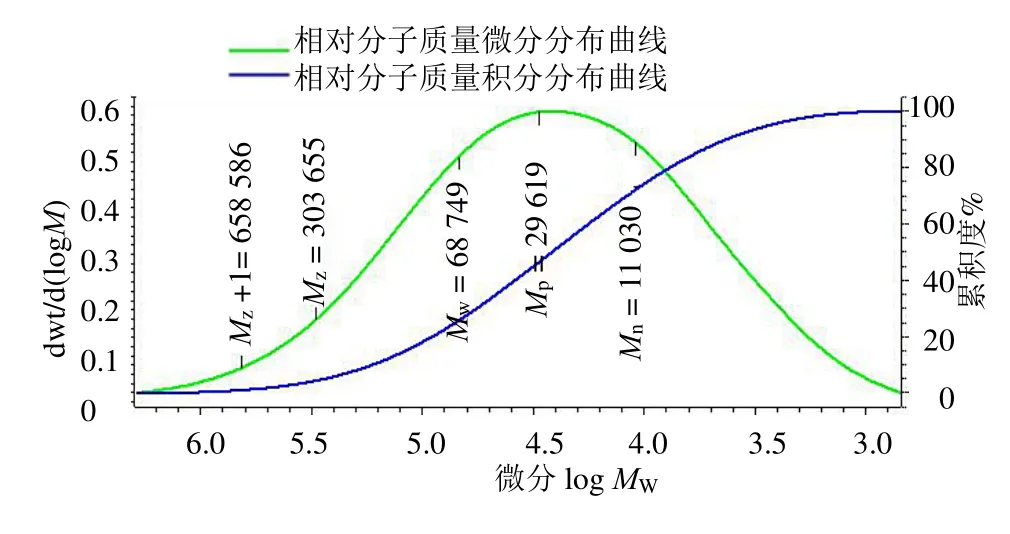
图2 GCP-1 高效凝胶色谱Fig.2 HPGPC of GCP-1
3.2 GCP-1 的结构解析
3.2.1 GCP-1 的单糖组成 如图3 所示,GCP-1 由甘露糖、鼠李糖、葡萄糖醛酸、半乳糖醛酸、葡萄糖、半乳糖和阿拉伯糖7 种单糖组成,其物质的量比为0.07∶3.07∶0.42∶1.98∶1.33∶5.22∶6.76。

图3 混合对照品溶液 (A) 和GCP-1 的单糖组成 (B) 的HPLC 分析Fig.3 Monosaccharide composition analysis of mixed standard and GCP-1 by HPLC
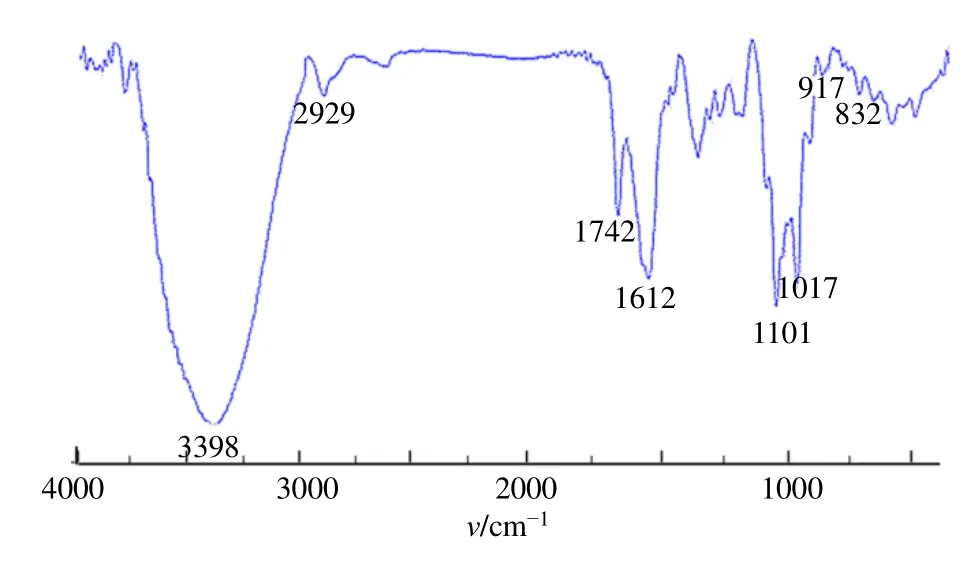
图4 GCP-1 的红外光谱分析Fig.4 FT-IR characterization of GCP-1
3.2.2 GCP-1 的红外光谱分析 GCP-1 的IR 光谱中,具有多糖的典型吸收带(图4)。在3600~3200 cm-1、3000~2800 cm-1处出现特征吸收峰[10]。GCP-1 在3398 cm-1处有一强而宽的吸收峰,该峰是由于羟基的伸缩振动形成,说明存在分子内、分子间氢键。2929 cm-1处是一弱的吸收峰,由C-H的伸缩振动造成[10]。1742 和1612 cm-1处的吸收峰由酯羰基(COOR)和羧酸酯(COO-)伸缩振动造成[11-12],表明GCP-1 是酸性多糖。GCP-1 在1541 cm-1处没有吸收峰,表明它不含蛋白质[13]。
3.2.3 GCP-1 的甲基化分析 GCP-1 经过脱羧基、甲基化、酸水解以及乙酰化之后进行GC-MS 分析,结果见表1。因为甘露糖和葡萄糖酸的含量低于甲基化分析方法检测限度,因此信号不明显。
3.2.4 GCP-1 的核磁分析 →2)-α-L-Rhap(1→和→2,4)-α-L-Rhap-(1→残基的确定:13C-NMR 谱(图5)中δ16.5 处的化学位移和1H-NMR 谱(图6)中δ1.24和1.16 处化学位移,以及HSQC 谱(图7)上δ16.8/1.22和16.6/1.16处的化学位移对应于α-L-Rhap的C-6/H-6,结合甲基化分析结果可知,GCP-1 含有→2)-α-L-Rhap(1→和→2,4)-α-L-Rhap-(1→残基[14-15];结合文献可知,→2)-α-L-Rhap(1→和→2,4)-α-LRhap-(1→残基表示GCP-1存在I型鼠李糖半乳糖醛酸聚糖(RGI)区域[16]。
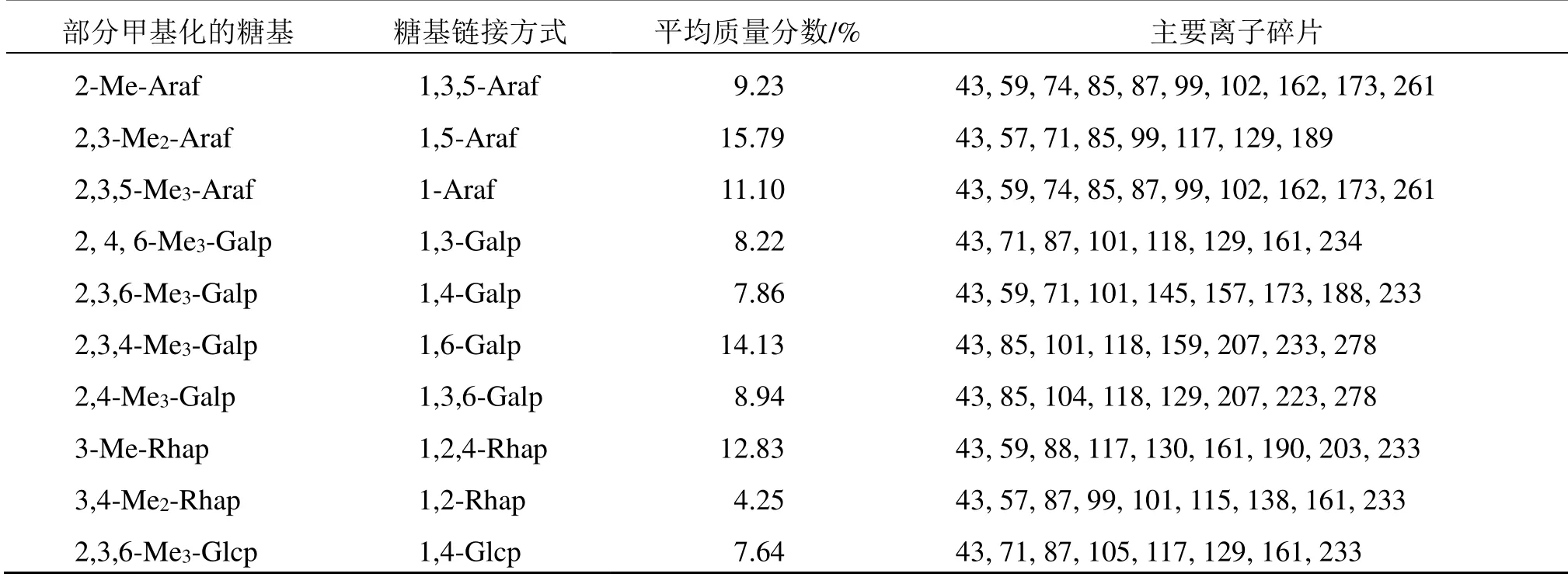
表1 GCP-1 的甲基化分析结果Table 1 Analysis of GCP-1 methylation

图5 GCP-1 的1H-NMR 谱Fig.5 1H-NMR spectrum of GCP-1
→4)-α-D-GalpA-(1→残基的确定:δ100.2/4.87,68.0/3.64,68.5/3.92,78.6/4.38,70.5/5.06 处的化学位移(图5、6)分别对应于→4)-α-D-GalpA-(1→的C-1/H-1、C-2/H-2、C-3/H-3、C-4/H-4,C-5/H-5[15]。结合文献可知,GCP-1 存在高半乳糖醛酸聚糖(HG)区域;在13C-NMR 谱(图5)中,→4)-α-D-GalpA-(1→残基酯化和未酯化C-1 的化学位移分别为δ100.0和99.4,对应C-6 处化学位移分别为δ170.6 和175.1,分别来自甲酯的羰基碳和羧基碳;酯化的甲基碳在δ52.8 处有信号[17-18]。HSQC 谱(图7)上化学位移δ20.5/2.09 和20.4/2.01 是典型乙酰基基团的信号[19]。综上可知,GCP-1 存在高半乳糖醛酸聚糖(HG),并且残基→4)-α-D-GalpA-(1→被部分甲基化和乙酰化。
α-L-Araf 基团的确定:13C-NMR 谱(图5)中δ106.3,106.8,107.4 处的化学位移均为α-L-Araf 基团的信号,结合HSQC 谱(图7)可知,δ106.8/5.16和106.8/5.07 处的化学位移分别对应于→3,5)-α-LAraf-(1→和→5)-α-L-Araf-(1→的C-1/H-1[17-18],→3,5)-α-L-Araf-(1→和→5)-α-L-Araf-(1→的大量存在表明GCP-1 存在阿拉伯聚糖[18,20-22]。
β-D-Galp 基团的确定:13C-NMR 谱(图5)中δ104.3 (C-1),77.6 (取代的C-4),74.4 (C-5),73.6(C-3),71.8 (C-2) 和61.0 (C-6) 处的化学位移以及HSQC 谱(图7)上δ102.7/4.42、103.9/4.56 和103.3/4.36 处的化学位移均属于β-D-Galp 基团,结合甲基化结果可知,大量的β-D-Galp 的存在表明GCP-1 存在I 型阿拉伯半乳聚糖(AGI)和II 型阿拉伯半乳聚糖(AG II),通常存在于侧链中[18,20-22]。
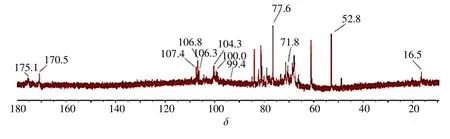
图6 GCP-1 的13C-NMR 谱Fig.6 13C-NMR spectrum of GCP-1
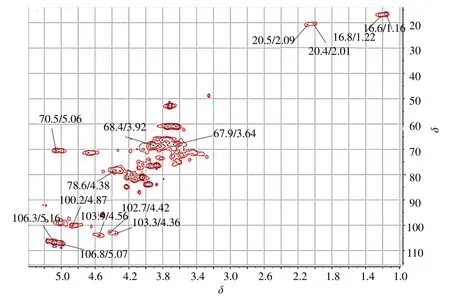
图7 GCP-1 的1H-13C HSQC 谱Fig.7 1H-13C HSQC spectrum of GCP-1
综上可知,GCP-1 是一种典型的果胶多糖,含有HG 和RG I 区域及AG I 和AG II 侧链。在碳谱中,δ100.0 和99.4 处为→4)-α-D-GalpA-(1→酯化和未酯化C-1 的化学信号值,对应C-6 处化学位移分别为δ170.6 和175.1,酯化羰基的甲基碳在52.8 处有信号,C-2~5 信号化学位移值依次为68.0、68.5、78.6、70.5;这些光谱数据表明存在甲基酯化的HG[17]。Vincken 等[16]研究发现HG 可能作为RGI的侧链存在。结合单糖分析中GalpA 含量不是很高,因此推测此多糖含有HG 区域,且可能作为RGI 的侧链存在。
3.3 GCP-1 对小鼠单核巨噬细胞RAW264.7 细胞增殖及分泌IL-1β、NO 和TNF-α 的影响
由图8 可知,GCP-1 对小鼠单核巨噬细胞RAW264.7 作用24 h 后,与对照组相比,GCP-1 在质量浓度为10、50、100、200 μg/mL 时均可显著促进小鼠单核巨噬细胞RAW264.7 细胞的增殖(P<0.01)。
由图9 可知,与对照组相比,LPS 能显着增加IL-1β、NO 和TNF-α 的产生;由图9-c 可知,与LPS组相比,GCP-1在质量浓度为10、50、100、200 μg/mL时均可显著抑制NO 的产生;如图9-a、b,随着GCP-1 质量浓度的增大,对TNF-α 和IL-1β 的产生抑制越大;在GCP-1 质量浓度为200 μg/mL 时对IL-1β、NO 和TNF-α 的抑制作用最大;说明GCP-1通过抑制细胞因子IL-1β、NO 和TNF-α 的产生发挥抗炎功能。

图8 GCP-1 对RAW264.7 细胞的增殖活性 (±s,n=3)Fig.8 Effects of GCP-1 on proliferation of RAW264.7 cells(±s,n=3)
4 讨论
GCP-1 经HPGPC 谱图分析为均一性多糖,其相对分子质量为6.87×104;由单糖分析表明GCP-1由甘露糖、鼠李糖、半乳糖醛酸、葡萄糖醛酸、半乳糖、葡萄糖和阿拉伯糖7 种单糖组成,其物质的量比依次为0.07∶3.07∶0.42∶1.98∶1.33∶5.22∶6.76;其中半乳糖醛酸、葡萄糖和阿拉伯糖含量比较高,甘露糖和葡萄糖醛酸含量较少;而同时GC-MS 和NMR 检测发现其含有由残基→4)-α-DGalpA-(1→构成的HG 区域,但单糖分析中GalpA含量不是很高,推测是该多糖RGI 的侧链可能含有HG;其同时含有由α-L-Araf 和β-D-Galp 基团组成的阿拉伯聚糖、AG I 和AG II 区域;这些都是典型的果胶多糖所具有的结构。通过体外细胞实验表明GCP-1 能明显增强RAW264.7 细胞的增殖,并能抑制RAW264.7 细胞TNF-α、IL-1β 和NO 的产生,呈现显著的抗炎活性。

图9 GCP-1 对RAW264.7 细胞释放TNF-α (a)、IL-1β (b) 和NO (c) 的影响 (±s,n=3)Fig.9 Effects of GCP-1 on TNF-α (a),IL-1β (b),and NO (c) of RAW264.7 cells (±s,n=3)
GCP-1 结构和抗炎活性的探讨,对于深入研究粗茎秦艽抗炎作用的物质基础具有重要意义。对中药均一多糖结构的研究,可为以多糖为主要成分的中药质量控制水平的提升奠定基础,避免现代标准中多采用的总多糖测定方法存在的抗干扰能力弱的问题。
利益冲突所有作者声明不存在利益冲突
——α-葡萄糖醛酸酶的研究进展*