一测多评法测定补心气口服液中7种成分的含量
张伯锋,王 杰,陈海燕(.济南市中医医院药剂科,济南 500;.济南市第五人民医院,济南 50000;3.广西卫生职业技术学院,南宁 53003)
补心气口服液由人参、黄芪、石菖蒲和薤白4味中药制成,主治气短、心悸、乏力和头晕等心气虚损型胸痹心痛病症[1]。现代研究表明,补心气口服液对慢性稳定型心绞痛[2]、慢性心力衰竭心气虚损证[3]、心血管神经症[4]、慢性肺心病急性发作[5]和冠心病心绞痛[6]等疾病的临床治疗效果显著,能有效改善心肌缺血和临床症状,减少心肌损伤,改善心肌供血,降低心肌耗氧和机体炎症反应,可提高患者的生活质量等。补心气口服液现行质量标准[1]和文献报道[7]仅对黄芪甲苷进行了定量检测,未对方中其他成分进行定量研究,中药及其制剂具有成分繁多复杂、协同作用的特点,单一成分控制模式难以确保中成药复方制剂临床疗效的一致性,多指标成分控制模式已广泛应用于其质量控制中。一测多评(QAMS)法利用中药成分间存在的内在函数关系,通过测定其中一种对照品稳定易得的成分,实现多指标成分含量的同时测定,降低检验成本,有助于多指标成分控制模式的普及应用。本研究参考中药质量标志物确认原则,以毛蕊异黄酮葡萄糖苷、毛蕊异黄酮、芒柄花素、人参皂苷Rg1、人参皂苷Re、β-细辛醚和α-细辛醚为研究对象,选取毛蕊异黄酮葡萄糖苷作为内参物,建立QAMS法同时测定补心气口服液中7种成分的含量,为全面评价补心气口服液的整体质量提供科学依据。
1 仪器与试药
1.1仪器 Waters 2695型高效液相色谱仪(美国Waters公司);Agilent 1100型高效液相色谱仪,Agilent Extend-C18色谱柱(250 mm×4.6 mm,5 μm)、Zorbax Eclipse C18色谱柱(250 mm×4.6 mm,5 μm),美国Agilent公司;Diamonsil C18色谱柱(250 mm×4.6 mm,5 μm),北京迪科马科技有限公司;XS105DU型电子分析天平(瑞士Mettler Toledo公司)。
1.2试药β-细辛醚(批号112018-201802,质量分数为99.3%)、α-细辛醚(批号100298-201203,质量分数为100.0%)、人参皂苷Rg1(批号110703-201933,质量分数为93.4%)、人参皂苷Re(批号110754-202028,质量分数为93.9%)和毛蕊异黄酮葡萄糖苷对照品(批号111920-201606,质量分数为97.6%),均购于中国食品药品检定研究院;毛蕊异黄酮(批号PRF8062601,质量分数为99.6%)和芒柄花素对照品(批号PRF8091225,质量分数为99.9%),均购于成都普瑞法科技开发有限公司;乙腈和甲醇为色谱纯,均购于天津市彪仕奇科技发展有限公司;其余试剂均为分析纯;补心气口服液(规格:10 mL·支-1;批号:190108,190509,190604),购于湖北福人金身药业有限公司。
2 方法与结果
2.1混合对照品溶液的制备 精密称取7种成分对照品各适量,分别用甲醇制成7种成分质量浓度分别为0.162,0.318,0.746,0.372,1.294,2.956,0.978 mg·mL-1的单一对照品溶液;精密吸取上述7种单一对照品溶液各2.5 mL,用甲醇定容至50 mL量瓶中,制成各成分质量浓度分别为8.1,15.9,37.3,18.6,64.7,147.8,48.9 μg·mL-1的混合对照品溶液。
2.2供试品溶液的制备 精密吸取补心气口服液2.0 mL,用甲醇定容至25 mL,过滤,即得。
2.3阴性样品溶液的制备 按照《中国药典》2015年版一部项下补心气口服液质量标准的工艺处方,分别制备缺人参、黄芪和石菖蒲的阴性样品,再按照2.2项下方法制成阴性样品溶液。
2.4色谱条件及专属性实验 色谱柱:Agilent Extend-C18色谱柱(250 mm×4.6 mm,5 μm)。流动相:乙腈(A)-1 mL·L-1磷酸(B),梯度洗脱(0~9.0 min,16.0%A;9.0~15.0 min,16.0%A~24.0%A;15.0~28.0 min,24.0%A~52.0%A;28.0~42.0 min,52.0%A~74.0%A;42.0~50.0 min,74.0%A~16.0%A)。流速:1.0 mL·min-1;检测波长分别为203 nm(0~15.0 min检测人参皂苷Rg1和人参皂苷Re)[8-12],257 nm(15.0~50.0 min检测毛蕊异黄酮葡萄糖苷、毛蕊异黄酮、芒柄花素、β-细辛醚和α-细辛醚)[13-18];进样量:10 μL;柱温:25 ℃。精密吸取2.1项下制备的混合对照品溶液、2.2项下制备的供试品溶液和2.3项下制备的阴性样品溶液各适量,按照上述色谱条件进样检测,色谱图见图1。由图1可知,供试品色谱图中7种成分色谱峰峰形对称,理论塔板数按照各成分色谱峰计算均不低于3 000,主成分峰与相邻色谱峰分离度均大于1.5,阴性样品对补心气口服液中7种成分的同时测定无干扰。

图1 HPLC图
2.5线性关系考察 分别精密吸取2.1项下制备的7种单一对照品溶液各0.1,0.5,1.0,1.5,2.0,2.5 mL,用甲醇制成6个系列质量浓度的混合对照品溶液,按照2.4项下色谱条件进样测定7种成分的峰面积,以质量浓度为横坐标(x)、峰面积为纵坐标(y),进行线性回归,结果见表1。

表1 各成分线性关系
2.6精密度实验 取2.1项下制备的混合对照品溶液,重复进样6次,测得7种成分峰面积的RSD值分别为1.29%,1.09%,0.96%,1.11%,0.62%,0.57%,0.79%,表明仪器精密度良好。
2.7重复性实验 取同一批补心气口服液,按照2.2项下方法平行制备6份供试品溶液,按照2.4项下色谱条件进样检测7种成分的峰面积,外标法(ESM)计算得7种成分含量的RSD值分别为1.78%,0.63%,1.39%,1.55%,1.02%,0.87%,1.14%,表明实验重复性良好。
2.8稳定性实验 取2.2项下制备的同一份供试品溶液,于制备后0,2,4,6,12,18 h进样检测7种成分的峰面积,结果7种成分峰面积的RSD值分别为1.04%,1.12%,0.93%,1.09%,0.66%,0.59%,0.82%,表明供试品溶液在18 h 内稳定性良好。
2.9回收率实验 取含量已知的补心气口服液9份,每份精密吸取1.0 mL,置于25 mL量瓶中,按照《中国药典》2015年版四部要求,分别按已知含有量的50%,100%,150% 3个水平精密加入混合对照品溶液(7种成分质量浓度分别为0.057,0.119,0.272,0.138,0.487,1.061,0.364 mg·mL-1)1.0,2.0,3.0 mL,各3份,再按照2.2项下方法制成加样供试品溶液,按照2.4项下色谱条件进样检测7种成分的峰面积,计算得7种成分的平均回收率(RSD)分别为97.44%(1.14%),99.80%(0.75%),100.05%(0.68%),96.98%(0.90%),98.87%(1.35%),99.88%(0.73%),97.91%(1.49%)。
2.10相对校正因子(RCFs)的计算及耐用性考察
2.10.1RCFs的计算 RCFs的计算公式:
fs/i=fs÷fi=(Xs×Yi)÷(Xi×Ys)
(1)
待测成分i质量浓度计算公式:
Xi=(Xs×Yi)÷(fs/i×Ys)
(2)
式中fs/i表示待测成分i的RCFs,X表示质量浓度,Y表示峰面积,s表示内参物,i表示其他待测成分。
精密吸取2.5项下制备的6个系列质量浓度的混合对照品溶液,进样检测7种成分的峰面积,以毛蕊异黄酮葡萄糖苷作为内参物,按照公式(1)计算其他6种成分的RCFs,结果见表2。
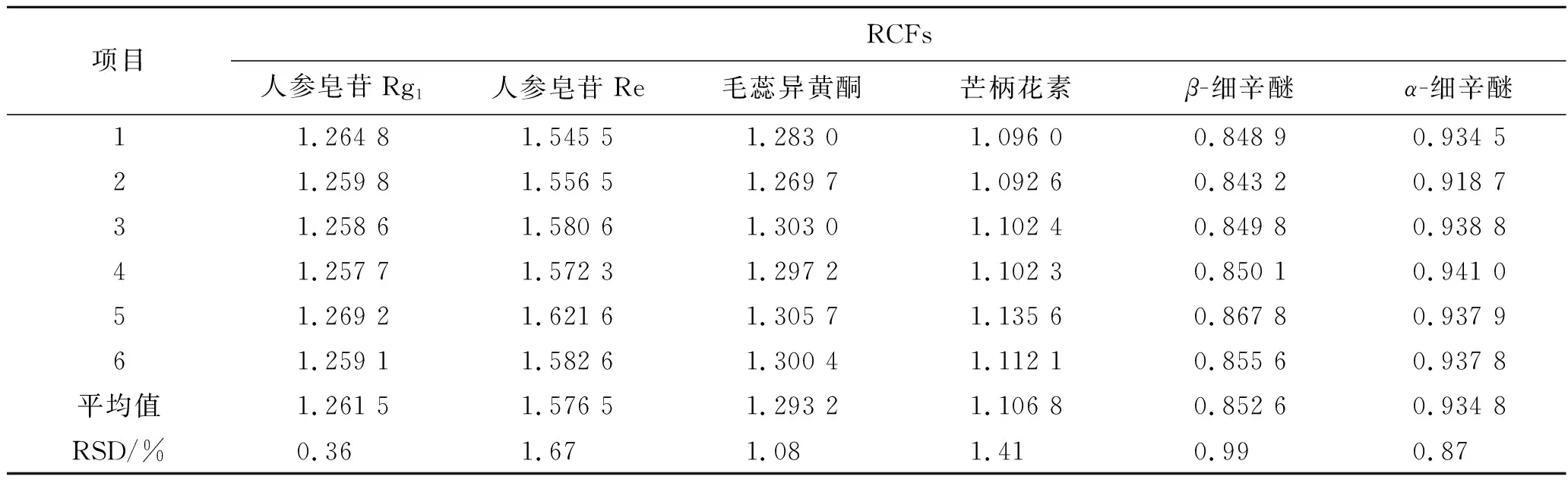
表2 各成分的RCFs
2.10.2不同仪器、色谱柱对RCFs的影响 精密吸取2.1项下制备的混合对照品溶液,按照2.4项下色谱条件进样检测7种成分的峰面积,考察Agilent 1100型、Waters 2695型高效液相色谱仪和Agilent Extend-C18(250 mm×4.6 mm,5 μm)、Zorbax Eclipse C18(250 mm×4.6 mm,5 μm)、Diamonsil C18(250 mm×4.6 mm,5 μm)色谱柱对RCFs的影响,见表3。

表3 不同仪器、色谱柱对RCFs的影响
2.10.3不同柱温对RCFs的影响 精密吸取2.1项下制备的混合对照品溶液,按照2.4项下色谱条件进样检测7种成分的峰面积,考察不同柱温对RCFs的影响,见表4。
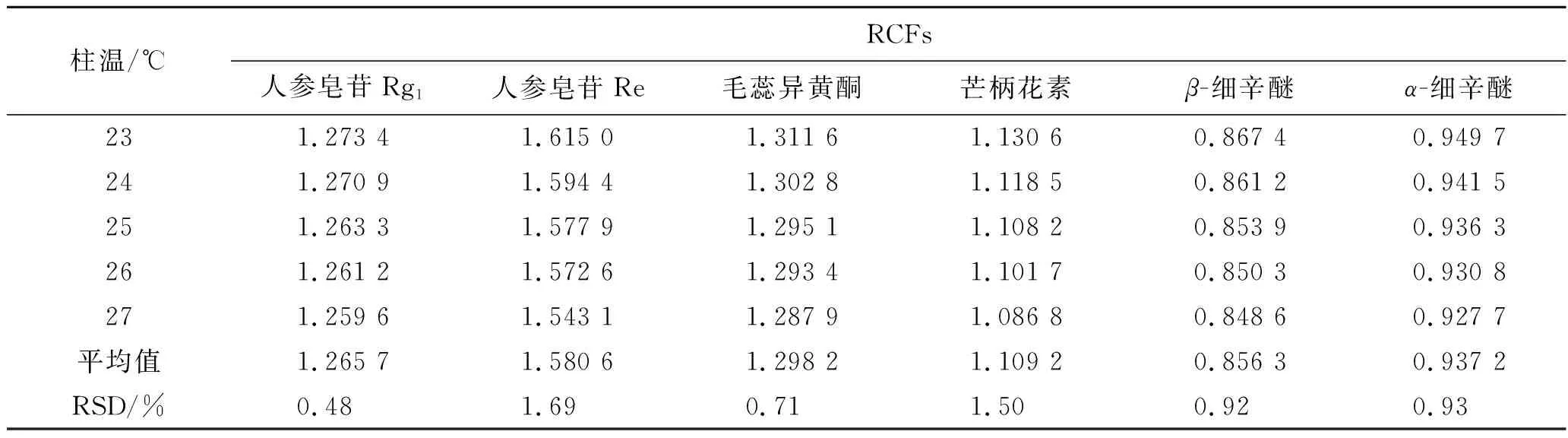
表4 不同柱温对RCFs的影响
2.10.4不同流速对RCFs的影响 精密吸取2.1项下制备的混合对照品溶液,按照2.4项下色谱条件进样检测7种成分的峰面积,考察不同流速(0.8,0.9,1.0,1.1,1.2 mL·min-1)对RCFs的影响,见表5。

表5 不同流速对RCFs的影响
2.11待测组分色谱峰的定位 相对保留时间值法是QAMS法中待测成分色谱峰定位的常用方法。本实验采用相对保留时间值法对待测成分色谱峰进行定位,分别记录不同仪器和色谱柱条件下7种成分的保留时间,结果见表6。

表6 不同仪器、色谱柱对相对保留时间值的影响
2.12样品含量测定 取3批补心气口服液,各批次按照2.2项下方法平行制备3份供试品溶液,按照2.4项下色谱条件进样测定7种成分的峰面积,首先采用ESM法计算7种成分的含量,再以毛蕊异黄酮葡萄糖苷作为内参物,按照2.10.1项下RCFs和公式(2)计算其他6种成分的含量,结果见表7。由表7可知,QAMS法计算值与ESM法实测值无明显差异,相对平均偏差(RAD)均<2.00%,表明RCFs可信度较高,建立的QAMS法可同时测定补心气口服液中7种成分的含量。
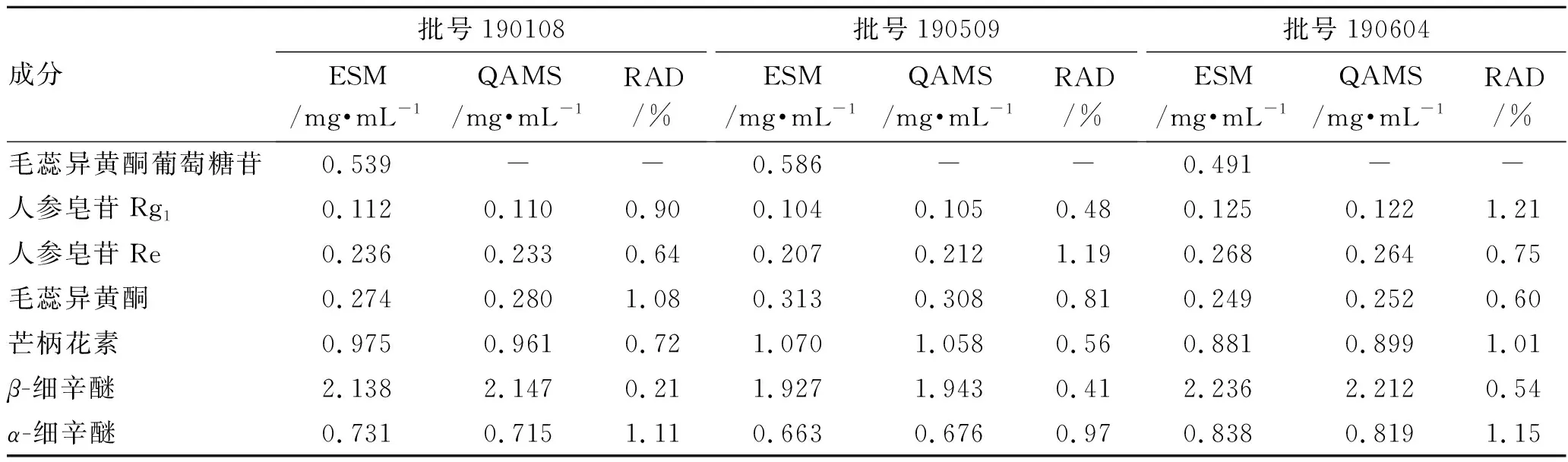
表7 7种成分的含量测定结果
3 讨论
3.1目标成分的选择 补心气口服液由黄芪、人参、石菖蒲和薤白4味中药材按照中医理论配伍制成,黄芪补气升阳、生津养血、行滞通痹,为方中君药;人参大补元气、生津安神,为臣药;石菖蒲化湿开胃、开窍豁痰、醒神益智,为佐药;薤白行气通阳,引药入心经,为使药。诸药共奏,以达补益心气、理气止痛的临床功效。现代研究表明,黄芪主要含有黄酮类、皂苷类、多糖类及微量元素等活性成分,其中毛蕊异黄酮葡萄糖苷、毛蕊异黄酮、芒柄花素和芒柄花苷等为其黄酮类代表性成分[19];人参的主要药效成分是人参皂苷,其中人参皂苷Rg1、人参皂苷Re和人参皂苷Rb1等为其代表性成分;石菖蒲主要含有β-细辛醚和α-细辛醚等挥发油类成分[20]。本文参考中药质量标志物优选原则,选取补心气口服液方中药物所含毛蕊异黄酮葡萄糖苷、毛蕊异黄酮、芒柄花素、人参皂苷Rg1、人参皂苷Re、β-细辛醚和α-细辛醚为定量测定目标成分。
3.2检测波长的确定 取2.1项下制备的7种成分的单一对照品溶液,分别在190~400 nm波长范围内进行紫外扫描,结果发现,毛蕊异黄酮葡萄糖苷、毛蕊异黄酮和芒柄花素在260 nm波长附近有较大吸收,且杂质干扰较少,灵敏度较高;人参皂苷Rg1和人参皂苷Re在203 nm波长处有最大吸收;β-细辛醚和α-细辛醚在257 nm波长处有最大吸收。综合考虑7种待测成分的检测响应值和杂质干扰程度,最终确定在203 nm波长处检测人参皂苷Rg1和人参皂苷Re,在257 nm波长处检测毛蕊异黄酮葡萄糖苷、毛蕊异黄酮、芒柄花素、β-细辛醚和α-细辛醚。
3.3流动相的选择 本实验参考相关文献,在选择流动相时,依次对甲醇-水[14,21]、乙腈-水[8-9]、乙腈-甲醇(9∶1)[13]3个流动相系统进行考察对比,结果发现,以甲醇-水和乙腈-甲醇(9∶1)为流动相体系检测时,基线漂移严重,部分待测成分色谱峰分离不完全,可能与甲醇在低波长处有紫外吸收有关;乙腈-水流动相体系检测色谱图基线平稳,但β-细辛醚色谱峰存在拖尾现象,考虑加入酸类改善,待测成分人参皂苷Rg1和人参皂苷Re为紫外末端吸收,甲酸[14,21-22]和冰醋酸为有机酸,存在紫外末端吸收,影响色谱图基线和检测结果,而磷酸为无机酸,无紫外末端吸收,遂采用乙腈-1 mL·L-1磷酸[9]为流动相进行实验,结果7种成分色谱峰峰形对称,与相邻色谱峰的分离度均大于1.5,色谱图基线较为平稳。同时对流动相比例不断优化,最终按照2.4项下的流动相洗脱程序对补心气口服液中7种成分的含量进行同时测定。
4 结论
本实验首次采用QAMS法对补心气口服液中人参皂苷Rg1、人参皂苷Re、毛蕊异黄酮葡萄糖苷、毛蕊异黄酮、芒柄花素、β-细辛醚和α-细辛醚的含量进行同时测定,所建立的方法操作简单、结果准确,对补心气口服液的质量标准提升和全面评价提供了参考。

