城市河道有机物、氮、硫污染物的分布规律研究
张肖静,位登辉,陈召,张楠,张红丽
郑州轻工业大学 材料与化学工程学院,河南 郑州 450001
0 引言
水是人类生存的基础物质之一,随着我国工业的快速发展,水环境的恶化和水资源的短缺造成水资源形势的日趋紧张.城市河道是城市生态系统的重要组成部分,承担着提供水源、防洪排涝、调节气候、降低污染等重要任务[1-2].然而,近年来随着工业化和城市化的迅速发展,大量工业废水及生活污水未经有效处理就直接排入城市河道,导致其生态系统遭到严重破坏,水体呈现季节性或者终年黑臭[3-5].国务院高度重视城市水体黑臭问题,2015年4月公布的《水污染防治行动计划》[6]强调,到2020年,地级及以上城市建成区黑臭水体控制在10%以内;到2030 年,基本消除城市黑臭水体问题.中华人民共和国住房和城乡建设部办公厅于2016 年2 月公布的黑臭水体名单显示,全国有73%以上的城市存在黑臭水体,共计1811 个,其中河流占85.3%[7].由此可知,城市河道的水体黑臭问题仍然十分严重,其生态修复是目前研究的重点.
有机物、硫酸盐、氨氮是导致城市水体黑臭的重要原因,明确这几种污染物在城市河道中的分布规律对于分析污染物的转化途径,以及进一步确定城市河道的生态修复策略至关重要[8-9].目前,关于城市河道污染情况的系统研究较少,尚不足以支撑河道生态修复策略的确定.因此,本文拟对淮河流域某城市河道的上覆水、孔隙水及底泥中的污染物分布特征进行研究,以期为确定城市河道生态修复方案及彻底解决河道污染问题提供数据支撑和理论依据.
1 材料与方法
1.1 主要试剂与仪器
主要试剂:(NH4)2SO4、NaNO2、KNO3,均为优级纯,阿拉丁试剂有限公司产.
主要仪器:TU-1810型紫外分光光度计,北京普析通用仪器有限责任公司产;Pro Plus型便携式水质参数测定仪,美国YSI集团产.
1.2 研究对象选取
选取淮河流域某城市河道为研究对象,所选区域段全长10.4 km.截至采样前,该段河道沿岸均有居民,其生活污水均未经处理直接排入河流,导致河道常年黑臭.在该段河道沿河水流向设置了5个采样点,如图1所示.
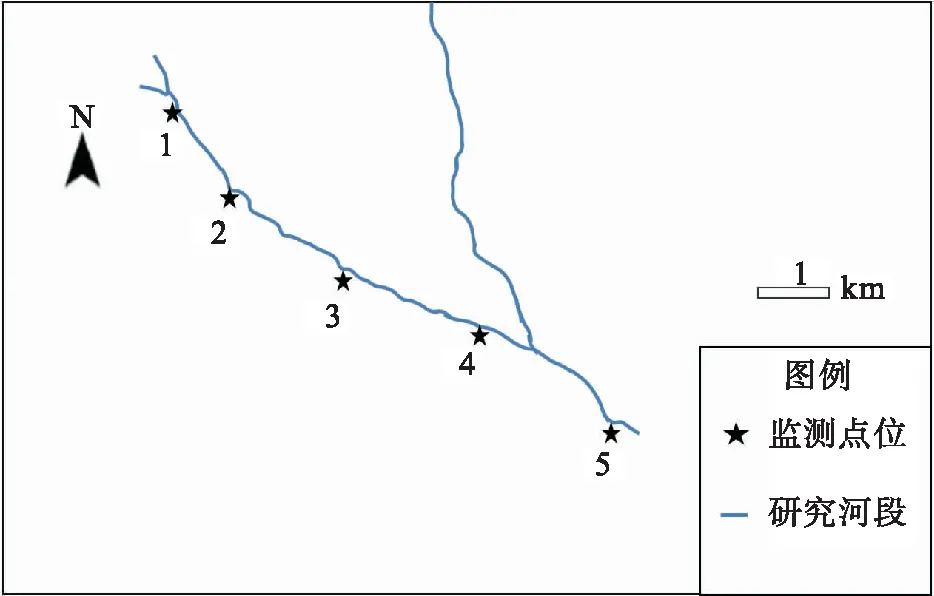
图1 采样点分布图Fig.1 Distribution map of the sampling point
1.3 实验方法
1.3.1 采样方法根据《水质采样方案设计技术规定》(HJ495—2009)[10]的相关要求,分别在5月份、8月份、11月份、2月份(分别代表春、夏、秋、冬4个季节)对图1所示的5个采样点进行采样.采样前,对采样点的pH值、溶解氧(DO)质量浓度、温度(T)等参数进行现场测定.之后,采用直立式采水器采集上覆水,并迅速转移到对应编号的带盖棕色储存瓶内.采用底泥采样器采集表层5 cm以下底泥样品,并转移到对应编号的带盖聚乙烯瓶内.样品采集完毕后带回实验室,于4 ℃冰箱内保存,待测.
1.3.2 底泥处理方法底泥静置2 h后,弃去上清液,在8000 r/min,20 ℃条件下离心15 min,提取上清液作为孔隙水样品测定污染物含量.剩余底泥在60 ℃条件下烘干后再自然风干,完全干燥后取出,冷却后碾碎至10目以下.将5 g筛后泥样倒入锥形瓶中,加入100 mL浓度为2 mol/L的KCl溶液,在振荡器上振荡48 h,以浸提底泥中的污染物,静置后取上层清液,待测[11].
1.3.3 分析方法分别采用纳氏试剂分光光度法、N-1-萘基乙二胺分光光度法、铬酸钡分光光度法、快速消解分光光度法测定样品中氨氮、亚硝酸盐氮、硫酸盐、COD含量,测定波长分别设置为420 nm、540 nm、440 nm、440 nm;采用紫外分光光度法测定样品中硝酸盐氮含量,测定波长设置为220 nm和275 nm.
2 结果与讨论
2.1 河水的理化指标检测结果
不同采样点、不同季节河水的理化指标参数如表1所示.由表1可知,河道上覆水温度在5月份和8月份较高.5月份,8月份,11月份,2月份的温度范围分别为23.0~23.9 ℃,27.9~29.0 ℃,12.4~18.7 ℃,14.0~15.2 ℃.由此可知,不同采样点的河水温度在春、夏、冬三季的分布相对均匀,不同采样点之间相差不大,但在秋季波动较大.这可能是由于河道沿线的化肥厂在11月份产量较大,排放污水较多,在不同地点排放的水量不同,影响到河水的水质参数.河水中的DO质量浓度可以直接反映河道的污染程度[12],在不同采样点、不同季节的分布变化较大.总体来说,夏季河水中的DO质量浓度最低,5个采样点均小于1 mg/L,这是由于夏季气温高,O2在水中的溶解度降低,另外较高温度下微生物的活性增加,消耗DO的速度加快,从而导致河水中的DO质量浓度降低.此外,从采样点来看,5#取样点的DO质量浓度总体低于4#采样点,这表明支流的汇入带来了更多的污染物,进而影响到采样河道中的DO质量浓度.由于周边生活污水的排入,河道的pH值在不同采样点、不同季节均处于中性偏碱性的范围,适合进行氨氮的氧化反应[13].因此,在DO充足的条件下,氨氮可以较快地氧化为硝态氮.
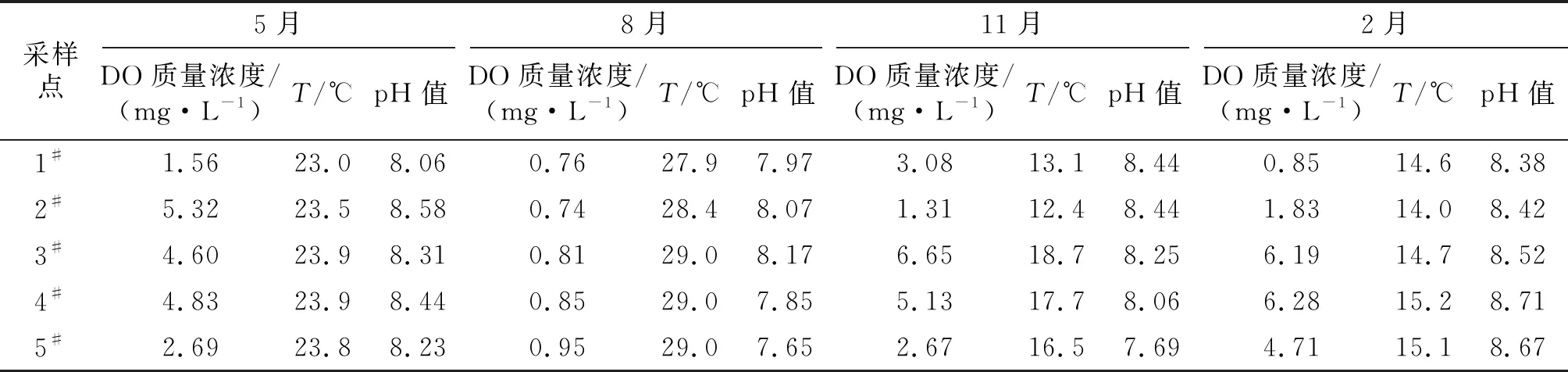
表1 不同采样点、不同季节河水的理化指标参数
2.2 河道中有机物的分布规律
河道上覆水、孔隙水和底泥中的有机物含量均以COD质量浓度表示,如图2所示.由图2可以看出,上覆水中COD质量浓度在不同季节的波动较大,5个采样点在不同季节的平均值分别为99.6 mg/L、70.3 mg/L、10.0 mg/L和18.4 mg/L.这主要是因为春季和夏季居民用水量较多,生活污水排放量较大,因此COD质量浓度相对于秋季和冬季较高.同时,由于夏季河水中DO质量浓度较低,限制了有机物的降解速率,因而更易导致水体黑臭现象的发生.孔隙水中的COD质量浓度在不同季节也有较大的差异,其中,春季COD质量浓度最高,为85.2 mg/L,而夏季COD质量浓度最低,仅为21.2 mg/L.同时,夏季底泥中COD含量也较低,仅为 0.57 mg/g.这再次说明,夏季微生物的活性较高,不但可加速有机物的氧化,同时也消耗了DO,而DO的不足,又限制了排入上覆水中的有机物的完全降解.该研究结果与DO质量浓度在夏季最低的结果一致.在冬季,虽然上覆水和孔隙水中COD质量浓度均有所降低,但底泥中COD含量显著增加,从秋季的0.61 mg/g增加到1.54 mg/g.由表1和2.1部分分析可知,冬季温度较低,河水温度仅为15 ℃左右,而底泥温度可能更低,这限制了微生物的活性,大量的有机物被吸附在底泥中而没有被进一步降解.虽然该季节的DO质量浓度较高,但也从侧面反映了微生物并没有充分消耗掉DO.此外,有机物的变化与反硝化过程有较大的关联[14],反硝化过程也会影响COD的变化,当COD充足时,反硝化过程会及时消耗硝态氮.
通过以上分析可知,春夏两季的排水量较大,河道中有机物的质量浓度较高,特别是夏季温度较高,可以及时转化COD,因此底泥和孔隙水中COD含量均较低.秋冬两季虽然没有大量的废水排入,上覆水中COD质量浓度较低,但污泥吸附有机物后不能及时将其氧化,导致孔隙水中COD质量浓度较高,且底泥中COD含量在冬季达到最高.由此可知,上覆水中的有机物更多受到排水、降雨等的影响,而孔隙水和底泥中的污染物则主要受微生物活性的影响.
2.3 河道中氮污染物的分布规律
在不同季节的采样点中均没有检测到亚硝酸盐氮,氮污染物以氨氮和硝氮为主,不同季节河道中氨氮、硝氮含量变化情况如图3所示.
由图3a)可知,在不同季节,氨氮在上覆水中的质量浓度均较低,为12.6~28.4 mg/L,在孔隙水中的质量浓度均较高,为 34.3~173.7 mg/L.
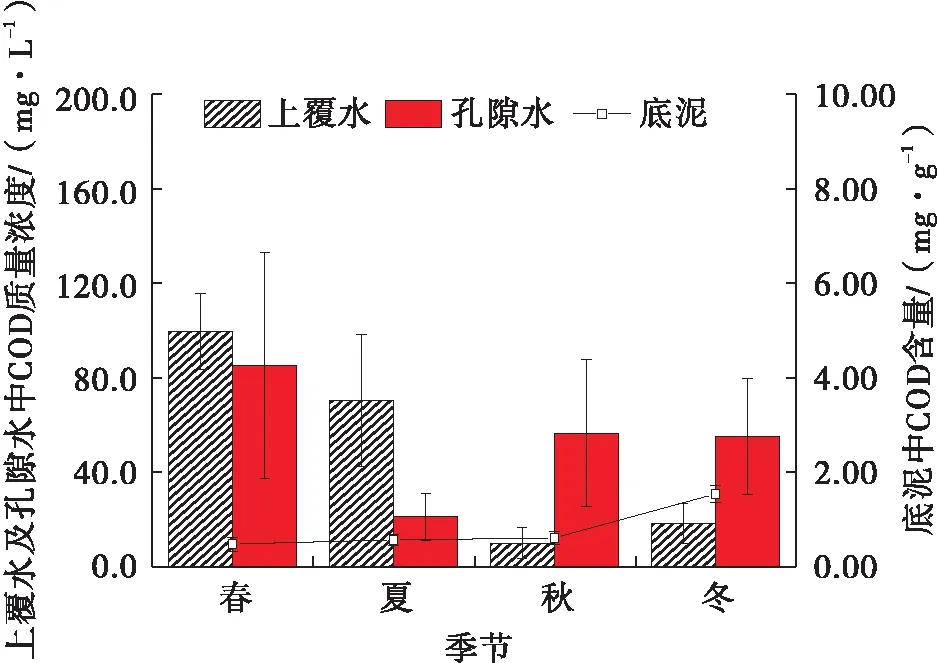
图2 不同季节河道中COD含量变化情况Fig.2 Changes of COD content in channels in different seasons
4个季节孔隙水中氨氮与上覆水中氨氮比值分别为7.0、7.5、2.7、1.6.这说明氨氮主要存在于孔隙水中,该部分氨氮是由河水中污染物的沉降及污泥的吸附-解吸作用产生的,是长年累月的积累,而上覆水中的氨氮质量浓度较低,主要受废水排放和降雨的影响.氨氮是由底泥缓释到孔隙水中的[15],春季和夏季孔隙水中的氨氮质量浓度最高,这是由于温度较高时,氨氮从底泥中解吸出来后没有及时被氧化,因而存在于孔隙水中.4个季节底泥中氨氮含量分别为0.62 mg/g、0.79 mg/g、1.34 mg/g、1.43 mg/g,总体变化趋势和孔隙水中氨氮质量浓度呈负相关,在春夏季较低,而在秋冬季较高.这是由于在温度较高的春夏季,各种微生物体内的酶活性提高,代谢加快,底泥中的氨氮能够快速氧化为硝氮,而在温度较低的秋冬季,微生物的代谢活动受到了抑制,因而底泥中的氨氮含量相对较高.这个结果进一步说明了孔隙水中的氨氮来自于底泥的释放.由此可知,底泥及孔隙水中的氨氮变化能够更加准确地反映河道的污染情况.
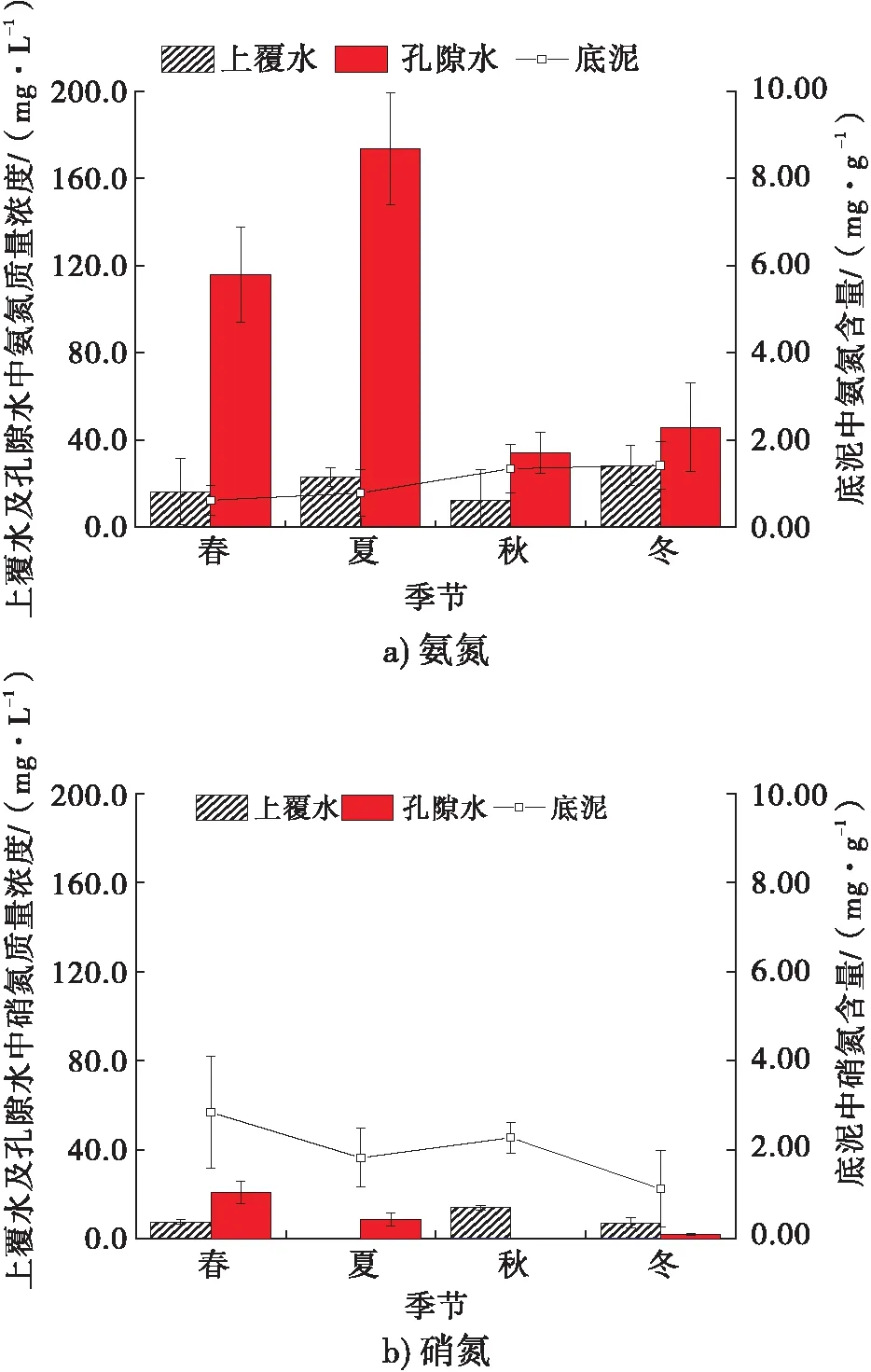
图3 不同季节河道中氨氮、硝氮含量变化情况Fig.3 Changes of ammonia nitrogen and nitrate nitrogen contents of the channel in different seasons
由图3b)可知,在不同季节,硝氮在上覆水和孔隙水中的质量浓度均较低.其中,在夏季的上覆水中几乎检测不到硝氮.这可能一方面是由于此时排入的污水以氨氮为主;另一方面,夏季河水中的DO质量浓度较低,会限制氨氮被氧化为硝氮.因此,硝氮主要存在于底泥中.在不同季节,底泥中硝氮含量分别为2.84 mg/g、1.82 mg/g、2.27 mg/g、1.12 mg/g,远远大于底泥中氨氮含量,说明底泥吸附的氮污染物以硝氮为主,这主要与微生物的转化过程有关.在冬季,底泥中硝氮含量有所降低,这可能是由于反硝化过程或内源硫反硝化过程将底泥中的硝氮还原[16];同时秋冬两季的氮污染物整体偏少,这与人们的生活、生产方式有关,在这两个季节,用水量减小,排污量减小,故河道中氨氮和硝氮的含量均降低.
通过以上分析可知,受排污量的影响,氮污染物的含量在春、夏两季较高.氨氮主要存在于孔隙水中,与底泥吸附-解吸作用密切相关,因而受温度影响较大;硝氮主要存在于底泥中,受微生物活性的影响较大,而底泥对氮污染物的缓释会严重影响河水的污染状况.因此,提高微生物的活性,促进氨氮的氧化和硝氮的进一步还原,对氮污染物的去除至关重要.
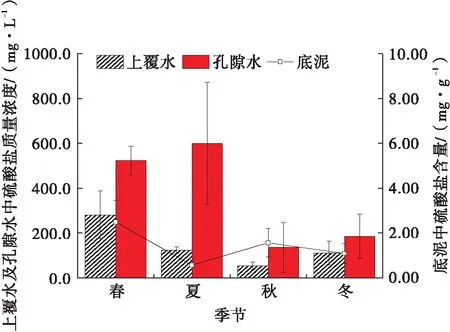
图4 不同季节河道中硫酸盐含量变化情况Fig.4 Changes of sulfate contents in different seasons
2.4 河道中硫酸盐的分布规律
不同季节河道中硫酸盐含量变化情况如图4所示.由图4可知,在不同季节,硫酸盐在孔隙水中的质量浓度均高于上覆水,表明硫酸盐主要存在于底泥孔隙中,而底泥对硫酸盐的吸附是发生在城市河道中的主要行为,这也是硫酸盐容易被还原,进而产生硫化氢等臭味气体的重要原因[17].夏季孔隙水中的硫酸盐质量浓度最高,达600.3 mg/L,而底泥中硫酸盐含量较低,仅为0.57 mg/g.这说明底泥中的硫酸盐在较高的温度下被解吸出来,进入到孔隙水中.硫酸盐主要来源于排泄物及工业废水,春季底泥中硫酸盐含量最高,达2.50 mg/g,这是由于春季温度相对较低,同时居民用水量大、排污量大,进入河道的硫酸盐量增多,这一方面会导致上覆水及孔隙水中硫酸盐质量浓度的提高,另一方面会导致底泥吸附大量硫酸盐,为夏季底泥中硫酸盐的解吸提供支撑.水中的硫酸盐不能完全还原,堆积到底泥中,导致孔隙水中的硫酸盐质量浓度升高.在秋冬两季,底泥中硫酸盐含量相对较高,但上覆水和孔隙水中硫酸盐质量浓度较低.整体而言,春季的硫酸盐总体含量高于其他季节.底泥中硫酸盐含量的升高表明,较低的温度更有利于底泥对污染物的吸附,上覆水及孔隙水中不能及时被微生物消耗的部分硫酸盐,会再次被底泥吸附.因此,对于硫酸盐而言,在春夏温度较高的季节,通过增强底泥活性,提高对孔隙水中硫酸盐的还原,是消除该污染物的关键.
此外,孔隙水中硫酸盐的质量浓度分布与氨氮的质量浓度分布呈现相关性.在春夏两季,孔隙水中氨氮和硫酸盐质量浓度均较高.孔隙水中的污染物含量反映了微生物转化过程的强弱,这一方面表明,氨氮和硫酸盐来自同一排污源;另一方面也反映底泥中可能存在同时转化氨氮和硫酸盐的反应,例如硫酸盐还原氨氧化反应,该反应可同时去除硫酸盐和氨氮,将氨氮转化为氮气,将硫酸盐转化为单质硫,从而使孔隙水中氨氮与硫酸盐的质量浓度变化呈正相关.关于该反应如何强化河道污染物的转化,以及对氮硫循环的贡献,仍需作进一步研究.
通过以上分析可知,不同季节河道中硫酸盐的变化趋势与氨氮一致,主要存在于孔隙水而非上覆水中,且在春夏两季含量较高.底泥中硫酸盐含量也较高,但在夏季由于底泥的解吸作用,硫酸盐含量最低.
比较几种污染物的分布可知,孔隙水中的污染物含量均高于上覆水,这说明底泥的缓释是河道污染的一个重要因素.强化底泥活性、增强氮硫循环,是彻底解决河道污染的关键.此外,底泥的解吸作用受温度影响较大,温度升高能够促进其对污染物的释放,因而应该选择在温度较高的季节强化微生物的活性.
3 结论
通过对某城市某段河道河水的理化指标参数,以及上覆水、孔隙水及底泥中有机物、氨氮、硝氮、硫酸盐等污染物的测定及分析可知:1)夏季水温最高,DO质量浓度最低,pH值始终处于8.0左右;2)上覆水中的有机物更多受排水、降雨等因素影响,而孔隙水和底泥中的有机物含量则受温度、DO和微生物活性等因素影响,底泥中的COD含量在冬季最高;3)氨氮主要存在于孔隙水中,且在春夏两季较高,硝氮主要存在于底泥中,强化底泥中氮的转化是彻底去除氮污染物的关键;4)硫酸盐在孔隙水中的含量均高于上覆水,且随季节的变化趋势与氨氮一致.总体而言,对城市河道的修复应该从底泥入手,提高底泥中相关微生物的活性,增强污染物的转化,同时,为了保证底泥中污染物的充分释放,应选择在夏季进行修复.

