HPLC-MS/MS法同时测定参附强心丸中制附子6种生物碱含量
刘言浩,梁大虎,孙 华,吴子静,张袁祥,李 超,董 健,李红金,韩诚正,谢海棠
(1.皖南医学院 研究生学院,安徽 芜湖 241002;2.皖南医学院第一附属医院 弋矶山医院 a.安徽省药物临床评价中心;b.中西医结合门诊,安徽 芜湖 241001)
参附强心丸为中成药名,由人参、附子(制)、桑白皮、猪苓、葶苈子、大黄组成。具有益气助阳、强心利水的作用。多用于慢性心力衰竭引起的心悸、气短、胸闷喘促、面肢浮肿等症状的治疗,收载于《中国药典》2015年版一部[1]。制附子作为参附强心丸中一项重要组成部分,具有回阳救逆、强心护心的作用[2-3]。然而其所含的生物碱成分既是药效物质也存在极大的毒性,过量服用会导致出现如室性心律失常等一系列危及生命的症状[4-6]。制附子含有的双酯型生物碱毒性极强,其中乌头碱成人致死量为2~5 mg,乌头碱、中乌头碱和次乌头碱的小鼠静脉给药的LD50分别为0.12~0.27、0.1~0.13、0.47 mg/kg。而作为其主要药效成分的单酯型生物碱也具有一定的毒性[7-10]。乌头类生物碱引起的中毒事件屡见不鲜,因此对含附子的药物制剂进行质量控制显得极为重要[11-14]。因此,建立参附强心丸的主要生物碱含量测定方法,对于确保参附强心丸安全性和有效性很有必要。本实验采用HPLC-MS/MS技术建立了参附强心丸中6种主要生物碱乌头碱(AC)、新乌头碱(MA)、次乌头碱(HA)、苯甲酰乌头原碱(BAC)、苯甲酰新乌头原碱(BMA)、苯甲酰次乌头原碱(BHA)的含量测定方法,为参附强心丸中制附子的质量控制提供参考。
1 材料与方法
1.1 仪器与试药 API4000质谱仪,Analyst1.6.2质谱数据处理软件(美国应用生物系统公司),METTLER TOLEDO ME55微量分析天平(德国赛多利斯公司);N-1001旋转蒸发仪(上海爱郎仪器有限公司);Thermo-21R高速离心机(赛默飞世尔科技有限公司)。AC(批号19062402,含量98%)、BAC(批号19070506,含量98%)、BMA(批号19062701,含量98%)、BHA(批号19090903,含量98%)购于成都思天德生物科技有限公司;MA(批号19062701,含量98.97%)、HA(批号28867,含量98%)购于MedChemExpress LLC;内标:氢溴酸高乌甲素(LH)(批号Z14N7B24783,含量98%),购于上海源叶生物科技有限公司;参附强心丸(天津中兴药业集团股份有限公司达仁堂制药厂,批号5150009、5150012、5150013)。乙酸铵和浓氨水为分析纯;乙醚、甲基叔丁基醚、乙酸乙酯、异丙醇、甲醇、甲酸等为色谱纯;水为去离子超纯水。
1.2 色谱及质谱条件
1.2.1 色谱条件 Agilent ZORBAX Eclipse XDB-C18(4.6 mm×150 mm,5 μm)色谱柱,流动相:70%乙腈-水(含0.1%甲酸、10 mmol/L乙酸铵),流速为0.5 mL/min,柱温30℃,进样量10 μL。
1.2.2 质谱条件 采用电喷雾电离源(ESI),正离子扫描,多反应离子监测模式(MRM)进行定量分析。各成分的质谱参数见表1。
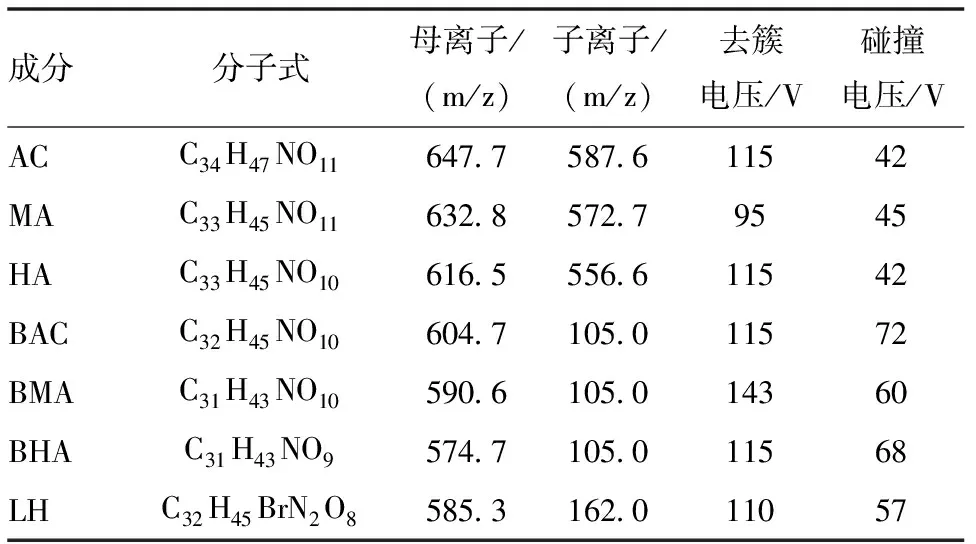
表1 各种成分的质谱分析参数
1.3 溶液的配制
1.3.1 对照品溶液的配制 分别精密称取AC、MA、HA、BAC、BMA、BHA对照品适量,置量瓶中,加甲醇定容至刻度,溶解得6.55、1.42、1.65、2.13、3.57、3.19 mg/mL的单一对照品储备液,精密量取各对照品储备液适量混合加纯甲醇稀释得6种生物碱的浓度分别为AC 0.655 9 mg/mL;MA 0.142 mg/mL;HA 0.165 mg/mL;BAC 0.213 mg/mL;BMA 0.357 mg/mL;BHA 0.319 mg/mL的混合对照品储备液,所有溶液均4℃保存。
1.3.2 内标溶液的配制 精密称取LH对照品适量,以甲醇溶解得浓度为0.128 mg/L的内标储备液。使用时,以甲醇进一步稀释得浓度为95 mg/mL的内标溶液,4℃保存。
1.3.3 供试品溶液的配制 取参附强心丸9丸,称重,计算平均粒重,剪成小块,混匀,精密称定0.1 g,置有塞锥形瓶中,加浓氨试液4 mL充分润湿,加乙醚40 mL,25℃以下超声(250 W,50 kHz)处理50 min,过滤,并用乙醚洗涤滤渣3次,每次10 mL,合并滤液后用旋转蒸发仪挥干溶剂,甲醇溶解残渣,转移并定容至10 mL量瓶中,摇匀。用0.45 μm微孔滤膜过滤得续滤液。
1.4 方法学考察
1.4.1 专属性 精密吸取供试品与对照品溶液各10 μL,按“1.2”色谱与质谱条件进行测定。在此条件下6种生物碱的出峰时间分别为AC 3.09 min;MA 2.93 min;HA 3.16 min;BAC 2.75 min;BMA 2.67 min;BHA 2.82 min;LH 2.68 min。对照品及参附强心丸供试品溶液的色谱图见图1。
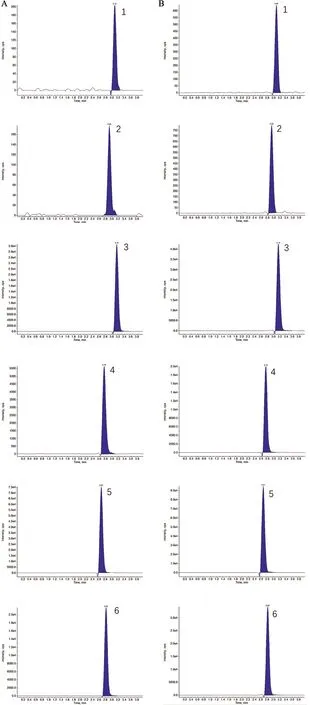
A.对照品;B.供试品;1.AC;2.MA;3.HA;4.BAC;5.BMA;6.BHA。
1.4.2 线性关系考察及定量下限测定 使用甲醇将“1.3.1”配置的对照品储备液按梯度稀释得对照品工作液。其中AC的线性浓度为1、2、4、6、8、10 mg/mL,MA的线性浓度为1、2、4、6、8、10 mg/mL,HA的线性浓度为10、20、40、60、80、100 mg/mL,BAC的线性浓度为120、240、480、720、96、1200 mg/mL,BMA的线性浓度为500、1 000、2 000、3 000、4 000、5 000 mg/mL,BHA的线性浓度为30、60、120、180、240、300 mg/mL,所有溶液均按“1.2”色谱与质谱条件进行测定,记录各分析物的峰面积AS和内标LH的峰面积AIS,以AS与AIS的比值Y为纵坐标,浓度X为横坐标,作加权线性回归计算权重系数为1/χ2,AC、MA、HA、BAC、BMA、BHA的最低检测限(LOD)、定量限(LOQ)、回归方程、回归系数等参数见表2,信噪比S/N均大于10。
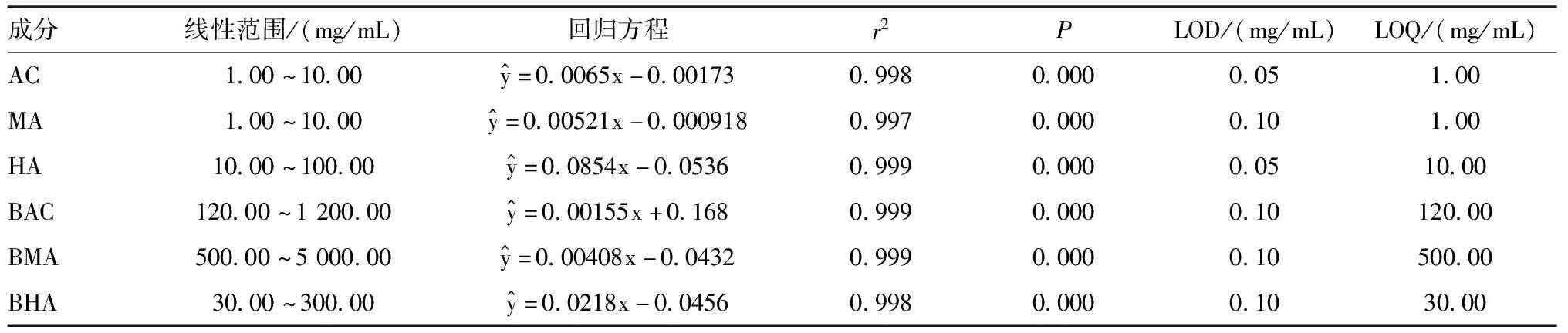
表2 各成分线性关系
1.4.3 精密度试验 按“1.2”色谱与质谱条件进行测定。对同一混合对照品溶液24 h内重复进样6次,6种生物碱成分的峰面积的RSD分别为AC 2.82%;MA 3.33%;HA 3.40%;BAC 3.21%;BMA 2.15%;BHA 2.54%,表明日内精密度良好。精密吸取“1.3.1”项下同一混合对照品溶液,每日进样1次,连续3 d,测得6种生物碱成分的峰面积的RSD分别为AC 4.20%;MA 3.70%;HA 1.93%;BAC 3.34%;BMA 2.63%;BHA 4.09%,日间精密度良好。
1.4.4 重复性试验 取批号5150013的参附强心丸6份,按“1.3.3”方法制备得供试品溶液6份,按“1.2”色谱与质谱条件进行测定。测得参附强心丸中6种生物碱成分的平均质量分数与RSD分别为AC:1.98 mg/mL、2.00%;MA:2.69 mg/mL、1.08%;HA:13.74 mg/mL、2.51%;BAC:341.50 mg/mL、1.38%;BMA:628.79 mg/mL、1.58%;BHA:44.97mg/mL、1.92%,重复性良好。
1.4.5 稳定性试验 取批号为5150013的同一供试品溶液,分别于0、1、2、4、6、8、10、12、24 h在上述条件进行测定。测得参附强心丸中6种生物碱成分的相对标准偏差分别为AC 3.06%;MA 1.76%;HA 2.08%;BAC 1.33%;BMA 0.73%;BHA 1.32%,供试品溶液在24 h内相对稳定。
1.4.6 加样回收率试验 取9份已知6种生物碱含量的参附强心丸(批号5150013),按6种生物碱含量的80%、100%、120%(同一比例配置3份)添加混合对照品溶液后按“1.3.3”项下制备供试品溶液,在上述条件下测定AC、MA、HA、BAC、BMA、BHA的平均加样回收率(n=6)分别为93.25%、95.28%、100.76%、96.92%、94.52%、96.37%;RSD分别为3.02%、3.66%、3.39%、1.69%、1.20%、2.44%。
1.5 数据分析 采用SPSS 18.0统计软件进行数据分析。采用t检验对标准曲线回归系数进行检验,P<0.05表明两参量间存在直线关系。
2 结果
精密称取3个批号的参附强心丸(批号5150009、5150012、5150013)各3份,按“1.3.3”项下制备,各成分含量结果如下。参附强心丸(批号5150009)中6种生物碱含量分别为AC 0.22 mg/kg,MA 0.29 mg/kg,HA 1.55 mg/kg,BAC 35.56 mg/kg,BMA 65.23 mg/kg,BHA 4.67 mg/kg。参附强心丸(批号5150012)中6种生物碱含量分别为AC 0.21 mg/kg,MA 0.25 mg/kg,HA 1.49 mg/kg,BAC 33.58 mg/kg,BMA 59.76 mg/kg,BHA 4.45 mg/kg。参附强心丸(批号5150013)中6种生物碱含量分别为AC 0.26 mg/kg,MA 0.35 mg/kg,HA 1.90 mg/kg,BAC 42.27 mg/kg,BMA 74.58 mg/kg,BHA 5.57 mg/kg。
有研究指出服用AC致成人中毒量为2 mg,为保证安全,AC每日服用量不得超过1 mg[12]。根据参附强心丸说明书中用法用量所述,每人每日最大服用剂量为6丸,按本实验中测得附子中6种生物碱最高含量计算,参附强心丸中6种生物碱每日最大服用量为AC 1.58 μg,MA 2.11 μg,HA 11.39 μg,BAC 253.6 μg,BMA 447.5 μg,BHA 33.43 μg,远低于中毒剂量。
3 讨论
3.1 色谱条件的确定 参考文献与待测物性质,考察了多种色谱柱与体系,最后确定采用Agilent ZORBAX Eclipse XDB-C18(4.6 mm×150 mm,5 μm)色谱柱,70%乙腈-水(含0.1%甲酸、10 mmol/L乙酸铵)系统,流速为0.5 mL/min,柱温30℃,进样量10 μL。6种生物碱在此色谱条件下的出峰时间分别为AC 3.09 min,MA 2.93 min,HA 3.16 min,BAC 2.75 min,BMA 2.67 min,BHA 2.82 min。
3.2 质谱条件的确定 本实验分别将各待测分析物及内标配制成1 mg/mL的溶液,用于注射泵连续进样,以优化质谱参数。采用电喷雾电离源(ESI),多反应离子监测模式(MRM)进行定量分析,并比较了正离子和负离子模式下离子峰强度,结果表明正离子条件下离子峰更稳定、强度最好。在正离子模式下,根据先前选定的母离子、子离子,组成离子对,做MRM扫描,分别优化DP、EP、CE、CXP等参数。
从检测结果来看,各批次间参附强心丸中6种生物碱的含量仍存在一定差异,在后续研发中是否将此类毒效兼具的物质进行定量控制是一个值得思考的问题。此外,虽然参附强心丸中AC的含量远远达不到中毒剂量,但考虑附子中其他成分毒性及累加后可能会导致的毒性增加,因此有必要对其进行进一步的质量控制。
本实验中建立的HPLC-MS/MS法较其他检测方法耗时短,能于4 min内快速分离检测出参附强心丸中的6种生物碱成分,方法简单、灵敏、准确,可为参附强心丸的质量控制提供科学依据。

