全自动分包机用于两种阴凉贮存药品调配的可行性研究*
蔡 琳,代贝贝,张慜媛,任刘丽,程 钢,宋 帅,钱芳芳,夏 泉
(安徽医科大学第一附属医院药剂科·国家中医药管理局中药化学三级实验室,安徽 合肥 230022)
自动分包机广泛应用于住院患者口服药物单剂量调配工作,可提高摆药速度,避免药品污染,减少摆药和发药差错率[1-2]。拆零药品改变药品外包装,保管贮存时易受温度、光线、湿度等影响,可能会影响药品的质量和安全[3]。阴凉贮存药品占全部药品种类的20%[4],部分阴凉贮存药品拆零后置分包机贮存缺乏相关管理标准。根据医疗机构药品拆零管理工作经验,发现头孢丙烯分散片(CDT)和阿莫西林克拉维酸钾分散片(ACDT)拆零变色时有发生,关于两药拆零分包尚缺乏系统研究[5-6]。本研究中以CDT和ACDT 2种阴凉贮存药品为例,开展其在全自动分包机贮存条件下的稳定性考察,分析药品外观和药物含量,为上述药品的拆零保存提供药品稳定性依据,同时也为阴凉贮存药品拆零管理提供参考。现报道如下。
1 仪器与试药
1.1 仪器
Xana-U4001型全自动分包机(日本东商株式会社);e2695-2489型高效液相色谱仪(美国Waters公司);D90型数码相机(Nikon公司,包括腾龙90mm微距镜头);BT25S型分析天平(赛多利斯科学仪器有限公司,精度为十万分之一);AT-Ⅱ-MTH-2型无线温湿度测量监控系统(武汉阿米特科技有限公司)。
1.2 试药
头孢丙烯对照品(批号为130567-201203;头孢丙烯Z异构体含量为85.9%,E异构体含量为9.2%),阿莫西林对照品(批号为130409-201509,含量为86.6%),克拉维酸对照品(批号为132025-201504,含量为94.9%),均由中国食品药品检定研究院提供;CDT(批号分别为2180018,2180020,2180026,白云山制药总厂);ACDT(批号分别为1806006,1807015,1808002,哈药集团制药总厂);甲醇(色谱纯,美国Tedia公司);磷酸二氢钠、磷酸二氢铵均为市售分析纯。
2 方法与结果
2.1 药品分组设计
选择CDT和ACDT开展稳定性考察。拆零药品稳定性研究分别在分包机机载药盒和周转盒贮存条件下开展,机载药盒不完全密闭、遮光并附带干燥剂,药品周转盒均已洗净、消毒、晾干且置遮光贮存柜。于28 d内动态评价药品外观和含量的变化。
2.2 环境温湿度监测
采用无线温湿度测量监控系统记录全自动分包机温湿度变化,考察时间为2019年2月8日至3月7日,监测记录显示全自动分包机所处调剂室环境温度为20~27℃,环境相对湿度为45%~55%。相对湿度符合规定,温度不符合阴凉贮存药品相关规定。
2.3 外观变化
我院中心药房全自动分包机中拆零药品实际周转周期为14 d,确定考察时间为28 d。每周观察药品外观并拍照记录,采用Image软件对药品外观进行数据标准化并得到药品外观灰度值。灰度值变化与观察周期间的变化趋势见图1。结果表明,机载药盒中CDT和ACDT均于第14天可见外观变化;周转盒储存条件下,CDT和ACDT分别在第14,21天外观发生改变。其中,CDT变黄,颜色变深;ACDT表面出现花斑,颜色变深。两药灰度值均随时间延长而增加。与周转盒相比,机载药盒贮存条件下药品灰度值变化趋势较快。
2.4 不同贮存条件下药物含量变化
参考2015年版《中国药典(二部)》[7]中2种药品含量测定方法,采用高效液相色谱法进行定量分析。色谱柱均为HypersilODS柱,流动相及其他检测条件:CDT以磷酸二氢铵溶液(取磷酸二氢铵20.7 g,加水1 800mL溶解,用磷酸调pH值至4.4)-乙腈(90∶10,V/V)等度洗脱,流速为1.0mL/min,检测波长为280 nm,柱温为30℃,进样量为20μL;ACDT采用磷酸二氢钠溶液(取磷酸二氢钠7.8 g,加水900mL溶解,用磷酸或氢氧化钠调节pH值至4.4±0.1,加水稀释至1 000mL)-甲醇(95∶5,V/V),等度洗脱,流速为1.0mL/min,检测波长为220 nm,柱温为40℃,进样量为20μL。CDT及ACDT质量标准规定其检测结果应分别为标示量的90.0%~110.0%和90.0%~120.0%。2种拆零药品的标准曲线和精密度试验结果见表1和图2。
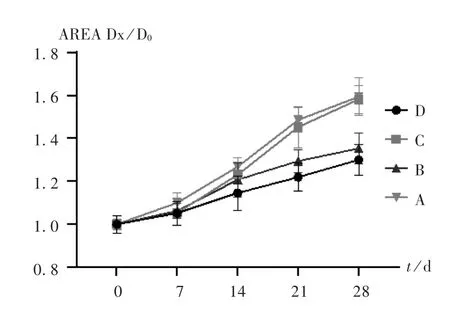
图1 不同贮存条件下头孢丙烯分散片(CDT)和阿莫西林克拉维酸钾分散片(ACDT)外观灰度值变化趋势图A.Themedicine box for storing CDT B.The turnover box for storing CDT C.Themedicine box for storing ACDT D.The turnover box for storing ACDTFig.1 Change trend of appearance and gray value of CDT and ACDT under different storage conditions
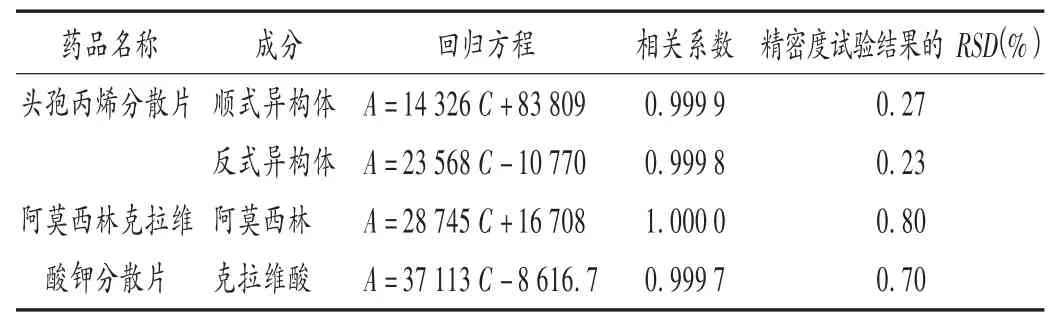
表1 两种药品的标准曲线考察和精密度试验结果Tab.1 Results of standard curve inspection and p recision test of the two drugs
结果表明,2种贮存条件下,头孢丙烯和阿莫西林含量测定结果(n=10)均在规定标示量范围内,且变化不大。在周转盒内的第28天,克拉维酸测定含量为标示量的89.80%;机载药盒条件下,第14天为91.98%,接近标准的临界值范围,第28天继续降至81.87%。ACDT作为复方制剂,在机载药盒贮存14 d时克拉维酸的测定值已接近标示量的临界值,且随时间的延长而递减,贮存28 d时克拉维酸降解显著且低于规定标示量;在周转盒条件下,克拉维酸贮存28 d时的测定含量略低于规定标示量。可见,CDT和ACDT在相同贮存环境下,周转盒药品贮存周期高于机载药盒。
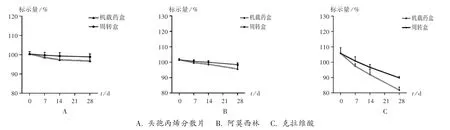
图2 头孢丙烯分散片及阿莫西林克拉维酸钾分散片含量测定变化趋势Fig.2 Change trend of content determ ination of CDT and ACDT
3 讨论
常温贮存药品拆零数量因实际消耗量而异。药品拆零后先放于周转盒,待机载药盒中药品消耗完毕,再将周转盒贮存药品转至机载药盒发放。本研究中,2种阴凉贮存药品在试验周期(28 d)内均发生外观改变,其中阿莫西林克拉维酸钾分散片出现含量明显降低。由于阴凉贮存药品需要特定贮存温度,且全自动分包机不具备阴凉贮存条件,推测阴凉贮存药品并不适用于全自动分包机拆零。因此,阴凉贮存药品不宜长期放于摆药机中,应现拆现用。
药品改变原包装后,其稳定性受较多因素影响。药品拆零后常见如下变化:外观性状改变;水分超标,尤其是易潮解药品;药物含量降低,甚至变质;微生物污染。这些变化均会导致药品有效期或保质期发生改变,药效降低或失效,甚至可能导致毒副作用增大[8-10]。对于青霉素类药物,青霉素Ⅰ型过敏反应抗原由半抗原(β-内酰胺环水解产物和侧链)结合人体血清或组织蛋白形成[11],阿莫西林克拉维酸钾分散片β-内酰胺类成分降解或可增加过敏等风险。
由于试验条件限制,本研究中仅考察了2种药品,且对拆零药品的稳定性研究仅涉及外观及含量变化,未对杂质限量、水分、微生物限度等予以考察,后期研究需进一步拓展稳定性考察指标及药物品种。
阴凉贮存药品不宜直接放于摆药机贮存,药品分包应依据当日使用量现用现拆,其他拆零药品应根据各自药品性质确定相应贮存环境和周期。全自动分包机或可依据药品稳定性增加阴凉贮存条件的配套设备,以进一步提升拆零药品的质量和用药安全。

