柠檬醛基抗油茶炭疽病菌衍生物的定量构效关系研究
曾 嵘, 司红燕, 陈尚钘, 宋 杰, 王宗德, 廖圣良*
(1.江西农业大学 林学院,国家林业和草原局木本香料(华东)工程技术研究中心,江西 南昌 330045;2.密歇根大学-弗林特 化学与生物化学系,美国 弗林特 48502)
油茶是具有很高综合利用价值的木本油料树种[1],在我国南方诸省都有广泛的种植,油茶产业是许多县市地方经济的重要组成部分[2-4]。油茶在生长的过程中容易受到各种病菌入侵,油茶炭疽病是油茶的主要病虫害之一[5],它会导致油茶树大量落果乃至树体死亡,严重影响油茶的产量和质量[6]。因而,油茶炭疽病的防治对于保障油茶的安全种植,稳定油茶产业的发展具有重要意义。目前对油茶炭疽病的防治方法主要是使用化学杀菌剂,但是长期使用现有杀菌剂会导致植物抗菌性增强、污染环境以及对人畜的健康造成威胁[7-8]。以天然产物为原料合成的抗菌剂在人畜安全与环境友好方面具有较大的优势。前人研究发现山苍子精油中的天然柠檬醛具有广谱的抗菌作用[9]。同时,天然柠檬醛具有芳香低毒、对环境友好以及容易改性的特点[10-12],因此以天然柠檬醛为原料开发防治油茶炭疽病的新型抗菌剂具有良好的开发应用前景。目前,已有研究报道了一些柠檬醛衍生物的合成及其对油茶炭疽病菌的抑制活性[13-14]。但是大部分衍生物并未体现出理想的抗菌活性,其根本原因在于柠檬醛衍生物的分子结构与抗油茶炭疽病菌活性之间的构效关系尚不明确,导致在设计衍生物的分子结构时,目标性差,分子结构设计过于简单。定量构效关系对于分析药物的结构和活性关系、药物前体的开发和优化有着不可估量的价值。目前,定量构效关系研究在药物领域[15]、农药领域[16-17]、化合物和材料的理化性质研究[18]等方面已有广泛应用。基于此,作者开展了柠檬醛基抗油茶炭疽病菌衍生物的定量构效关系研究,旨在为新型柠檬醛基抗油茶炭疽病菌衍生物的设计提供理论参考。
1 材料与方法
1.1 数据集的来源
从王喜男[19]和黄晶[20]的研究中获得了柠檬醛及其衍生物共计26个化合物的结构信息和对油茶炭疽病菌(Colletotrichumgloeosporioides)的抗菌活性数据:半数抑制浓度(IC50),具体见表1。1~21号化合物将用于QSAR模型的构建,22~26号化合物将作为外部检验集用于模型预测能力的检验。用对数函数来处理抗菌活性数据IC50,取lg(IC50)值作为本研究中构建模型时的因变量。
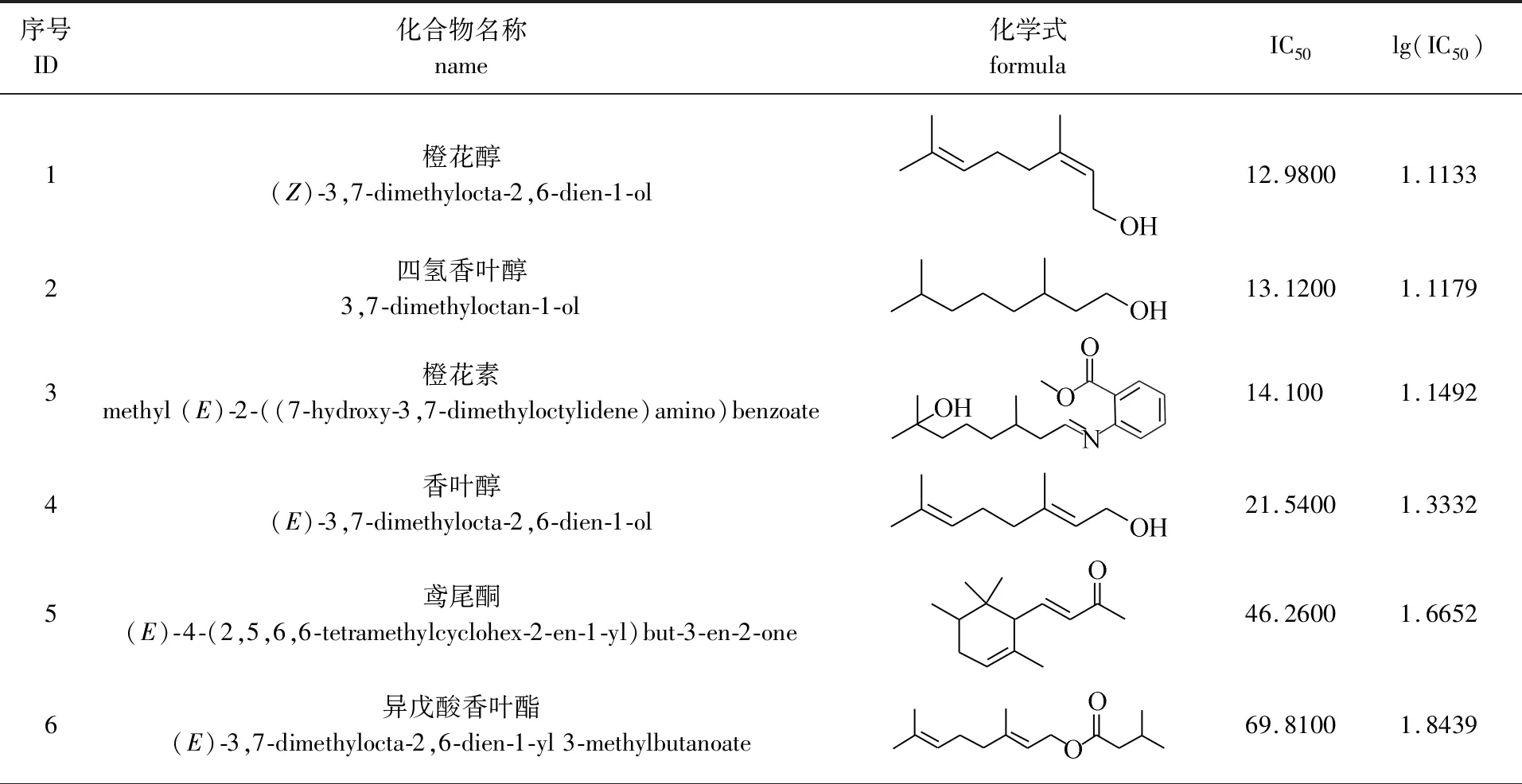
表1 化合物的信息[19-20]Table 1 Information of the compounds[19-20]

续表1
1.2 柠檬醛基衍生物的结构构建、优化及参数计算
在Gauss View 05软件中构建柠檬醛基衍生物的立体构象,利用Gaussian 09和Ampac软件完成结构优化和参数计算。结构优化使用密度泛函理论(DFT)的B3LYP方法,基组为6-31G*,获得衍生物分子的最低能量构型。
1.3 描述符的生成与筛选
将Ampac软件处理后的三维分子结构导入Codessa软件中,通过结构参数化过程,将每个柠檬醛衍生物的分子结构转变成一系列具有具体数值的结构描述符。每个化合物至少含有400个描述符,具体的描述符类型包括6类:结构组成描述符、拓扑描述符、几何描述符、静电描述符、量子化学描述符和热力学描述符。获得的描述符通过启发式回归方法,剔除与活性不相关的描述符,筛选出来的描述符将用于下一步QSAR模型的构建。
1.4 QSAR模型的构建
利用启发式回归方法,在筛选出来的描述符中选取与活性显著相关的描述符构建一系列含有不同描述符个数的QSAR模型。最优模型描述符个数的确定遵循以下规则:n≥3(k+1)(其中,n为衍生物个数,k为最终模型中的描述符个数);当相关系数随参数个数的增加并无显著增大时(0.02<△R2<0.04),回归终止,此时获得的模型为最优模型。
1.5 QSAR模型的检验
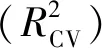
2 结果与讨论
2.1 模型的构建
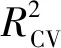
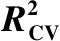
表2 不同描述符个数对应的R2和Table 2 R2 and values of the models with different number of descriptors
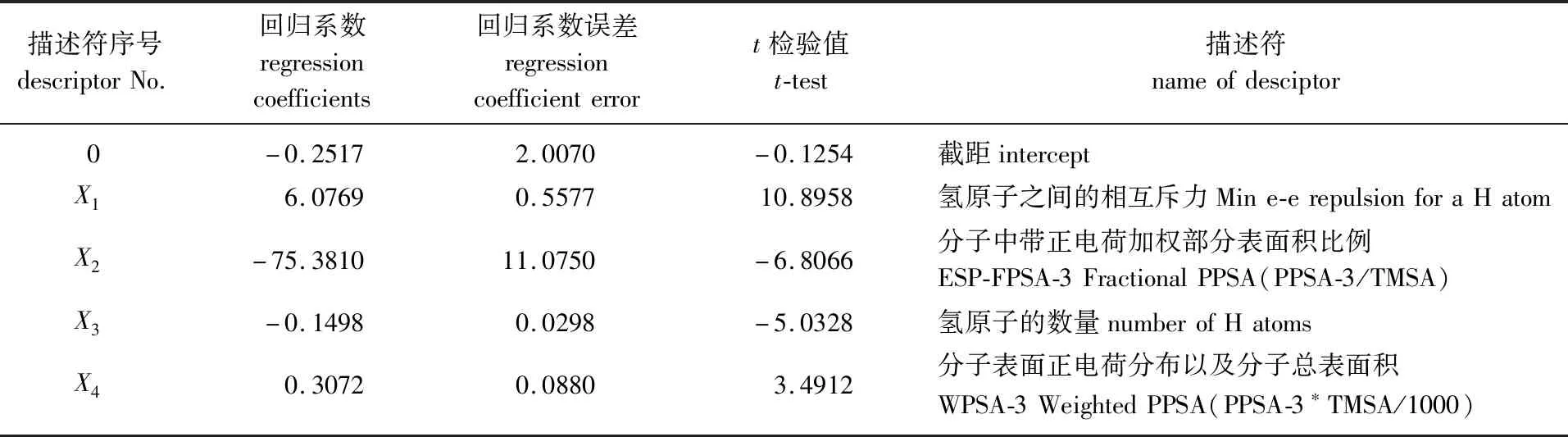
表3 含4个描述符的QSAR模型Table 3 QSAR model with four-descriptor
2.2 模型的检验
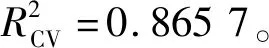
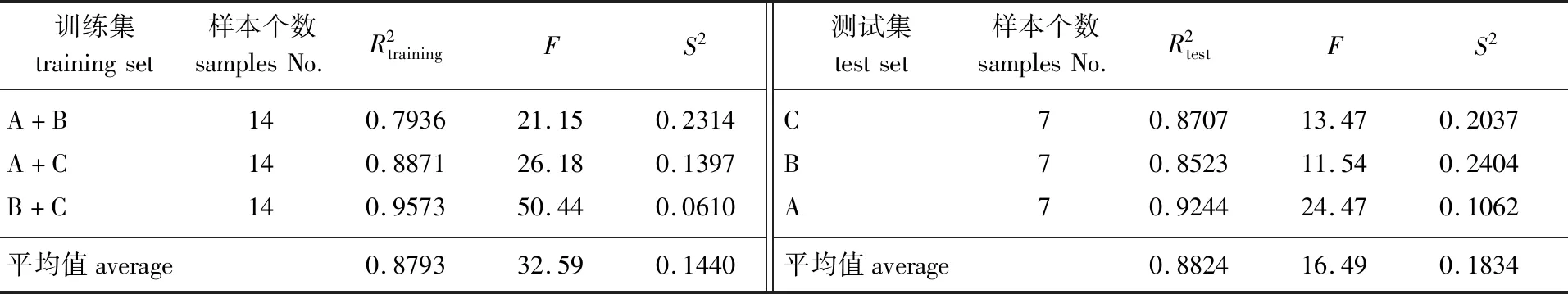
表4 最佳模型内部检验Table 4 Validation of the best model
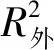

表5 外部检验的化合物lg(IC50)值的实验值与预测值Table 5 Experimental and predicted values of lg(IC50) values for externally tested compounds
用最佳QSAR模型对21个化合物对进行活性预测可以获得21个化合物lg(IC50)预测值,将其与相应的实验值进行相关性分析,可以获得构建最佳QSAR模型的21个化合物lg(IC50)实验值和lg(IC50)预测值的线性拟合曲线(图2)。由图2可知,21个化合物lg(IC50)实验值和lg(IC50)预测值之间相关性高,R2达0.926 5,数据分布合理。
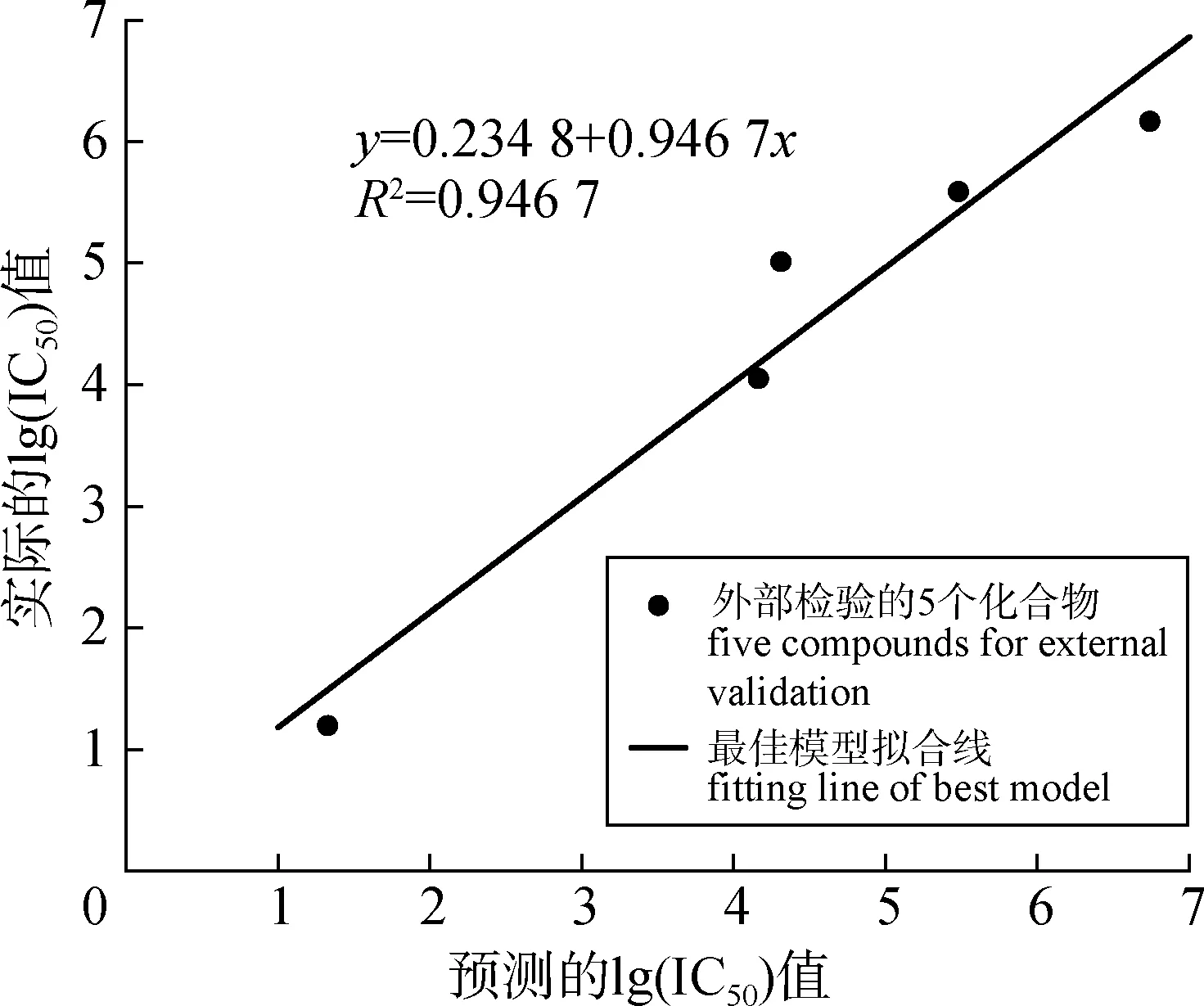
图1 外部检验集化合物lg(IC50)值的实验值和预测值的线性回归关系Fig.1 The linear regression relationship between the experimental lg (IC50) value and the predicted lg (IC50) value of the compounds from external validation set
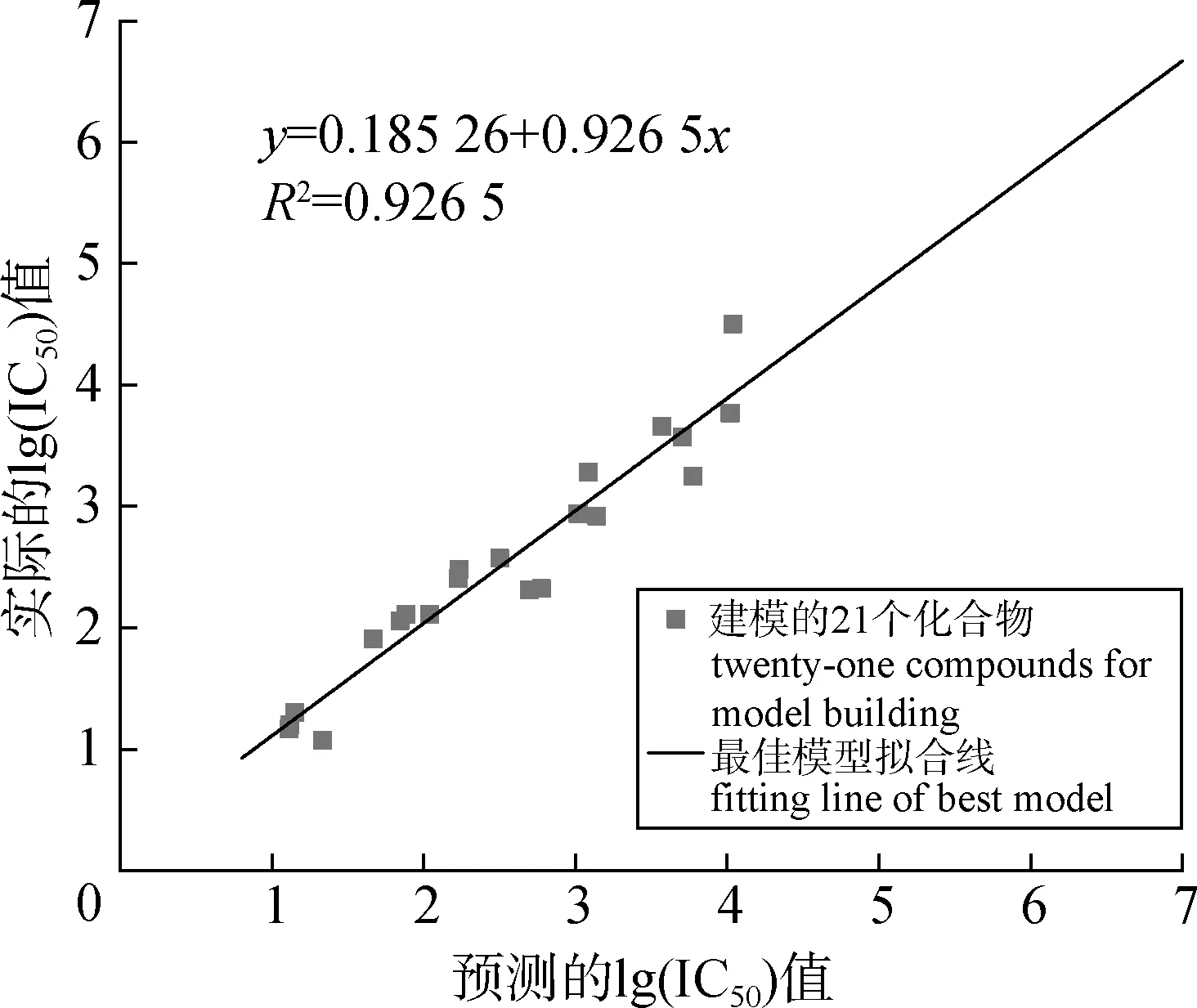
图2 最佳QSAR模型的21个化合lg(IC50)实验值和lg(IC50)预测值的线性拟合曲线Fig.2 Linear fitting curve of the experimental lg(IC50) values and predicted lg(IC50) values of twenty-one compoundsfrom the best QSAR model
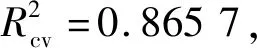
2.3 影响抗菌活性的描述符分析
根据Codessa的参考手册[21]和相关文献[22],对最佳QSAR模型的4个描述符进行解析,结果如下:
第二个描述符是分子中带正电荷加权部分表面积比例,其计算公式为FPSA3=PPSA3/TMSA,其中,PPSA3为原子正电荷加权部分表面积;TMSA为分子总表面积。由以上公式可说明抗菌活性跟分子表面正电荷的分布有关。
第三个描述符是氢原子的数量。第四个描述符是分子表面正电荷分布以及分子总表面积,该描述符与第二个描述符含义类似,同样是提示衍生物抗菌活性与分子表面正电荷分布以及分子总表面积有关。
结合2.1节最优模型式子分析可知,随着氢原子之间相互斥力的增加,以及化合物分子表面正电荷分布、分子总面积的增加,化合物对油茶炭疽病菌的IC50值变大,从而降低化合物对油茶炭疽病菌的抗菌活性;随着化合物分子中带正电荷加权部分表面积比例的增加,以及化合物中氢原子个数的增加,化合物对油茶炭疽病菌的IC50值变小,从而增强化合物对油茶炭疽病菌的抗菌活性。
由抗菌化合物相关的作用机理可知,一些有机小分子类抗菌化合物发挥抗菌作用时,通常会与靶标蛋白进行结合,抗菌化合物与靶标蛋白内的特定氨基酸通过氢键相互作用、疏水作用和π-π堆积作用等方式相互作用[23-25],其中氢键作用是最主要的结合方式。在形成稳定的结合体后,可以使靶标蛋白失去功能,菌体生长停滞或者死亡,从而达到抗菌效果。氢原子个数、分布和比例可以影响衍生物与靶标蛋白之间的与氢键相互作用,衍生物分子表面电荷的分布情况可以影响氢键作用位点和强度。
综上,柠檬醛基衍生物分子结构中与氢键供体相关的描述符,包括:氢原子之间的相互斥力、分子中带正电荷加权部分表面积比例、氢原子的数量、分子表面正电荷分布以及分子总表面积,对抗菌活性具有显著影响。
3 结 论
本研究开展了柠檬醛基抗油茶炭疽病菌衍生物的定量构效关系分析。构建了1个含有4个描述符的QSAR模型,相关系数R2为0.926 5,具有良好稳定性和预测能力。分析该模型可知,柠檬醛基衍生物分子结构中与氢键供体相关的描述符,均对抗菌活性具有显著影响。未来在设计新型柠檬醛基抗油茶炭疽病菌衍生物时,可在其分子骨架上适当增加氢原子,同时通过引入取代基增加衍生物分子表面的正电荷比例,以影响衍生物与靶标蛋白之间的相互作用,从而提高化合物的生物活性。本研究可为设计具有更好抗油茶炭疽病菌活性的柠檬醛衍生物提供理论指导,对于山苍子精油创新深加工利用以及新型抗菌剂的开发具有积极的意义。

