氯胺酮联合异丙酚麻醉对无抽搐电休克治疗难治性抑郁症的疗效及认知功能的影响
古智文,黄雄,张春平,王志杰,张敏玲
难治性抑郁症(treatment-resistant depression,TRD)是指既往采用至少2种抗抑郁剂按照标准剂量及疗程治疗后并无明显效果的疾病,患者主要临床症状为思维动作减慢、常出现躯体不适感及极度负面情绪,甚者具有明显的自杀意图,使其正常生活受到严重困扰,危及生命[1]。因此,如何治疗TRD以减轻患者临床症状是近年来临床研究的重点课题之一。目前,临床常采用无抽搐电休克(MECT)治疗TRD,其有效率约60%,但大部分患者MECT治疗后存在暂时性意识模糊和顺行性遗忘,其中少部分患者的逆行性遗忘可持续6个月以上,这种对于认知功能损害的担忧阻碍了MECT在临床的更广泛应用。故临床急需采取一种有效的治疗措施,在提高该类患者治疗效果的同时减少认知不良反应,对MECT的治疗有着重要的临床意义。
现临床常采用的MECT麻醉剂有依托咪酯、美索比妥钠、丙泊酚及硫喷妥钠等,上述药物对电流诱发的癫痫可产生不同程度的拮抗,对MECT疗效造成影响[2]。近年来,氯胺酮(ketamine)的快速抗抑郁效果得到该领域的高度重视,已有国外学者证实,采用氯胺酮作为MECT的麻醉剂治疗TRD,可有效提高治疗效果。异丙酚(propofol)是临床常用的一种全身麻醉剂,在临床应用广泛。ketamine与propofol混合剂被简称为ketafol麻醉[3]。但临床关于氯胺酮如何在MECT治疗中发挥抗抑郁机制的报道甚少。基于此,现探讨ketafol麻醉提高MECT治疗难治性抑郁症的疗效同时减少认知功能损害的机制,以期为临床提供借鉴,报道如下。
1 资料与方法
1.1 临床资料 选取2012年2月—2018年2月广州医科大学附属脑科医院收治难治性抑郁症患者120例作为研究对象,按随机数字表法分为异丙酚MECT组、氯胺酮MECT组、 联合MECT组,每组40例。异丙酚MECT组男21例,女19例,年龄21~44(30.83±3.21)岁;病程1.8~13.9(7.8±1.2)年;莫兹利分级(MSM):中度29例,重度11例;诱因:身体疾病17例,社会心理因素14例,无诱因9例;临床表现:睡眠障碍17例,食欲下降31例,躯体不适36例,头痛32例,头晕21例;并发症:神经衰弱38例,失眠17例,高血压7例,低血压6例;既往治疗史:6个月前曾治疗过1次,家族遗传史7例。氯胺酮MECT组男22例,女18例,年龄22~45(30.91±3.52)岁;病程1.9~14.0(7.9±1.3)年;MSM分级:中度30例,重度10例;诱因:身体疾病16例,社会心理因素16例,无诱因8例;临床表现:睡眠障碍16例,食欲下降30例,躯体不适37例,头痛33例,头晕22例;并发症:神经衰弱37例,失眠16例,高血压6例,低血压7例;既往治疗史:8个月前曾治疗过1次,家族遗传史7例。联合MECT组男20例,女20例,年龄21~45(30.93±3.31)岁;病程1.8~13.92(7.9±1.3)年;MSM分级:中度31例,重度9例;诱因:身体疾病18例,社会心理因素15例,无诱因7例;临床表现:睡眠障碍17例,食欲下降32例,躯体不适35例,头痛33例,头晕22例;并发症:神经衰弱36例,失眠17例,高血压5例,低血压8例;既往治疗史7个月前曾治疗过1次,家族遗传史6例。3组患者一般资料比较差异无统计学意义(P>0.05),具有可比性。本研究方案的制定符合《世界医学协会赫尔辛基宣言》的相关要求,经医院伦理委员会审核批准,患者及家属知情同意并签署知情同意书。
1.2 病例选择标准 (1)纳入标准:①年龄18~45岁;②符合《中国精神障碍分类与诊断标准》第3版CCMD-3中关于抑郁症的诊断标准;③采用≥2种抗抑郁药物按规范化治疗后无效;④汉密尔顿抑郁量表(HAMD-17项)评分≥20分。(2)排除标准:①不适合进行MECT治疗者;②同时合并其他精神障碍,如痴呆、精神分裂症;③高血压、青光眼、动脉瘤,或脑血管畸形;④既往麻醉剂过敏史;⑤存在对酒精滥用等依赖病史;⑥体内存在起搏器或脑内电极等金属异物。
1.3 治疗方法 治疗前患者均禁食8 h,麻醉过程:患者均给予阿托品1 mg, 异丙酚MECT组给予异丙酚1.0 mg/kg,氯胺酮MECT组给予氯胺酮1.0 mg/kg,联合MECT组给予氯胺酮0.5 mg/kg、异丙酚1.0 mg/kg;麻醉后面罩给氧手控呼吸。待患者腱反射消失且全身肌肉松弛后,将患者贴电极处的皮肤进行清洁,测电阻(正常电流量>500 Ω,<2 500 Ω),等待醒脉通电抽搐治疗仪(美国)显示准备状态,将电极片放置于患者颞部两侧,若患者年龄<20岁,电阻则选择年龄值的50%;若患者年龄20~25岁,电阻则选择年龄值的60%;若患者年龄>25岁~<45岁,电阻则选择年龄值的70%~80%;若患者年龄45~50岁,电阻则选择年龄值的100%或120%。选择DGX模式3 min,2XDOS模式4 min,治疗结束后待患者恢复自主呼吸后安全离开治疗室。每周治疗3次,每次间隔1~2 d,总疗程为8次, 在3周内完成。治疗过程均由同一组治疗医师及麻醉医师共同完成。为确保患者的治疗安全性,进行MECT时必须监护呼吸、血氧饱和度、脑电图(EEG)、促性腺激素(ECG)及排空大小便,且在治疗过程中禁用其他抗癫痫药、抗焦虑药及精神病药。
1.4 临床疗效评价 治疗8次后采用汉密尔顿抑郁量表(HAMD)[4],蒙哥马利抑郁量表(MARDS)[5],临床总体印象量表(CGI)[6],简明精神病量表(BPRS)[7]对患者进行评价。其中HAMD包括精神和躯体2个维度,共14个项目,评分采用5级评分法,0分为无症状,4分为极重,得分越高表示患者症状越严重。MARDS包括内心紧张、睡眠减少等共10个条目,评分0~6分,0分为无症状,6分为极度严重,得分越高表示患者症状越明显。CGI可分为病情严重程度、疗效总评及疗效指数3个维度,评分为0~7分,0分为无病,7为极重,得分越高表示患者症状越明显。BPRS共18个项目,评分为1~7分,1分为无病,7分为极度严重,得分越高表示患者症状越明显。痊愈:各项总评分减分率≥75%;显效:各项总评分减分率50%~74%;好转:各项总评分减分率30%~49%;无效:各项总评分减分率<30%。总有效率=(痊愈+显效+好转)/总例数×100%。
1.5 观察指标与方法
1.5.1 认知功能评估: 在治疗前和末次治疗结束1周时,采用神经认知功能测验(MCCB)量表[8]评估认知功能,该量表包括7个心理维度和10项分测验,总分越高表示患者恢复越好。
1.5.2 血清脑源性神经营养因子(BDNF)及BDNF/BDNF前体(pro-BDNF)比值: 观察治疗前和末次治疗结束1周后翌日清晨抽取空腹肘静脉血3~5 ml,离心取上清保存于-80℃ 冰箱待测。采用双抗体夹心ELISA法检测血清BDNF水平,并计算血清BDNF/pro-BDNF比值,其比值越高表示抗抑郁效果越好,反之则效果差。
1.5.3 脑电慢波发生率检测:患者脑电图慢波特征均采用美国Cadwell公司生产的Easy Ambulatory 脑电图仪及上海诺诚电气有限公司生产的NATION7128W视频脑电图仪进行观察,统计屏幕上出现脑电慢波的例数,基线脑电慢波水平可预测患者对氯胺酮治疗的疗效。脑电慢波发生率=出现脑电慢波的例数÷总例数×100%。
1.5.4 不良反应(TESS)评定[9]:根据患者出现行为毒性可分为中毒性意识模糊、兴奋或激越、情感忧郁及活动增加,根据严重程度评分:无为0分,较轻为1分,轻度为2分,中度为3分,重度为4分。
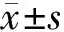
2 结 果
2.1 3组治疗效果比较 治疗后,联合MECT组总有效率(95.0%)优于异丙酚MECT组(50.0%)(χ2=62.297,P<0.001),而与氯胺酮MECT组(92.5%)比较,差异无统计学意义(χ2=0.213,P=0.644),见表1。
2.2 3组治疗前后MCCB总分比较 治疗前,3组MCCB总分比较,差异无统计学意义(P>0.05);治疗后,3组MCCB总分均提高,且联合MECT组>氯胺酮MECT组>异丙酚MECT组(P均<0.01),见表2。
2.3 3组治疗前后血清BDNF及BDNF/pro-BDNF比值比较 治疗前,3组患者血清BDNF水平及血清BDNF/pro-BDNF比值比较,差异无统计学意义(P>0.05);与治疗前比较,治疗后异丙酚MECT组上述指标变化不明显(P>0.05),而氯胺酮MECT组及联合MECT组均增高,且联合MECT组高于氯胺酮MECT组(P均<0.01),见表3。
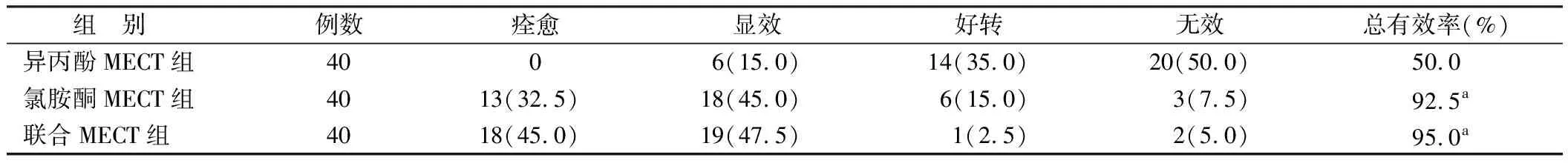
表1 3组患者治疗8次后效果比较 [例(%)]
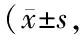
表2 3组患者治疗前后MCCB总分比较分)

表3 3组患者治疗前后血清BDNF及BDNF/pro-BDNF比较
2.4 3组脑电慢波发生率比较 治疗后,联合MECT组脑电慢波的发生率5.0%(2例)低于氯胺酮MECT组25.0%(10例)低于异丙酚MECT组72.5%(29例)(χ2=38.393,P<0.01)。
2.5 3组不良反应评分比较 治疗后,不良反应评分异丙酚MECT组为(9.67±2.38)分,氯胺酮MECT组为(9.92±3.01)分,联合MECT组为(9.41±2.17)分,3组比较,差异均无统计学意义(F=0.402,P=0.670)。
3 讨 论
抑郁症是全球重大的慢性、致残性精神疾病之一,预计到2030年抑郁症的发病率将位居所有疾病负担的首位[10]。该病的主要特点为高患病率、高致残率、高自杀率及高复发率,其中最为严重的后果为自杀死亡。相关研究提示[11],近50%的抑郁症患者采用一线抗抑郁药物治疗无效,近33%的抑郁症患者对2种或2种以上的药物及心理干预并无效果,该类抑郁症被称为TRD。目前公认TRD最为有效的治疗方法为MECT,其缓解率为50%~70%。大部分TRD患者经MECT治疗后,会伴随不同程度的认知功能损害,影响MECT在临床的推广。故如何提高MECT治疗TRD的临床疗效,同时减少认知不良反应具有重要临床意义。
氯胺酮是苯环己哌啶的衍生物,是一种麻醉剂,该药具有潜在的快速抗抑郁效果,已成为精神医学领域研究的重点及热点[12]。有临床研究提示[13],采用氯胺酮治疗单相和双相抑郁,能迅速缓解患者的自杀观念。故相关研究推测,氯胺酮可作为MECT麻醉剂以提高其治疗效果。异丙酚又称丙泊酚,是临床常用的一种快速强效的全身麻醉剂,具有起效快、持续时间短、苏醒快而平稳,且安全性高,该药已在临床广泛应用。MECT是将处于麻醉状态的TRD患者通过短暂、适量的电流对大脑造成刺激,在其脑内诱发一次癫痫发作,从而达到控制精神症状的一种物理疗法。已有相关小样本研究对不同麻醉剂在治疗MECT时的疗效进行对比,如Wang等[14]通过研究发现,治疗后,混合组(氯胺酮合并异丙酚)与氯胺酮组的临床疗效明显优于异丙酚组,且混合组不良反应明显低于氯胺酮组与异丙酚组,由此可推断将ketafol麻醉作为首选的MECT麻醉剂。Amini等[15]研究提示,氯胺酮是一种安全有效的麻醉药物,且起效快。本研究结果与以往研究相似,提示ketafol麻醉MECT治疗TRD起效更快,HAMD、MARDS、CGI、BPRS量表评分均明显改善。
研究提示[16],MECT会对患者的记忆及认知功能造成不同程度的影响,特别是对近记忆的影响更为明显,损伤程度有限且具有可逆性,停止用药后过段时间可恢复正常。Chen等[17]将氯胺酮作为麻醉剂,结果显示,氯胺酮对患者的认知功能损伤更少。本研究结果与之相似,联合MECT组MCCB总分增加,提示ketafol麻醉MECT可减少对TRD患者认知功能的损害,使TRD患者定向力恢复更佳,对其短期记忆功能损害较少。
BDNF主要在中枢神经系统内表达,集中分布在皮质、杏仁核及海马,其主要作用为刺激和促进神经细胞生长分化、对神经细胞存活和正常功能起到维持作用,可调控活性依赖的突触修饰、效能和联系。已有相关研究证实[18],BDNF可参与神经元的生存,是神经可塑性的分子标志物,参与中枢神经系统中5-HT神经元的可塑性,对神经系统的发育和成熟具有重要作用,参与抑郁障碍的生理病理过程。大脑和外周中存在丰富的BDNF,且在人类血浆及血清中均存在,血清BDNF水平明显高于血浆100倍,上述差异主要是由于凝血过程中血小板脱落颗粒造成的。故血浆BDNF水平可充分反映循环血液的水平,且BDNF可透过血脑屏障循环,从而可能促进产生大脑神经元和基底节细胞,因此,可通过测量人体血浆BDNF水平反映大脑BDNF水平。诸多研究证实[19],BDNF表达参与了抑郁症的病理过程。抑郁症与BDNF水平下降有关,抑郁症患者大脑BDNF水平降低会影响血循环BDNF水平。文献研究提示,抑郁症的发病与大脑神经网络可塑性受损呈正相关,BDNF水平降低反映了神经网络和可塑性受损,且BDNF水平降低会造成边缘结构的缩小,引发情绪障碍[20]。相关研究提示,TRD患者血清BDNF水平降低,经有效治疗后BDNF水平上升,提示BDNF水平为反映抗抑郁疗效的生物学指标,且BDNF在抑郁症的病理生理机制和恢复过程中起到重要的作用[21]。Vasic等[22]研究提示,抑郁症患者的脑组织形态学改变为海马状突起明显较正常人的脑组织小,其细胞数目减少或神经胶质细胞及神经元缩小,给予有效治疗后可逆转或阻止神经元缩小及神经细胞数目减少,提示抑郁症发病与脑损伤相关。Su等[23]研究提示,抑郁症患者BDNF水平降低可能与萎缩的海马体积、神经细胞凋亡及某些神经元摄取神经营养因子能力降低相关。最新研究提示[24],MECT治疗和亚麻醉剂量的氯胺酮治疗TRD有可能促使血清BDNF水平升高。最新报道指出[25],pro-BDNF是BDNF释放进入循环系统的初始形式,pro-BDNF与胰岛素类似,在机体内循环系统经酶切后转化为活性更高的BDNF,由此可推断反映抗抑郁疗效的有效指标可能是BDNF/pro-BDNF的比值。乔卉等[26]研究证实,BDNF及pro-BDNF均参与了应激性抑郁的发生,其在神经元可塑性变化中发挥了重要作用。 陈英等[27]研究提示,将氯胺酮作为麻醉剂可有效提高TRD患者血清BDNF浓度水平;黄雄等[28]研究也证实,以氯胺酮作为麻醉剂可有效提高MECT治疗难治性抑郁症患者BDNF浓度水平。本研究结果与上述研究相符,这与ketafol麻醉MECT治疗可刺激TRD患者血清BDNF水平、BDNF/pro-BDNF比值有关,可减少神经细胞凋亡、预防海马体积缩小及发挥维护神经元正常状态的作用,确保神经突触的可塑性,从而作用于丘脑与垂体释放促肾上腺皮质激素,改善脑损伤。
在抑郁症患者中慢波睡眠明显降低,特别是睡眠早期阶段。有效地抗抑郁治疗可增加慢波睡眠比例。反映大脑皮质神经元突触可塑性的有效指标是睡眠脑电图活动。且已有相关研究提示,对抑郁症患者采用亚麻醉剂量的氯胺酮注射治疗后,可明显增加抑郁症患者睡眠早期阶段的睡眠脑电图慢波活动,而基线睡眠脑电图慢波水平可预测抑郁症患者对氯胺酮治疗的疗效。且MECT治疗的主要作用机制是诱导大脑皮质增加睡眠脑电图慢波水平。氯胺酮是一种精神活性物质,若剂量过高会诱发精神病性症状,且其可兴奋交感神经;另外可大量激活儿茶酚胺,故氯胺酮在MECT治疗时是否会诱发清醒恢复期的兴奋激越行为,是否会成瘾,是否会导致患者血压升高而引发意外需进一步研究。本研究结果显示,ketafol麻醉MECT并不会对脑电慢波的发生率造成不良影响,且不会增加不良反应,其原因如下:(1)氯胺酮具有抗抑郁作用,主要表现为通过升高BDNF水平和增加脑电慢波,从而改变中枢神经系统的突触可塑性,而诱导大脑皮质增加脑电慢波水平一直被认为是MECT治疗的作用机制之一。(2)由于ketafol麻醉MECT需要的电流量较小,且具有较高的抽搐指数及长时间抽搐,与治疗的最终疗效和认知不良反应程度密切相关。由此可推断,ketafol麻醉MECT能够提高TRD患者的疗效,同时减少认知不良反应,中枢突触可塑性的改变是重要的作用机制。但由于本研究所纳入样本量较少,且未对BDNF基因Val66Met位点基因分型进行分析,尚需扩大样本量进行更深一步研究,应同时对TRD患者的BDNF基因Val66Met位点基因分型展开分析。
总之,在TRD患者中采用ketafol麻醉MECT治疗,效果明显优于氯胺酮MECT和异丙酚MECT,且可减少对TRD患者认知功能的损伤,提高血清BDNF水平及血清BDNF/pro-BDNF比值,减少脑电慢波的发生率,且安全性较高。ketafol麻醉MECT治疗TRD患者的主要机制为其可减少认知不良反应,改变中枢突触的可塑性。
利益冲突:所有作者声明无利益冲突
作者贡献声明
古智文、黄雄:提出研究方向、思路、选题,制定方案、流程,撰写论文;张春平:进行文献整理;王志杰、张敏玲:实施研究过程,数据收集,分析整理

