水合物法天然气脱碳技术模拟研究
范明龙,陈 杰,花亦怀,苏清博
(中海石油气电集团技术研发中心,北京 100028)
天然气中CO2的存在会降低气源热值, 腐蚀和堵塞输气管路,有必要将其分离出来。 常用的天然气中CO2脱除方法包括:醇胺吸收法、膜分离法和低温分离法。 其中,醇胺吸收法是利用强碱性胺与CO2的反应,将CO2从混合气体中分离出来,该工艺流程成熟、净化程度高,但再生能耗较高、强碱性溶剂腐蚀性强, 容易与酸气结合生成难分解的副产物,导致溶剂性能失效较快[1];膜分离法是利用中空纤维分离膜对CH4与CO2气体分子的选择性差异,在压力的推动下,各气体分子渗透的速率不同从而达到分离目的,工艺流程简单、分离速度快,但脱碳效率低、CH4损失率高[2];低温分离法是在CH4-CO2体系三相点以下的温度区间内, 通过降低温度实现CH4和CO2凝华后的气固分离,即可控制的CO2冻结区域法(Controlled Freeze Zone,CFZ法),降低了预处理CO2的设备投资,但冷能耗需求较大[3,4]。
根据相关报道,水合物分离法在天然气脱碳中具有应用潜力。 水合物分离法利用不同气体组分的水合物生成条件不同,使混合气体中某一组分形成水合物,另一组分仍以气态形式存在,从而实现混合气体分离[5-8]。 相较于低温分离法,本方法的操作温度可提高到0 ℃以上,降低了冷能的需求。文献[9,10]首先测量了CO2-N2以及CO2-CH4混合物在不同温度、压力下的三相平衡条件,结果发现随着CO2浓度的增大,水合物形成压力逐渐降低; 并采用带有二阶修正MHV2混合规则的SRK状态方程来处理气液相,van der Waals-Platteeuw模型处理水合物相来预测三相平衡,计算结果和实验数据基本吻合,为水合物法分离提供了基本理论依据。 Linga等[11]通过建立水合物分离与膜分离耦合工艺, 实现17% CO2+83% N2(物质的量分数)混合气体的分离,经过三级水合分离后得到98%~99%的CO2气体。 Klara等[12]基于水合物的新型CO2捕集技术, 从煤气发电厂获得的合成气(40%CO+60%H2)中实现了CO2的脱除。 Chen等[13]以四丁基溴化铵(TBAB)作为水合物形成促进剂,进行了水合物法同时捕获烟气中CO2和SO2的实验研究,结果表明烟气中95%的SO2可以通过水合物法脱除,并且CO2的浓度可以降低到8%左右。
虽然水合物分离技术在烟道气分离中得到了一定的研究,但该技术在天然气脱碳中的研究还较少。 本文借助Aspen HYSYS模拟软件搭建了水合物脱碳的工艺流程,进行了压力、温度和H2O流量的优化分析;并且基于动态控制结构,通过改变原料气流量与组分比例,考察了流程响应特性。
1 水合物法天然气脱碳模拟
1.1 水合物法分离原理
水合物法分离是利用不同气体生成水合物相平衡条件差异 (压力差),CH4与CO2的T-P水合物生成曲线如图1所示。由图1可知,当温度低于10 ℃时,相同温度下,CO2生成水合物的相平衡压力比CH4低,所以CO2水合物的稳定性高于CH4水合物。 当温度高于10 ℃时,相同温度下,CO2生成水合物的相平衡压力比CH4高, 所以CH4水合物的稳定性高于CO2水合物。 在图1中,CH4中混合CO2可以降低水合物的生成压力,当温度低于10 ℃时,混合气体与水在反应器中首先形成CO2水合物, 利用该规律, 可实现CH4和CO2的水合分离。
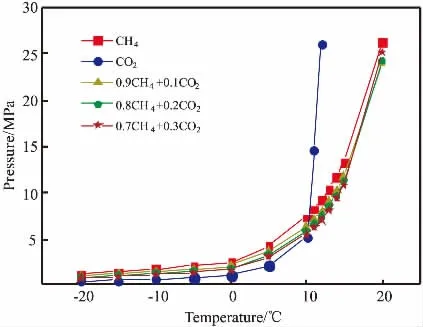
图1 CH4与CO2的T-P水合物生成曲线Fig. 1 T-P hydrate formation curve of CH4 and CO2
1.2 分离工艺流程模拟
采用Aspen HYSYS 8.6中的Peng-Robinson物性包进行水合物生成曲线的预测和水合物法脱碳的流程模拟。 图2为水合物法分离CO2工艺流程图。 在一定的温度(5 ℃)和压力(3.15 MPa)条件下,采用70%CH4和30%CO2(物质的量分数)的混合气体为原料气,与H2O通过混合器(MIX-100)后一起汇入分离器(V-100)中,模拟水合反应器中CO2水合物的形成。 V-100塔顶获得CH4含量95%以上的产品,塔底流出的CO2水合物进入再沸塔(T-100),模拟水合分解器中CO2的脱除以及H2O的回收, 即可实现CO2的水合分离。
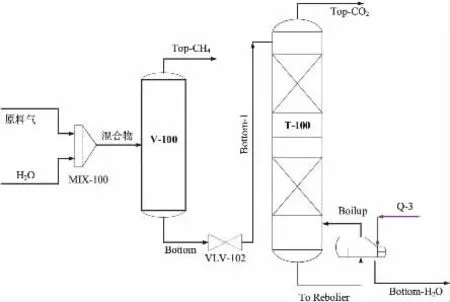
图2 水合物法分离CO2工艺流程Fig. 2 Process of CO2 separation by hydrate method
1.3 压力对分离效果的影响
设定混合物的温度为5 ℃、H2O流量为180.0 kmol/h,借助Aspen HYSYS Case Study工具, 考察了水合分离效果对混合物压力变化的敏感度,如图3所示。

图3 压力与分离器塔顶产品组分关系Fig. 3 Relationship between pressure and product compositions at the top of separator tower
由图3可知, 随着混合物压力的升高, 分离器(V-100) 塔顶产品的CH4含量逐渐升高,CO2含量逐渐下降,并趋于平缓。 由水合物生成条件可知,提高体系压力可以提高水合物的生成速率,且生成的水合物不易分解。 因此,适当提高体系的压力可以促进CO2水合物的生成, 进而获得较高纯度的CH4产品。
1.4 温度对分离效果的影响
设定混合物的压力为3.15 MPa、H2O 流量为180.0 kmol/h, 借助Aspen HYSYS Case Study工具,考察了水合分离效果对混合物温度变化的敏感度,如图4所示。 由图4可知,随着混合物温度的升高,分离器(V-100)塔顶产品的CH4含量下降,CO2含量升高。 因为温度较高时,CO2水合物相和气相间的逸度差较大,而逸度差是气体分子扩散(渗透)的主要驱动力。 逸度差越大,CO2分子运动越剧烈,具体表现为CO2水合物的稳定性降低; 而当温度较低时,CO2分子运动受到限制, 生成的CO2水合物也能保持较好的稳定性,分离器(V-100)塔顶也可以获得较高纯度的CH4产品。 因此,需要适当降低体系的水合分离温度。
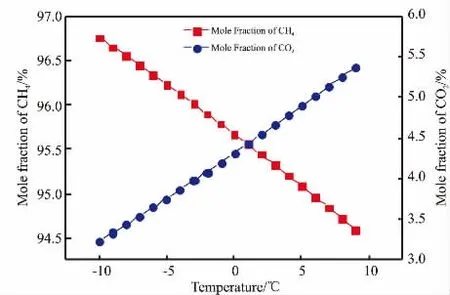
图4 温度与分离器塔顶产品组分关系Fig. 4 Relationship between mixture temperature and product compositions at the top of separator tower
1.5 H2O流量对分离效果的影响
设定混合物的压力为3.15 MPa、温度为5 ℃,借助Aspen HYSYS Case Study工具, 考察了水合分离效果对用H2O流量变化的敏感度,如图5所示。由图5可知,随着H2O流量的增加,分离器(V-100)塔顶产品的CH4含量逐渐升高,CO2含量逐渐降低。 由水合物生成条件可知, 水合物是天然气中的CO2分子与H2O分子以配位键结合形成的,因此液态H2O的存在是生成水合物的必要条件。H2O流量的增大,可以提高H2O分子和CO2分子的接触面积,CH4因缺少竞争力而较少地进入水合物相,更多的CO2溶解于液相,并生成水合物。 因此,适当增加H2O流量是生成CO2水合物的强化措施。
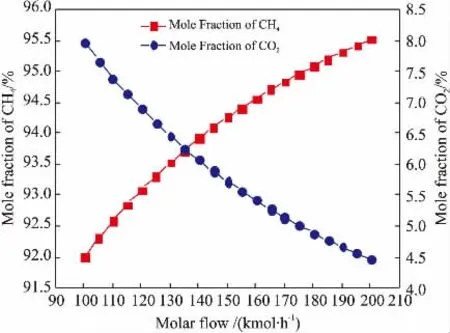
图5 H2O流量与分离器塔顶产品组分关系Fig. 5 Relationship between water molar flow rate and product compositions at the top of separator tower
2 流程动态控制与动态响应
2.1 搭建流程动态控制
稳态模拟是以所有工艺参数不随时间变化为前提搭建的,但是由于干扰的存在,实际装置的工艺参数在运行中是不断变化的,为了找出装置的最佳操作条件,搭建了水合物法分离流程的动态控制结构(如图6所示)。

图6 水合物法分离CO2流程动态控制Fig. 6 Dynamic control of CO2 separation process by hydrate method
在水合物分离流程中, 主要需要控制分离器(V-100)和再沸塔(T-100)的操作参数,使流出分离器塔顶产品的CH4含量高于95%, 并保证装置的能耗在较低水平。
原料气流量控制器(FIC-100)和H2O流量控制器(FIC-101)执行负反馈命令;分离器塔顶压力控制器(PIC-100)和再沸塔塔顶压力控制器(PIC-101)执行正反馈命令;分离器液位控制器(LIC-100)和再沸塔液位控制器(LIC-101)执行正反馈命令;再沸塔敏度塔板温度控制器(TIC-100)由再沸器能耗(Q-3)控制,执行负反馈命令。 其中,控制器参数为Tyrens-Luyben调优参数值[14],流量控制器参数比例增益Kc=0.1,积分时间Ti=12 s;液位控制器参数比例增益Kc=2.0,积分时间Ti=10 min;压力控制器参数比例增益Kc=2,积分时间Ti=2 min;温度控制器参数比例增益Kc=1.0,积分时间Ti=20 min。
由表1所示的水合物法分离CO2流程动态控制器参数可知,控制器参数和阀门开度维持在合理范围内,且保持稳定,表明实现了动态控制模拟。

表1 水合物法分离CO2流程动态控制器参数Table 1 Parameters of dynamic controller for CO2 separation process by hydrate method Parameters
2.2 原料气流量阶跃后的动态响应
在原料气组分固定的前提下, 通过设定Aspen HYSYS Dynamic模型中原料气流量控制器(FIC-100),使进料流量产生阶跃, 研究了系统的动态响应特性。 图7为原料气流量变化后, 分离器塔顶产品的CH4含量和流量的动态响应曲线。 由图7(a)可知,以水合物法分离稳态流程状态为初始条件,分离器塔顶CH4产品纯度为93.42%,低于95%。 通过设定流量控制器(FIC-100)降低原料气的流量,分离器塔顶产品的CH4含量随之升高,并达到新的稳定状态。 当原料气的流量下降30%时, 分离器塔顶产品达到新平衡时CH4含量为95.13%,满足产品质量要求。 同时,分离器塔顶产品的流量下降,如图7(b)所示,且随着流量的下降,流程达到新平衡所需要的时间增长。
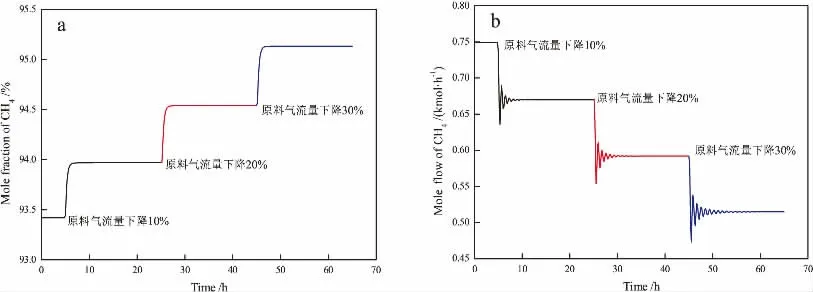
图7 原料气流量阶跃对分离器塔顶产品的CH4含量(a)和流量(b)影响Fig. 7 Effect of feed gas molar flow fluctuation on mole fraction (a) and mole flow (b) of CH4 product at the top of separator tower
2.3 原料气组分阶跃后的动态响应
在原料气流量固定的前提下,通过改变原料气组分占比,研究了系统的动态响应特性。 图8为原料气组分阶跃变化后, 分离器塔顶产品的CH4含量和流量的动态响应曲线。 由图8(a)可知,初始状态下分离器塔顶产品CH4含量为93.42%,低于95%。 为了获得满足要求的产品,可以提高原料气中CH4的含量。当原料气中CH4的含量增加10%时, 分离器塔顶产品达到新的平衡,CH4含量为95.68%,满足产品质量要求。 同时,分离器塔顶产品的流量升高,如图8(b)所示。
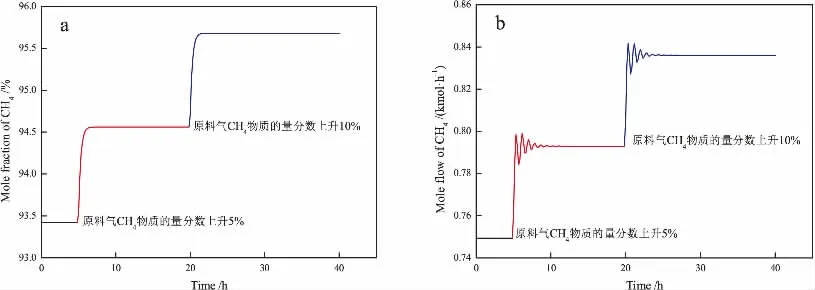
图8 原料气组分阶跃对分离器塔顶产品的CH4含量(a)和流量(b)影响Fig. 8 Effect of feed gas molar fraction fluctuation on molar fraction (a) and mole flow rate (b) of CH4 product at the top of separator tower
由图7和图8对比可知,原料气流量与分离器塔顶产品的CH4含量呈负相关, 与产品的流量呈正相关;原料气中CH4含量与分离器塔顶产品的CH4含量和流量都呈正相关。 同时可知,调整原料气中的CH4含量,更容易获得高纯度的CH4产品,说明相比于原料气流量, 模型对原料气组分变化的响应更加灵敏, 实际操作中需要注意原料气中组分含量的波动。
3 结论
根据水合物分离原理,设计模拟了水合物法天然气脱碳流程,并对其进行关键工艺参数(温度、压力、用水量)的优化分析及动态响应分析。
(1)随着混合物体系压力的升高,CO2水合物生成速率增高,且生成的水合物不易分解,产品的CH4含量升高,CO2含量下降;随着混合物体系温度的升高,CO2水合物相和气相间的逸度差较大,CO2分子运动剧烈,生成的CO2水合物稳定性低,产品的CH4含量下降,CO2含量升高; 增大H2O流量, 可以提高H2O分子和CO2分子的接触面积,CH4因缺少竞争力而较少地进入水合物相,更多的CO2溶解于液相,并生成水合物,最终得到CH4含量为95%以上的产品;
(2)由系统动态响应可知,原料气流量与分离器塔顶产品的CH4含量呈负相关, 与产品的流量呈正相关; 原料气中CH4的含量与分离器塔顶产品的CH4含量和流量都呈正相关。

