超声软指标联合母体血清甲胎蛋白和人绒毛膜促性腺激素筛查胎儿染色体异常
孔德明,韦卫中,纪伟英,饶箐箐
(华中科技大学同济医学院附属武汉儿童医院妇幼超声影像科,湖北 武汉 430030)
染色体异常又称染色体畸变、染色体发育不全,是严重先天性疾病,活产儿中发生率约0.15%,包括染色体数目异常(21-三体、18-三体、13-三体等)及结构异常(染色体异位、缺失、重复及遗传多态性等),可致胎儿先天性发育异常[1-3]。我国每年约有100万缺陷儿出生,给家庭及社会造成沉重负担[3]。尽早发现染色体结构异常、降低或防止患儿出生,是产前诊断的主要内容之一。目前临床检测染色体异常的手段包括羊膜腔穿刺染色体核型分析、产前超声及血清指标检查等[4]。根据孕中期母体血清标记物筛查染色体异常胎儿假阳性率较高[5],而针对高风险孕妇行介入性产前诊断后流产率可达1%。寻找安全、无创、准确的产前检查方法对早期筛查胎儿染色体异常十分重要 。朱继红等[6]发现产前超声软指标联合母体血清学检测有助于临床筛查胎儿染色体异常。本研究观察孕中期超声软指标联合检测母体血清甲胎蛋白(alpha-fetoprotein, AFP)和人绒毛膜促性腺激素(human chorionic gonadotropin, HCG)对于筛查染色体异常胎儿的价值。
1 资料与方法
1.1 一般资料 2017年1月—2018年12月1 625名于华中科技大学同济医学院附属武汉儿童医院接受孕中期产前筛查,年龄20~35岁,平均(25.5±4.5)岁;体质量45~75 kg,平均(53.72±6.34)kg;孕周(gestational age, GA)14~24周,平均(19.01±2.48)周。纳入标准:①初产妇;②自然受孕;③单胎妊娠;④孕妇自愿参与研究。排除标准:①胎位不正;②产道异常;③双胎或多胎妊娠;④先兆流产征兆;⑤早产或过期产;⑥伴遗传性疾病及其他疾病;⑦孕期曾服用可能影响血清标记物的药物。本研究经院伦理委员会审核通过,检查前所有孕妇均签署知情同意书。
1.2 检查方法
1.2.1 超声检查 采用GE Voluson E10彩色多普勒超声诊断仪,凸阵探头,探头频率2.5~5.0 MHz。嘱孕妇仰卧,依次扫查胎儿头颅、面部、胸、腹、脊柱、四肢及胎盘、脐带、羊水等结构;检出1项超声软指标时,再对其他部位进行扫查,确定有无其他软指标及结构异常。参照文献[7] 标准评价软指标。常用软指标包括颈项透明层(nuchal translucency, NT)增厚(厚度≥2.5 mm)、肾盂分离(前后径≥7 mm)、脉络膜囊肿(脉络膜内见圆形、椭圆形囊性结构无回声区)、侧脑室扩张(10 mm<侧脑室直径<15 mm)、鼻骨缺失或3个解剖平面均未显示鼻骨特征、肠回声增强、肠管回声增强、长骨短小(股骨或肱骨长度小于相应孕周2个标准差)和单脐动脉(脐带内及膀胱旁均仅显示1条脐动脉)等,见图1~5。将167名胎儿存在多个超声软指标(≥2个)者定义为高危孕妇,纳入高危组,将其余1 458名孕妇纳入低危组。
1.2.2 检测母体血清AFP、HCG水平 取孕妇静脉血3 ml,室温放置2 h后,常温下以1 000 r/min速度离心20 min,取上清液检测或置于-20℃冰箱中保存待检。分别采用AFP检测试剂盒、β-HCG检测试剂盒(购自武汉明德生物科技股份有限公司),严格按照说明书步骤检测血清AFP、HCG表达水平。
1.2.3 分析染色体核型及随访 对高危组于超声引导下经腹穿刺抽取约25 ml羊水,行羊水细胞G显带核型分析,观察20个中期分裂相,结合计算机分析系统进一步分析。以羊膜腔穿刺术及羊水细胞染色体核型检测结果或随访结果为金标准判断胎儿是否存在染色体异常。对低危孕妇行产后随访,并记录随访结果,与单项筛查结果进行对比。
1.3 统计学分析 采用SPSS 20.0统计分析软件。计数资料以百分率表示,组间比较采用χ2检验,以受试者工作特征(receiver operating characteristic, ROC)曲线评估母体血清AFP、HCG水平筛查胎儿染色体异常的价值,以血清AFP、HCG水平为自变量建立回归模型,计算相应概率值,通过拟合概率值绘制二者联合检测胎儿染色体异常的ROC曲线。P<0.05为差异有统计学意义。

图1 孕妇28岁,孕14周+1,超声声像图示胎儿NT稍增厚(箭) 图2 孕妇30岁,孕21周+6,超声声像图示胎儿右侧侧脑室脉络丛囊肿(箭) 图3 孕妇24岁,孕23周+4,超声显示胎儿鼻骨短(箭) 图4 孕妇35岁,孕23周+6,超声声像图示胎儿单脐动脉(箭) 图5 孕妇26岁,孕24周,超声声像图示胎儿上肢长骨短小(箭)
2 结果
2.1 胎儿染色体分析 1 561胎胎儿染色体正常(1 561/1 625,96.06%),64胎(64/1 625,3.94%)染色体异常,包括染色体数目异常胎儿35胎、结构异常胎儿29胎。
2.2 超声软指标阳性胎儿染色体分析 高危组中,经超声软指标筛查,40胎胎儿染色体异常,其中染色体数目异常23胎(21-三体11胎,18-三体8胎,13-三体4胎)、结构异常17胎(染色体异位、缺失或重复11胎,遗传多态6胎),见表1。
2.2 母体血清AFP、HCG指标筛查 孕妇血清AFP水平中位值为50.25(31.65,64.38)ng/ml,以之筛查胎儿染色体异常的敏感度为64.60%,特异度为66.00%,曲线下面积(area under the curve, AUC)为0.701(95%CI:0.638,0.762),截断值为56.24 ng/ml。HCG水平中位值为16.64(11.38,22.64)ng/ml,筛查胎儿染色体异常的敏感度为98.50%,特异度为14.40%,AUC为0.788(95%CI:0.751,0.826),截断值为19.36 ng/ml。血清AFP联合HCG筛查胎儿染色体异常的敏感度为71.88%,特异度为93.66%,AUC为0.796(95%CI:0.751,0.841)。见图6。
2.4 超声软指标、血清AFP、HCG及联合检测胎儿染色体异常 超声软指标、血清AFP及HCG联合检测诊断胎儿染色体异常的敏感度均高于单项指标检测(P均<0.05),见表2。
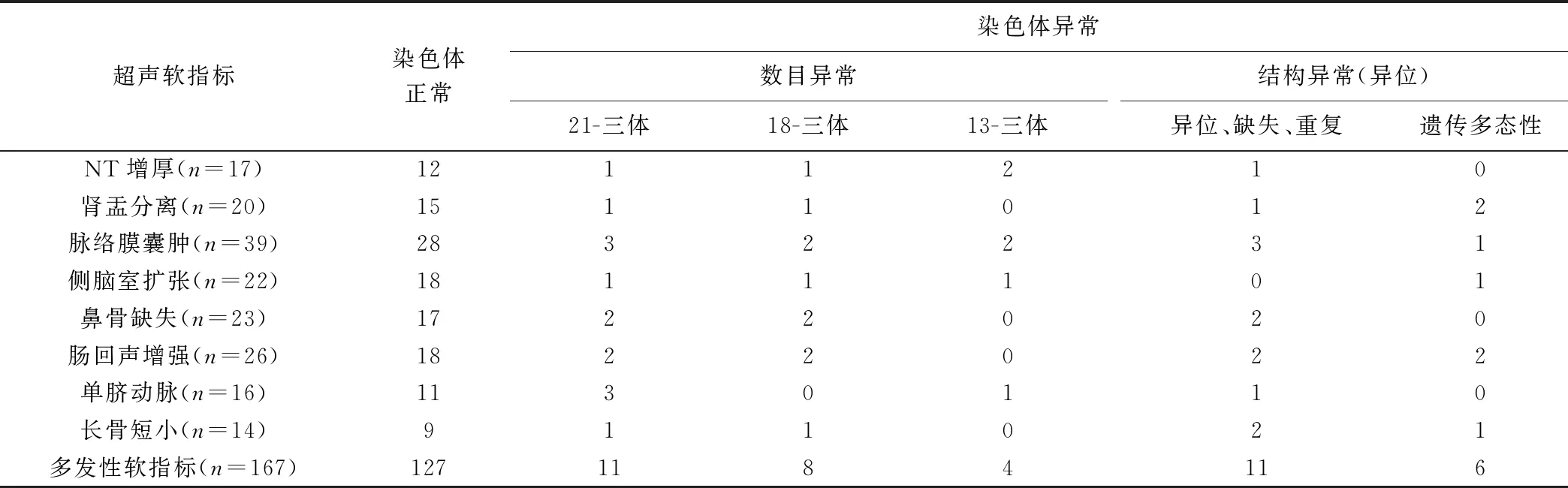
表1 胎儿超声软指标与染色体核型异常的关系(胎)

表2 胎儿超声软指标、母体血清AFP和HCG及联合检测对胎儿染色体异常的诊断价值[%(例)]
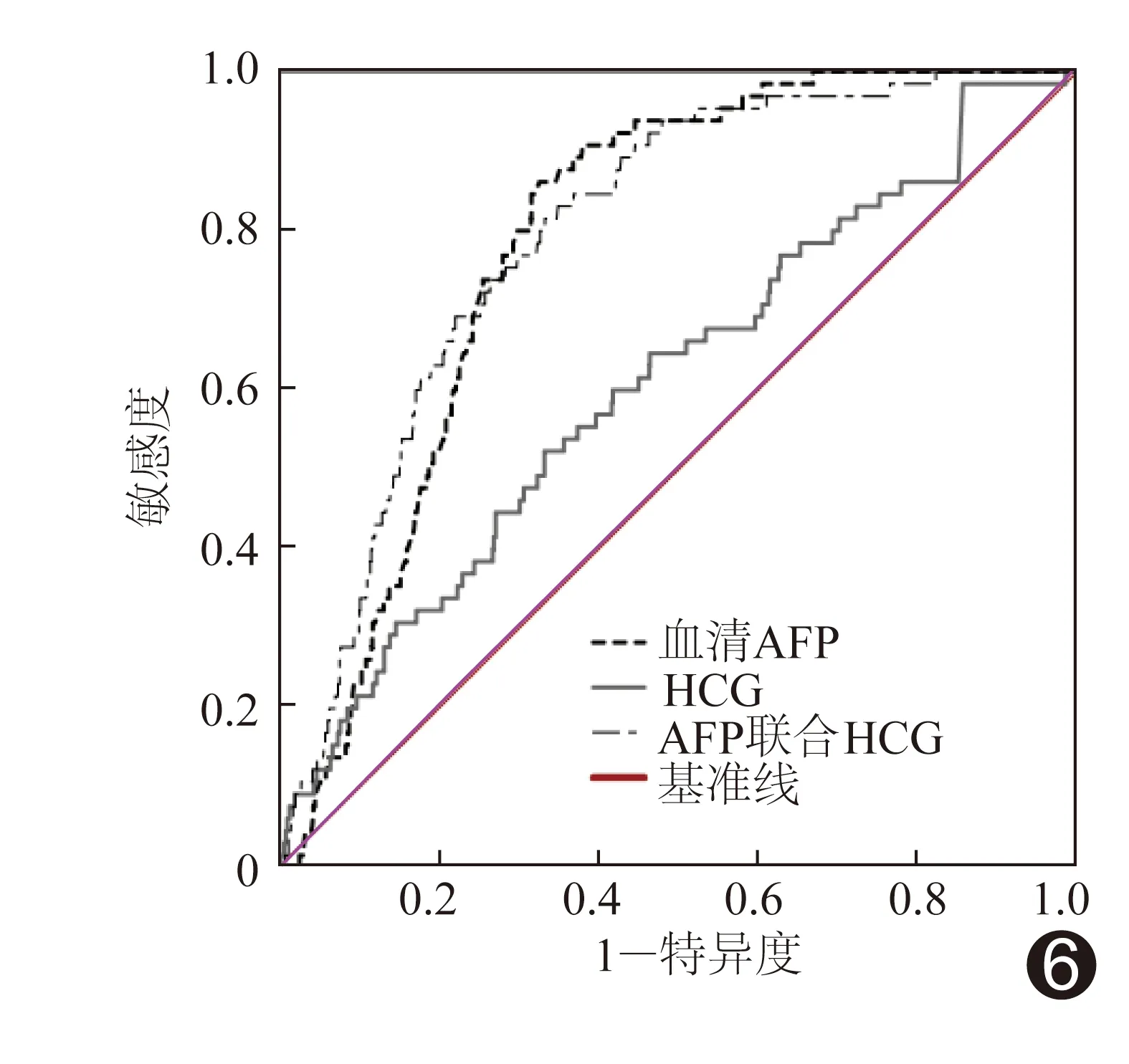
图6 母体血清AFP、HCG及联合筛查胎儿染色体异常的ROC曲线
3 讨论
出生缺陷是影响人口素质及社会稳定的重要原因之一。染色体异常可导致胚胎发育异常,为新生儿出生缺陷的主要原因。通过孕期筛查及产前诊断及时发现异常并终止妊娠,是减少或防止缺陷儿出生的主要环节[8]。产前诊断胎儿染色体异常的金标准是胎儿染色体核型分析,但均有创,流产率约为1%,仅适用于高危孕妇[9]。产前超声发现的胎儿微小异常被称为“软指标”[10],与染色体异常存在一定关联,GA 16~18周时超声软指标阳性提示发生严重畸形的风险增加[11]。本研究将167名胎儿2个以上超声软指标阳性的孕妇归入高危组,超声软指标筛查发现其中40胎胎儿染色体异常,包括23胎染色体数目异常、17胎结构异常,检出率62.50%,假阳性率7.82%,提示孕中期超声软指标检查可用于评估胎儿染色体异常风险,但检出率较低。
血清AFP、HCG是常见的反映胎儿染色体异常的二联血清标记物。血清AFP可在胎儿肝脏中合成,胎儿存在神经管缺损、无脑儿或脊柱裂等发育异常时,AFP可由开放的神经管进入羊水或母体血浆。因此,羊水或母体血浆AFP表达水平可用于产前检测胎儿发育异常[12]。HCG主要由胎盘细胞滋养层和中间细胞分泌,胎儿罹患唐氏综合征可使母体血清HCG水平明显升高。HSU等[13]于孕早期采用血清AFP、HCG二联法筛查唐氏综合征胎儿,检出率为68%。本研究中母体血清AFP联合HCG筛查胎儿染色体异常的敏感度为71.88%,特异度为93.66%,AUC为0.796,提示二联血清标记物诊断胎儿染色体异常的敏感度较低。
宋筱玉等[14]认为超声软指标联合检测母体血清AFP、HCG水平可提高孕中期诊断胎儿染色体异常的特异性。本研究结果显示,超声软指标结合联合检测母体血清AFP及HCG诊断胎儿染色体异常的敏感度高于单项指标,而特异度低于单项指标;超声软指标联合血清AFP、HCG诊断孕中期胎儿染色体异常的敏感度较高,达到98.44%,提示超声软指标联合血清AFP、HCG可有效筛查胎儿染色体异常孕妇,对其进一步行特异性较高的羊膜腔穿刺术及羊水细胞染色体核型检测有助于降低漏诊率,具有一定临床应用价值。
综上所述,孕中期超声软指标联合母体血清AFP、HCG检测可提高胎儿染色体异常的检出率。

