基于萘二酰亚胺的荧光探针的合成和甲醛检测
卢玉伟 康乐瑶 任雅斌 刘光仙 孔洁 肖立伟
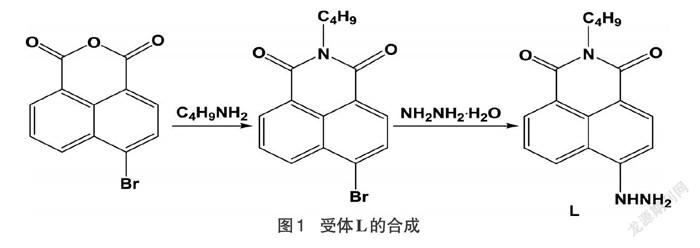
【摘要】以4-溴-1,8-萘二甲酸酐为原料,通过氨解、阱解等反应步骤合成了受体化合物L。采用荧光滴定法研究了受体L与甲醛间的相互作用情况,结果表明,受体L表现出对甲醛较好的识别作用,检出限为6.05×10-6mol/L。通过核磁滴定实验验证了受体L与甲醛之间的作用机制,即L中的肼基(-NHNH2)与甲醛缩合形成腙,导致体系荧光增强。
【关键词】荧光探针;萘二酰亚胺;甲醛检测
〔中图分类号〕O621.2〔文献标识码〕A 〔文章编号〕1674-3229(2021)04-0070-04
甲醛是重要的化工原料,在建材、家具、化妆品、塑料、医药等方面应用广泛。但是甲醛也是室内主要的污染物之一,会引发多种疾病,已经被世界卫生组织认定为一类致癌物,严重威胁人们的健康[1-2]。因此,开发检测和吸收甲醛的有效方法和技术对环境科学和医学等领域具有重要意义。
当前已经发展了多种方法用于甲醛检测[3-4],如色谱法、电化学分析法、差分光学吸收光谱、离子流管质谱法等,但上述方法存在样品处理繁琐、需要昂贵的仪器辅助等缺点。荧光探针是近年来发展起来的一种新型检测技术[5-6],具有操作简便、灵敏度高、能对活细胞内的目标物实时监测和原位成像等优点,已经成为科学研究、临床诊断和生产生活中对多种物质进行检测的理想工具[7-8]。荧光探针分子一般由荧光基团和识别基团构成,根据被检测物反应前后荧光信息的变化,对目标物进行分析。1,8-萘二酰亚胺是一种重要的荧光材料,具有稳定性好、斯托克斯位移大、荧光量子产率高等优点,是优良的D-π-A电子体系和荧光基团骨架[9-10]。我们[11]曾经设计合成了一种含1,8-萘二酞亚胺的荧光探针,对氟离子表现出很好的识别性能(检出限达到 8.06×10-7mol/L)。
基于此,本文设计合成了受体化合物4-肼基-1,8萘二酰亚胺L,并探讨了受体L与多种活性羰基化合物间的相互作用情况,结果表明,受体L对甲醛具有较好的选择性识别作用。
1 实验部分
1.1 试剂和仪器
实验所用的试剂为分析纯,使用前未进一步纯化。荧光光谱由F-4600型荧光分光光度计(日立公司)测定;氢谱和碳谱由Bruker Ascend-400MHz型核磁共振波谱仪(Bruker公司)测定;高分辨质谱由Shi-madzu LCMS-IT-TOF质谱仪(岛津制作所)测定。
1.2 受体L的合成步骤
中间体N-丁基-4-溴-1,8萘二甲酰亚胺的合成:取2.8g(0.01mol)4-溴-1,8萘二甲酸酐和1.8mL的正丁胺,溶于10mL无水乙醇中,搅拌下回流4h,溶液颜色变为棕褐色,趁热过滤,冷却,滤液中有晶体析出,抽滤,乙醇洗涤,晾干,得白色固体2.5g,产率约78.0%。m.p.203-204℃;1H NMR(400 MHz,DMSO-d6)δ:8.60(d,J=7.2 Hz,1H),8.51(d,J=8.8 Hz,1H),8.36(d,J=7.8 Hz,1H),7.98(d,J=8.2Hz,IH),7.79(t,J=7.9Hz,1H),4.22-4.01(m,2H),1.63-1.65(m,2H),1.37-1.39(m,2H),1.17-1.18(m,2H),0.91(t,J=7.3Hz,3H).
受体N-丁基-4-肼基-1,8萘二甲酰亚胺L的合成:取2.2g(0.067mol)上述中间产物和5mL80%水合肼溶于10mL无水乙醇中,搅拌下回流4h,反应体系溶液变成橙色,冷却,抽滤,乙醇洗涤,晾干,得黄色固体1.5g,产率80%。m.p.228~230℃;1H NMR(400MHz,DMSO-d6)δ:9.12(s,1H),8.61(d,J=7.8Hz,1H),8.52(d,J=8.3Hz,1H),8.04(d,J=8.2Hz,1H),7.65(t,J=7.6Hz,1H),6.57(s,1H),4.67(s,2H),3.84(s,2H),1.71-1.68(m,2H),1.50-1.39(m,2H),1.26-1.22(m,2H),0.96(d,J=7.4Hz,3H);13C NMR(101MHz,DMSO-d6)δ:164.3,163.4,153.7,134.7,131.0,129.8,128.7,124.6,122.2,118.9,107.8,104.5,40.3,29.6,20.3,14.1;HR-Ms:calculatedfor C16H17N3O2[M+H]m/e 284.1354,found 284.1352.
1.3 緩冲溶液的配制和甲醛溶液的标定
缓冲溶液的配置:按照参考文献[12]进行。取0.135、KH2PO4,0.71g Na2HPO4,4g NaCl和0.1gKCl,加水溶解,通过盐酸调节pH值至7.4,定容到500mL。
甲醛溶液的标定:选用市售甲醛或多聚甲醛,参照文献[13],采用碘量法进行标定。
1.4 荧光测定实验
配制0.2mmol/L的受体L的DMSO溶液和20mmol/L的活性淡基化合物的DMSO溶液。各取1mL主客体溶液,加入10mL容量瓶中,加入缓冲溶液和DMSO的混合液(VN=4/6)摇匀,定容。混合液超声处理0.5h,静置0.5h,依次进行荧光测试。激发波长为440nm,负高压为400V,狭缝宽度为10nm。
1.5 荧光滴定和核磁滴定实验
配制浓度为20μmol/L受体溶液和一系列梯度浓度的甲醛溶液(0~200μmol/L)加入缓冲溶液和DMSO的混合液(V/N=4/6)摇匀,混合液超声处理0.5h,静置0.5h,依次进行荧光测试。
核磁滴定实验时,配制浓度为2×10-3mol/L的受体L的DMSO-d6溶液,测定氢谱。加入等量的甲醛,混匀,超声处理1h,再次测定氢谱,前后比较。
2 结果与讨论
2.1 受体与不同羰基化合物的相互作用情况
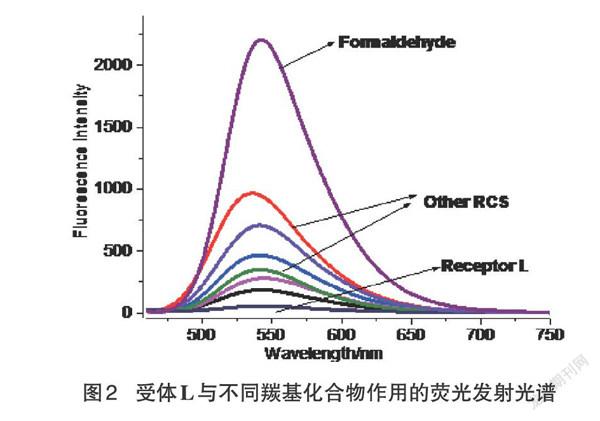
选取代表性的活性羰基化合物(RCS),如甲醛、乙醛、乙二醛、丙醛、苯甲醛、丙酮、环己酮等,与受体L相互作用后的荧光光谱如图2所示。受体L与上述羰基化合物作用后,体系的荧光发射光谱强度会有不同程度的增加,其中受体L中加入甲醛后体系荧光强度幅度最大,达到了加入前的30多倍,差别明显。
2.2 受体L与甲醛相互作用的荧光滴定
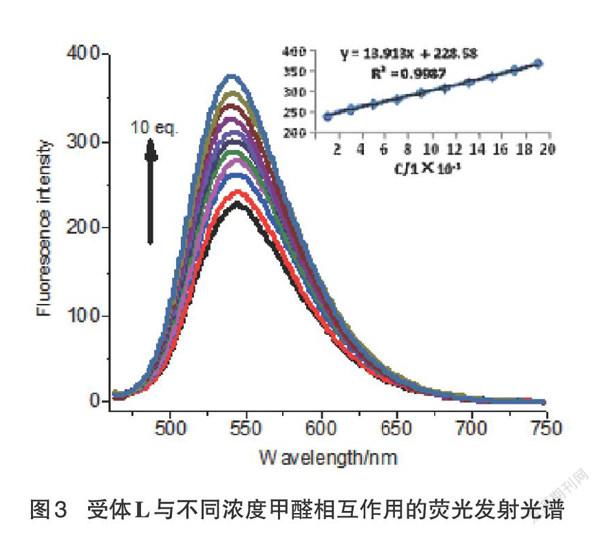
将不同浓度梯度(0~10eq)甲醛溶液分别加到受体L溶液(20μmol/L)中,混合体系的荧光光谱如图3所示。随着甲醛浓度的提高,在542nm处最大荧光强度呈现依次递增趋势,并在一定浓度范围内呈现线性关系。
以不同梯度浓度的荧光强度峰值和浓度(542nm)做曲线,归纳其线性方程为:Y=13.913x+228.58,相关系数R=0.9987,标准偏差为σ=1.4029,通过公式3σ(2×10-5)/s计算出检出限为6.05×10-6mol/L。
2.3 羰基化合物对受体L与甲醛相互作用的干扰
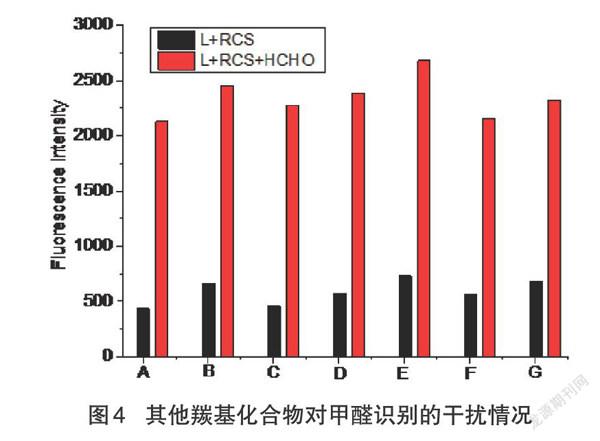
分别在受体L和乙醛、乙二醛、丙醛、苯甲醛、三氯乙醛、丙酮、环己酮等代表性羰基化合物的混合体系中加入等量甲醛,研究上述羰基化合物的存在对受体L与甲醛识别的影响。如图4所示,上述羰基化合物的存在对受体L与甲醛间的相互作用影响不大,说明受体L对甲醛的识别具有较好的选择性。
2.4 受体L对甲醛识别的机理探讨
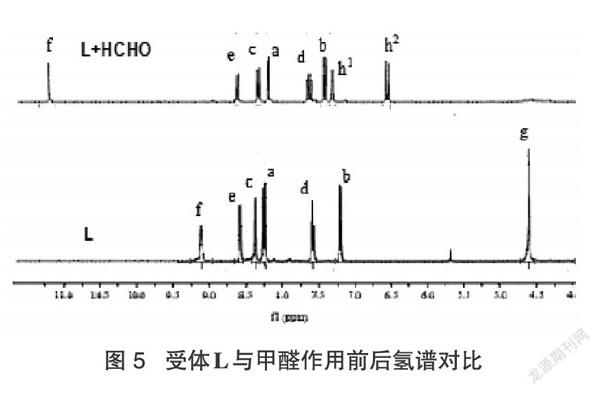
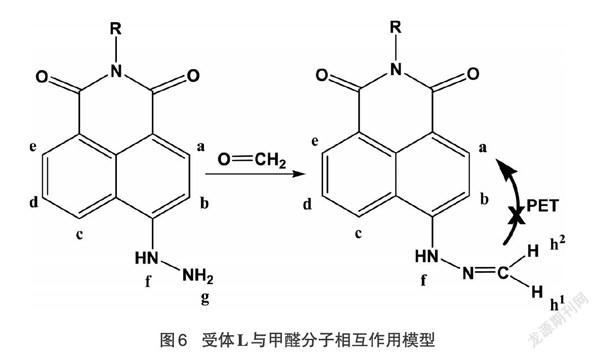
核磁滴定实验是研究分子间相互作用的重要手段。如图5所示,受体L与甲醛作用后,在氢谱中,受体中肼基-NH-的化学位移值由原来的9.12向低场迁移至11.2,可能是由于受体中肼基与甲醛形成腙后,希夫碱双键的各向异性及吸电子效应所致。在7.43和6.69分别出现了两个烯氢的信号,而4.70处代表肼基中-NHZ的信号消失。说明甲醛与受体L中的肼基发生缩合反应生成了腙,体系中光诱导电子转移(PET)受阻,导致荧光显著增强[12丁(图6),受体L显示出对甲醛的良好识别作用。由于位阻及电子相应的影响,其他羰基化合物与受体L的反应速度或程度不及甲醛,因而荧光增强程度不如甲醛明显。
3 结论
综上所述,合成的受体4-肼基一1,8萘二酰亚胺L对甲醛有较好的选择性识别作用,其作用机理是甲醛与肼基形成了腙,导致荧光增强是一种理想的甲醛荧光探针。
[参考文献]
[1]Salthammer T,Menteses S,Marutzky R.Formaldehyde inthe indoor environment[J].Chem Rev,2010,110(4):2536-2572.
[2]Zhang L,Steinmaus C,Eastmond D A,et al.Formalde-hyde exposure and leukemia:A new meta-analysis and po-tential mechanisms[J].Mutat Res-Rev Mutat,2009,681:150-168.
[3]Takeuchi A,Takigawa T,Abe M,et al.Determinationof formaldehyde in urine by headspace gas chromatogra-phy[J].B Environ Contam Tox,2007,79(1):1-4.
[4]Chen J,Chen K,Han B,et al.A novel single-fluoro-phore-based ratiometric fluorescent probe for detection offormaldehyde in air[J].Tetrahedron,2020,76(50):131681.
[5]Li X,Gao X,Shi W,et al.Design strategies for water-solu-ble small molecular cbromogenic and fluorogenic probes[J].Chem Rev,2014,114(1):590-659.
[6]Kikuchi K.Design,synthesis and biological application ofchemical probes for bioimaging[J].Chem Soc Rev,2010,39:2048-2053.
[7]XU Z,Chen J,Hu L-L,et al.Recent advances in formalde-hyde-responsive fluorescent probes[J].Chin Chem Lett,2017,28(10):1935-1942.
[8]吳少平,阮淞淞,宋欢欢.荧光探针法检测活性羰基化合物甲醛的研究进展[J].西北大学学报(自然科学版),2019,49(4):538-557.
[9]谢振达,付曼琳,尹彪,等.1,8-萘酰亚胺类荧光探针在双光子成像中应用的研究进展IJ].有机化学,2018,38(6):1364-1376.
[10]Nasirian A,Tikum A F,Fortibui M M,et al.Nap-thalimide-based fluorescent probe for selective and sen-sitive sensing of formaldehyde and biological applies-tions[J].Dyes and Pigments,2021,188:109156.
[11]Xiao L,Ren L,Li Z,et al.A selective naph-thalimide-based colorimetric and fluorescent chemosen-sor for“naked-eye”detection of fluoride ion[J].InorgChim Acta,2020,500:119207.
[12]Tang Y,Kong X,Xu A,et al.Development of atwo-photon fluorescent probe for imaging of endoge-nous formaldehyde in living tissues EJ].Angew ChemInt Edit,2016,55(10):3356-3359.
[13]尤铁学.碘量法标定二氧化硫和甲醛标准贮备溶液的改进[J].化学试剂,2008,30(6):447-448.
[收稿日期]2021-09-28
[基金项目]河北省大中学生科技创新能力培育专项(2021H100403);河北省高等学校科学技术研究项目(ZD2020153)
[作者简介]卢玉伟(2000-),女,廊坊师范学院化学与材料科学学院2018级材料化学专业学生。
[通讯作者]肖立伟(1970-),男,博士,廊坊师范学院化学与材料科学学院教授,研究方向:功能有机化合物的设计与合成。

