腹腔镜胃大部切除术后患者体温控制的相关研究
李志娟, 钱春格
(河南省人民医院/郑州大学人民医院, 1. 胃肠外科; 2. 普通外科, 河南 郑州, 450003)
腹腔镜胃大部切除术过程中患者易出现低体温现象,而人体凝血功能受到低体温的影响,导致手术中输血量和失血量增多,从而影响手术部位切口的愈合,极大影响了患者的术后康复[1-2]。胃大部切除术中患者的舒适度受低体温的影响而降低,延长了住院时间,增加了患者的医疗花费,加重经济负担[3]。临床上,术中体温控制得到重视,患者术后的体温控制却被忽略。本研究探讨体温控制对腹腔镜胃大部切除术后患者的影响,现报告如下。
1 资料与方法
1.1 一般资料
选取2017年1月—2019年3月均由本院同一手术小组行腹腔镜胃大部切除术的患者83例,依据是否对患者进行术中、术后体温控制分为实验组42例与对照组41例。实验组男22例,女20例,平均年龄(51.38±6.46)岁,体质量指数(BMI) (21.18±1.19) kg/m2, 心率(79.38±11.58)次/min, 耳温(36.12±0.19) ℃, 手术时间(140.58±70.78) min;对照组男20例,女21例,平均年龄(51.39±6.48)岁,BMI (20.56±1.29) kg/m2, 心率(78.78±12.11)次/min, 耳温(36.76±0.19) ℃, 手术时间(140.57±70.56) min, 2组基线资料比较差异无统计学意义(P>0.05), 具有可比性。纳入标准: 无手术禁忌证者; 认知功能良好者; 术前3 d无感染病史者; 麻醉方式相同者; 患者均知情同意; 本研究获得本院伦理委员会的批准。排除标准: 心肺功能差的患者; 术前体温超出正常范围者; 术中手术方法改变者。
1.2 方法
1.2.1 对照组: 术前宣教相关注意事项,讲解腹腔镜胃大部切除术的相关内容,获得患者及家属的积极配合和同意。术前不需要清洁灌肠,告知患者术前禁食时间及目的; 术前2 h口服10%葡萄糖500 mL, 不进行鼻胃管置入术,术前静滴加有抗生素的液体。术中给予短效麻醉药物静脉给药,采用全麻手术方式,开始麻醉后即使用充气式保温毯保温。术中给予患者提前加温至37 ℃的液体进行冲洗,采用5孔法腹腔镜胃大部切除术。如果患者的体温在术中出现变化,则不给予保暖处理。手术结束放置1根腹腔引流管于吻合口处,进入复苏室后,对患者进行常规术后管理,静脉输入室温液体,患者身下不放置保温毯。
1.2.2 实验组: 与对照组相比,术中输液使用在加温箱中提前加温后的液体。实施麻醉、开始手术后,监测并记录不同时间段患者的耳温、直肠温度及心率。手术结束后,由麻醉恢复间的责任护士继续观察。当患者的体温出现异常时给予保温措施,确保不发生低体温现象。操作方法: 调高充气式保温毯温度至37 ℃; 将冲洗腹腔的液体温度调高至37 ℃; 发生特殊情况时手术暂停。同时观察患者的生命体征,尤其是患者血压、心率的变化情况。术后转运床上,患者继续使用充气式保温毯。麻醉复苏间护士及病房护士都采用加温过的液体,静脉输入,保温至术后8 h。
1.3 观察指标
监测术后血压、心率、耳温。入手术室时至手术结束时患者的直肠温度进行比较。严格按炎症因子检测标准抽取静脉血,检测2组患者炎症因子水平,应用放射免疫分析法(上海研卉生物科技有限公司)检测白细胞介素-6(IL-6)和血清肿瘤坏死因子-α(TNF-α)。
1.4 统计学方法
2 结 果
2.1 耳温、心率水平比较
对照组术后各时点耳温低于实验组,心率高于于实验组,差异有统计学意义(P<0.05), 见表1。
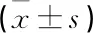
表1 术后耳温、心率变化比较
2.2 直肠温度比较
实验组术中各时点及手术结束时直肠温度均高于对照组,差异有统计学意义(P<0.05), 见表2。
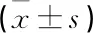
表2 术中直肠温度比较 ℃
2.3 炎症因子水平比较
术前2组炎症因子水平比较,差异无统计学意义(P>0.05); 术后实验组炎症因子水平低于对照组,差异有统计学意义(P<0.05), 见表3。
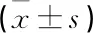
表3 炎症因子水平比较
3 讨 论
腹腔镜胃大部切除术过程复杂、手术时间长,腹腔不仅需要冲洗而且暴露面积较大,因此手术中低体温现象很常见。低体温会降低组织器官代谢率,保护组织器官,但是也会降低机体的免疫功能,使凝血机制受到影响,影响人体的循环系统功能,增加血液循环系统中各血管阻力,造成血压下降、心动过速、心律失常、心肌缺血的发生[4]。
本研究结果表明,与对照组比较,实验组患者术中直肠温度提高,术后心率减慢,耳温提高,患者术后生命体征更加稳定。分析原因,术后对患者进行保温,人体应激反应程度减轻,患者术后复苏时间缩短,减少了因体温下降导致的躁动、寒颤,使人体耗氧量降低,血液内含氧量增加,生命体征更加稳定,降低腹腔镜胃大部切除术术后并发症的发病率[5]。研究[6]表明,应用水循环温毯仪加充气式暖风毯进行保温,可以使手术过程中患者的生命体征维持相对稳定,为手术的顺利进行创造了有利条件。与薄被、电热毯、温控水垫相比,充气式保温毯保温效果更好[7]。
术中低体温会对患者术后炎症反应产生较大影响[8], 临床上所有的炎症因子在反应过程中,出现最重要、最早的炎性介质是TNF-α; 然而 IL-6可以使B细胞产生抗体和分化,是炎性反应的催化剂[9]。这2种炎症因子水平升高表明手术部位切口感染率升高。本研究结果显示, 2组术后IL-6、TNF-a水平均较术前升高,而实验组术后IL-6、TNF-a水平低于对照组,表明体温控制可以降低胃大部切除术后炎症因子水平。分析原因,术中体温对术后的应激炎症反应有很大影响。研究[10]发现,转化生长因子β(TGF-β)与体温和炎症反应的相关性有关,抗炎作用与TGF-β表达呈正相关关系,并且体温高低影响表达通路。因此,恰当的体温控制能影响TGF-β表达通路,从而降低炎症因子水平。其他研究[11]发现,术中采取综合保温措施可以降低胃大部切除术患者术后IL-6和血C反应蛋白的浓度,与本研究结果类似。
综上所述,体温控制有助于增加腹腔镜胃大部切除术后患者生命体征的稳定性,降低炎症因子水平和术后感染的风险。

