改良JAPAS截骨治疗陈旧性Lisfranc复合体损伤继发僵硬高弓畸形
陈宇 张晖 李亚星 邓伟 刘熹 秦博泉 任毅 吴仕舟
(四川大学华西医院骨科,成都 610041)
Lisfranc关节复合体损伤多为高能量损伤,不仅损伤Lisfranc关节,还常累及跖骨、跗骨以及骨间韧带、关节囊等软组织[1]。常表现为严重的骨折脱位、软组织开放伤以及血管神经损伤[2]。早期的复位固定或关节融合手术都能获得良好的临床结果[3]。但倘若早期因软组织危象或感染等多种因素未得到妥善处理,继而就会发展为陈旧性损伤,使得跖列关系紊乱,形成中足高弓或者平足,同时伴随着前足的内收或者外展[4,5]。既往的文献报道对于陈旧的Lisfranc骨折采用关节融合术[6],获得了良好的结果。但对于陈旧的Lisfranc复合体损伤继发僵硬高弓的患者来说,不仅有Lisfranc骨折脱位,也存在中足足弓的异常,单纯的跖楔关节融合术不能解决中足高弓的畸形,继而改变了足部生物力学关系导致前足以及后足的疼痛、畸形、创伤性关节炎等,治疗非常棘手。本课题组基于陈旧Lisfranc损伤后继发僵硬高弓畸形的病理以及JAPAS提出的治疗前足马蹄畸形的手术方法,提出并采用改良的中足截骨策略(改良的JAPAS截骨)治疗了21例不同程度单足陈旧性Lisfranc复合体损伤继发僵硬高弓畸形,现报道如下。
1 资料与方法
1.1 纳入与排除标准
纳入标准:①诊断明确的陈旧性Lisfranc复合体损伤且合并僵硬高弓畸形(负重侧位X线片上测量的Meary角大于5°、中足畸形顶点CORA点在中足平面及中足平面丧失活动度);②保守治疗无效,且接受截骨内固定手术;③随访资料完整,随访时间超过1年。
排除标准:①入院时小于3周的Lisfranc骨折脱位或陈旧Lisfranc复合体损伤伴平足畸形;②入院时已确诊感染或者因皮肤软组织条件差无法行内固定手术;③年龄较大或者合并多种内科疾病无法采用手术治疗;④Lisfranc复合体损伤伴有严重的僵硬型后足或者小腿畸形,需要辅助多种矫形术式。
1.2 研究对象
2014年1月至2016年1月四川大学华西医院共收治陈旧性Lisfranc复合体损伤继发高弓畸形患者29例。依据上述纳入与排除标准,最终21例患者纳入本研究。其中男13例,女8例,年龄29~55岁,平均年龄(41.9±12.9)岁。均为单足,右足14例,左足7例,手术时患足皮肤均完整无破溃。损伤原因:高坠伤8例,交通伤9例,重物压伤4例。受伤至本次就诊时间为3.0~10.1个月,平均(4.7±0.9)个月。所有患者均因走路时疼痛、不能持续负重而就诊,入院均行患足负重正、侧、斜位X线及三维CT检查。Myerson分类A类7例,B类4例,C类10例。所有患者根据Meary线测量分型(图1)均为中足高弓畸形,且均为僵硬型,正、侧位距骨第一跖骨角(Meary角)平均为(17.2±5.1)°、(32.8±6.9)°。4例患者出现爪形趾畸形,5例患者合并踝跖屈畸形,平均背伸角度为(-12.6±6.2)°。1例患者合并胫神经损伤,3例患者合并腓深神经损伤,2例患者合并腓肠神经损伤。21例患者中吸烟4例,糖尿病患者2例。

图1 术前X线片测量Meary角
1.3 手术方法
患者于全身麻醉下进行手术,取仰卧位,同侧臀部下方垫高,大腿近端放置止血带,控制压力在240~260 mmHg(1 mmHg=0.133 kPa)。术中内固定选用3.5系统中足锁定接骨板(美国Wright公司)。
1.3.1 中足畸形矫正:患者均于足背正中行6 cm长的纵向切口。锐性分离拇长伸肌腱和趾长伸肌腱,在其间探查分离足背动脉及腓深神经予以保护。首先根据术前X线片确定中足畸形在冠矢状面的顶点(CORA点),用电锯或骨凿与骨刀按下面方法做“V”形截骨:“V”形截骨线的内侧边起始于内侧楔骨,紧靠第一楔跖关节内侧;外侧边则位于骰骨,在第五骰跖关节的稍远侧将这两条截骨线向远侧延长相交于足中线上、高弓足畸形的顶点,一般在中间楔骨上,注意截骨线不要进入舟楔关节。完成截骨后,牵引远侧端并用骨膜剥离子把其近侧缘压向跖侧,同时抬高跖骨头以在矢状面消除畸形。同一切口内显露第二、三、四跖跗关节,检查有无跖列的冠状面的畸形,如有可在跖楔关节平面的骰骨处进行小的楔形截骨,并将截骨的楔形骨块植骨于内侧柱,用于消除冠状面的畸形(图2)。将克氏针临时固定中足,术中C型臂透视满意后,在中足安置锁定接骨板,3.5 mm螺钉固定,内外侧柱交叉克氏针固定。术后4~6周拔出。手术切口无张力缝合。
1.3.2 前足足趾矫正:前足爪型跖的矫正需在中足以及Lisfranc关节复合体矫正后处理。由于爪形趾多由足内在肌肌力不平衡继发或者畸形后肌腱滑动行程变短,粘连所致。足弓矫正后,如爪形趾自行恢复或者屈曲张力降低,则不予再次处理,术后采用支具或者康复训练矫正;如足弓纠正后,爪形趾仍存在,则可行趾屈肌腱松解延长,或者跖趾关节成型松解矫正畸形。而趾间关节僵硬的患者则行趾屈肌腱切断,或趾间关节融合术。
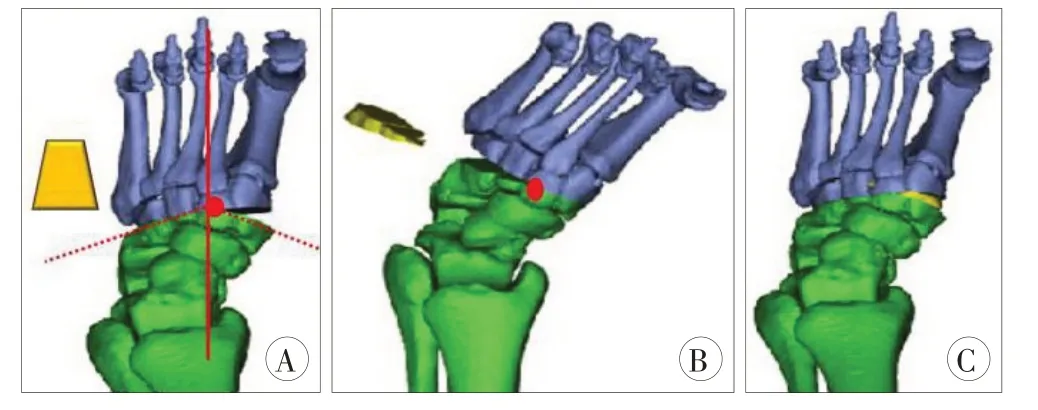
图2 改良JAPAS截骨
1.4 围手术期处理
患者术前采用一代或二代头孢类抗生素或者克林霉素预防感染。术后常规24~48 h内停用抗生素。术后第1天指导患者进行下肢等长肌力收缩训练以及直腿抬高训练,术后2周左右非负重下地活动,术后8周穿戴前足减压鞋进行部分负重行走功能训练,术后12周后逐步增加负重恢复到正常行走。
1.5 随访及观察指标
术后第1、3、6、9、12个月门诊随访,以后每年随访1次。随访评估足部畸形矫正质量:X线正位片上测量距骨第一跖骨角(正位Meary角),正常值范围为(0±5)°;X线侧位片上测量距骨第一跖骨角(侧位Meary角),正常值范围为(0±5)°。记录患者日常活动情况、步态、疼痛视觉模拟评分(visual analogue score,VAS)、踝关节活动度和美国足踝外科协会(American Orthopaedics Foot and Ankle Society,AOFAS)评分[7]。
1.6 统计学方法
采用SPSS 20.0统计学软件进行统计学分析。计量资料经统计学分析均符合正态分布,以表示。采用两独立样本t检验比较末次随访时与术前疼痛VAS评分、AOFAS评分、Meary角差异。以P<0.05为差异有统计学意义。
2 结果
所有患者均获得随访,随访时间36~60个月,平均随访(36.7±7.5)个月。19例患者切口均甲级愈合。2例患者发生足背切口延迟愈合,伤口换药后分别于术后第18天和第24天愈合。骨愈合时间为16~28周,平均(18.2±2.7)周。末次随访时,患者临床症状均明显改善,无骨不愈合、畸形愈合以及迟发性感染。术后1例患者出现止血带麻痹,口服神经营养药物,约术后第7天恢复。1例患者发生腓深神经损伤。
末次随访时,患者疼痛VAS评分、AOFAS评分均较术前改善,正、侧位Meary角均较术前减小,且差异均有统计学意义(表1)。典型病例见图3。
3 讨论
3.1 陈旧性Lisfranc复合体继发高弓畸形的病因以及机制
Jeremy等[8]发现,Lisfranc损伤患者的高弓足比普遍人更常见。不管是高能量的还是低能量的Lisfranc损伤都可能导致高弓足的产生,但机制存在一定的差异性。低能量的Lisfranc高弓多由于踝关节扭伤,腓骨肌腱疾病等产生的中足生物力学改变有关,但具体机制不明。而高能量的Lisfranc高弓多由于巨大暴力不仅导致跖跗关节的骨折脱位,还损伤了Lisfranc复合体韧带(包括跖楔韧带,楔骨间韧带及跗骨间背侧韧带等)[9-11],往往伴随严重的软组织损伤,甚至还导致严重的神经血管损害或足间隔内的骨筋膜综合征[12]。正是由于严重的皮肤软组织或者血管神经危象,使得早期的复位固定术或者关节融合术无法进行[13]。
表1 患者末次随访时疼痛VAS评分、AOFAS评分及正、侧位Meary角与术前比较(n=21,)
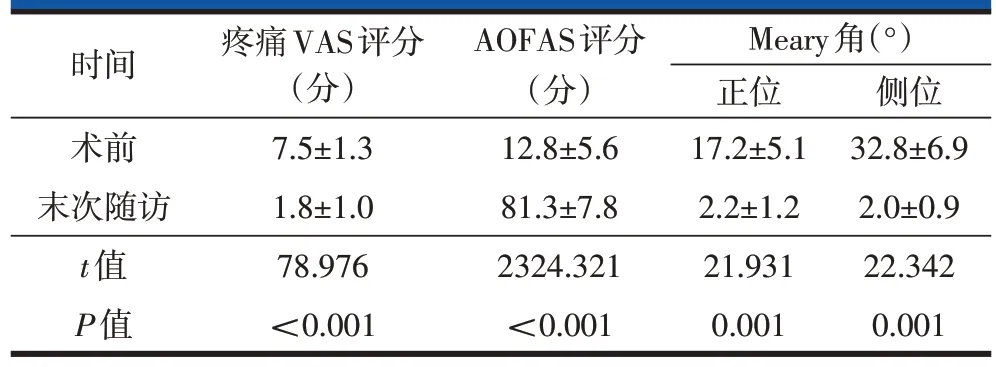
表1 患者末次随访时疼痛VAS评分、AOFAS评分及正、侧位Meary角与术前比较(n=21,)
陈旧性Lisfranc复合体继发高弓畸形患者的受伤机制多为直接暴力使Lisfranc关节复合体向背侧成角,同时伴随着前足的外展或内收以及旋前或旋后[14]。伤害程度取决于受伤当时暴力的方向及大小[15]。本组8例为高坠伤,9例为交通伤,4例为重物压伤。均为高能量损伤,虽然患者就诊手术时无皮肤破损或者感染,但所有患者早期都存在软组织危象,无法早期及时处理。本次就诊时患者足部小关节已出现僵硬,无法行走。此类患者多合并踝以及前足的畸形和血管神经损伤,本组研究中4例患者出现爪形趾畸形,5例患者合并踝跖屈畸形。1例患者合并胫神经损伤,3例患者合并腓深神经损伤,2例患者合并腓肠神经损伤。
3.2 中足截骨的优缺点

图3 患者男,38岁,右足陈旧Lisfranc复合体损伤伴僵硬型中足高弓畸形,行中足改良JAPAS截骨术治疗
陈旧性Lisfranc复合体损伤继发高弓畸形,是三维立体状畸形,除了矢状面的中足高弓畸形外,往往伴随着冠状面的畸形,常表现为前足的内收或外展[16]。除此之外往往还伴随着足趾的屈曲畸形。那么对于这类患者的处理不应仅仅局限于骨折复位或者关节融合,而要考虑已存在的中足多平面畸形及合并的前足畸形的矫正。因为一个平面的矫形必然影响其他平面,同时还需要考虑到周围软组织挛缩对矫形的影响,可见这种矫形技术必然是十分复杂困难的。既往文献报道的矫形方案中以中足截骨的报道最多,包括Cole、Japas、Jahss和Akron等,但目前还没有一种截骨方案能完美解决所有畸形问题[17]。Tullis等[18]报道的Cole截骨方法是在舟楔关节及骰骨背侧作楔形闭合截骨,其优点在于操作简单,结构稳定,截骨后愈合率很高,有很强的纠正高弓的作用。但是由于这种方法主要是通过楔形截骨后将前足推向背侧,即背向旋转来获得矫形,因此并没有足够的矫正旋转和内收的作用,属于单平面矫形。另外由于去除了较大一部分楔形骨块,所以会造成足的短小,使术后双足外形不对称,患者选鞋困难。Zhou等[19]报道的背侧楔形截骨与Cole截骨具有一定的类似性,但他将截骨的范围限制在楔骨以及骰骨内,极大程度的保留了中足的部分关节,避免关节退变。但也存在类似Cole截骨单平面矫形的缺点。Japas[20]报道的截骨在Cole截骨基础上做出了改进,在舟楔关节和骰骨间作“V”形截骨,再通过滑移和旋转矫正畸形。这是第一种能够在三维空间获得矫形效果的截骨方法,能够同时矫正高弓、前足内收及旋前。同时,由于不再需要去除部分骨质,因此术后患者并不会出现明显短缩变小。然而,受制于当时有限的内固定方法,需要借助榫卯结构才能获得截骨后断面间的足够稳定性,因此采用了“V”形截骨以增加截骨断面间的接触面积及相互的限制。然而,正是由于这种限制,阻挡了侧方移动,使其矫正内收的作用十分有限。在此之后,陆续又有研究者提出了Jahss截骨和Akron截骨。Jahss[21]报道的截骨方法是通过小切口分别在各个跖楔关节处截骨,能够对每个跖列单独进行调整,相对较为精巧,但严格的说这种截骨已经不是中足截骨,对于中足畸形,不在畸形顶点截骨,势必很难完全矫正畸形,且它牺牲了跖楔关节的活动度,增加了术后足的僵硬程度。Wilcox和Weiner[22]报道的Akron截骨通过在跖骨及骰骨内弧形截骨后滑动来矫正畸形,拥有比较强的三维空间矫形能力,且不会丢失骨质,不牺牲舟楔、跖楔关节活动度。但是当遇到严重的畸形时,需要极度的滑动才能达到矫形的目的,这可能导致截骨断端间接触面积不足而影响愈合。这种截骨方法需要较广泛的暴露,因此常常需要通过一个横行切口来完成,此切口神经血管及皮肤并发症风险较高。另一方面,需要特殊的弧形骨刀才能完成。
3.3 改良JAPAS截骨的优缺点
因此,正是上述的不同截骨方案的局限性,特别是Akron截骨提出后,仍有研究者在不断尝试提出新的截骨方法或对原有截骨方法进行改进,从而提高矫形效果。本课题组常采用中足畸形顶点多平面截骨的方案是基于JAPAS截骨改良而来的。本课题组尝试在JAPAS的基础上,对JAPAS截骨进行了进一步的改良,改良的JAPAS截骨操作中的“V”形双臂都沿楔骨和骰骨内部进行,其“V”形截骨方式保留了距舟、跖楔、跟骰关节的活动度,不会丢失太多的骨质造成术后患足短小,且能够同时矫正高弓、内收及旋转,是一种有很多优点的截骨方法。这种方法拥有较强的矫正中足冠矢状双平面上的畸形,可以在C型臂定位引导的条件下,通过相对微创的方法用简单的骨刀或摆锯完成,且可以根据畸形个体特征灵活调整。从本组结果来看,对于矢状面近35°,冠状面近20°以内的畸形,通过本课题组的改良方法能一次矫正,并不会明显增加软组织以及血管神经的并发症,本组无严重的软组织并发症,2例患者伤口并发症均为浅表瘢痕皮肤边缘坏死,1例患者发生血管神经并发症。
改良的JAPAS截骨与中足的关节内截骨相比,如果患者中足的关节仍有活动度的话,中足关节内的截骨是具有一定优势的,因为它最大程度的保留了中足诸关节的活动度。比如先天的马蹄高弓畸形的患者,中足的关节活动度大部分都尚好,应优先选择关节内截骨。但对于本研究中的目标人群来说,中足的关节因为创伤而丧失活动度变为僵硬,中足小关节已出现退变,改良的JAPAS截骨即使破坏了关节面对患者的预后也没有什么影响,但相反,此种截骨方式简单易行,可以更大的角度调整双平面的畸形,具有更大的优势。
当然,该方法也有一些不足之处。由于“V”形的阻挡,矫正冠状面上内收外展的能力是很有限的。同时,在不影响矫形效果的前提下,应尽量保留更多的关节活动度,以避免术后足的僵硬。需要比较好的三维空间判断能力,足够的经验和反复C型臂透视才能完成。其次,由于将改良JAPAS的“V”形压缩到了楔骨和骰骨的内部,截骨后断面间的稳定性弱于经典的JAPAS截骨,因此需要更加可靠的内固定,例如多枚空心螺钉或者钢板螺钉,术后建议用支具固定一段时间,并且需要适当延迟下地负重的时间。
综上所述,改良的JAPAS中足截骨策略可以多平面矫正陈旧Lisfranc损伤后继发僵硬高弓畸形,操作简便性,临床并发症少,是治疗陈旧Lisfranc损伤后继发僵硬高弓畸形的可行方法。

