建筑废旧竹木材料在环保中的应用试验研究*
林巧琴
(北京青年政治学院,北京 100102)
工业革命以来,大气中CO2浓度急剧增加,温室效应随之加重,引发了一系列环境问题,如全球变暖、土壤沙漠化、海平面上升等。为降低CO2排放量,CO2捕集和封存(CCS)被认为是最有前景的技术之一,在这项技术中,CO2捕集是最主要的组成部分[1-2]。目前,大规模捕集CO2的技术主要有吸附、吸收、膜分离等。其中吸附法由于设备简单、易操作、能耗低等优点被广泛研究,而吸附法的关键在于吸附剂的开发[3-4],研究有效的CO2吸附剂,减少CO2排放量,减弱温室效应已迫在眉睫[5]。近年来,金属有机骨架化合物(MOFs)、沸石分子筛、多孔有机聚合物(POPs)和多孔碳等吸附剂被纷纷提出,在众多吸附剂中,多孔碳材料由于制备简单、成本低、热和化学稳定性好、孔隙率易调控等优点脱颖而出。然而纯碳材料对CO2的吸附和选择能力都较差,在多孔碳材料中引入杂原子(N、S、P等),尤其是N元素,可以部分取代碳元素,调节孔道结构,改变材料表面特性,增强其亲水性,并影响材料表面的酸碱性,因而常被用于CO2吸附研究[6-8]。
本文选用建筑废料废旧竹木为前驱体制备多孔碳,不仅可实现对这类建筑废弃物的再利用,而且能实现对CO2气体的高效捕集。试验以KOH为活化剂,通过碳化-活化一步法制备多孔碳,通过调节活化温度来调节所得多孔碳的孔隙率和含氮量,研究了样品在不同温度下的CO2吸附量,以及对CO2/N2混合气体的分离能力。
1 材料与方法
1.1 材料
废旧竹木:建筑废料,购于木林森木材商城;氢氧化钾(KOH,分析纯)、盐酸(分析纯),天津大茂化学试剂厂。
1.2 设备
磁力搅拌器:SN-MS-M2 型,郑州生化仪器有限公司;管式炉:BTF-1200C,安徽贝意克有限公司;ElementarVario MICRO型元素分析仪,上海艾力蒙塔贸易有限公司;ESCALEAB 250Xi(Al Kα射线)光电子能谱仪,美国Thermo Fisher Scientific公司;D8 Advance型X射线衍射仪,德国Bruker公司;Confocal LabRam HR800 spectrometer光谱仪,法国HORIBA Jobin Yvon公司;ASAP 2060 型吸附仪,美国麦克仪器公司。
1.3 试验方法
1.3.1 样品处理
分别称取3 g废旧竹木和6 g KOH置于200 mL烧杯中,向其中加入80 mL去离子水,室温下剧烈搅拌12 h后,于80 ℃下加热搅拌至液体蒸干,然后将样品转移至瓷方舟并置于管式炉中,氮气氛围下于600、700、800 ℃活化90 min,待温度降至室温后,将样品取出,分别用1 mol/L HCl和去离子水洗涤至中性,最后于80 ℃烘箱中干燥12 h。得到的样品记为CA-x,其中x表示活化温度(600、700、800 ℃)。
1.3.2 产物表征
分别采用Elementar Vario MICRO型元素分析仪和ESCALE AB 250Xi型X射线光电子能谱仪检测样品的氮(N)元素含量和样品中氮元素的存在形式;采用D8 Advance型X射线衍射仪检测样品的结晶度,Kα辐射(λ=1.540 6 Å);采用Confocal LabRam HR800 spectrometer型拉曼光谱仪检测样品的缺陷程度;通过-196 ℃下N2的吸脱附曲线,利用ASAP 2060 型吸附仪分析样品的孔结构特性。
1.3.3 气体吸附性能测试
利用ASAP 2060 吸附仪测试0、25 ℃和50 ℃下CO2和N2的吸附-脱附等温线。测试前,先将样品在180 ℃下脱气15 h。
2 结果与分析
2.1 样品结构分析

图1 样品的N2 吸附-脱附等温线和孔径分布图Fig.1 N2 adsorption desorption isotherm and pore size distribution of the sample

表1 样品孔结构特性和氮含量Tab.1 Pore structure characteristics and nitrogen content of samples
图1(a)为所有样品的氮气吸附-脱附等温线,根据国际纯粹与应用化学联合会(IUPAC)的分类,这些等温线均属于I型,表明材料主要由微孔组成,吸附曲线与脱附曲线之间没有明显的迟滞环,且在低压区(P/P0<0.01)吸附量急剧增加,主要是因为微孔的毛细管凝聚效应所致,在中压区有相对平缓的吸收[9]。如表1 所示,活化温度从600 ℃升到700 ℃,样品的比表面积和孔体积分别为1 124.0~1 789.5 cm2/g和0.55~0.83 cm3/g,随着活化温度的升高,样品的比表面积和孔体积增大,说明活化过程中易挥发物质释放出来,生成了发达的微孔;当活化温度继续升高到800 ℃时,样品的比表面积和孔体积下降,过度活化,导致了孔道坍塌。图1(b)为样品的孔径分布图,所有样品的孔径集中在0.5~2 nm之间,说明样品由丰富的微孔构成,与氮气吸附-脱附等温线的结果一致,而据文献报道[10-11],微孔含量高对CO2的吸附是有利的。图2(a)是样品的XRD图谱,可以看出,所有样品都有两个比较宽的峰,约在2θ=24.8°和44.2°处,分别对应于无定型碳在(002)和(100)面的衍射,且随着活化温度的升高,这两个峰逐渐变宽,说明样品的无序度增加[12-13]。图2(b)是样品的拉曼光谱图,所有的样品都展现了两个碳的特征峰,一个是位于1 350 cm-1处的D峰,代表sp3杂化的具有结构缺陷的无定型碳;另一个是位于1 580 cm-1处的G峰,代表一阶散射E2g模式的对称,与2D的六边形sp2杂化的碳振动有关[14-15]。D峰与G峰的峰强度比值(ID/IG)通常用来表征碳材料的结构缺陷程度,随着活化温度的升高,ID/IG的值增加,说明样品的结构缺陷增多,无序度增加,与XRD的结果对应。
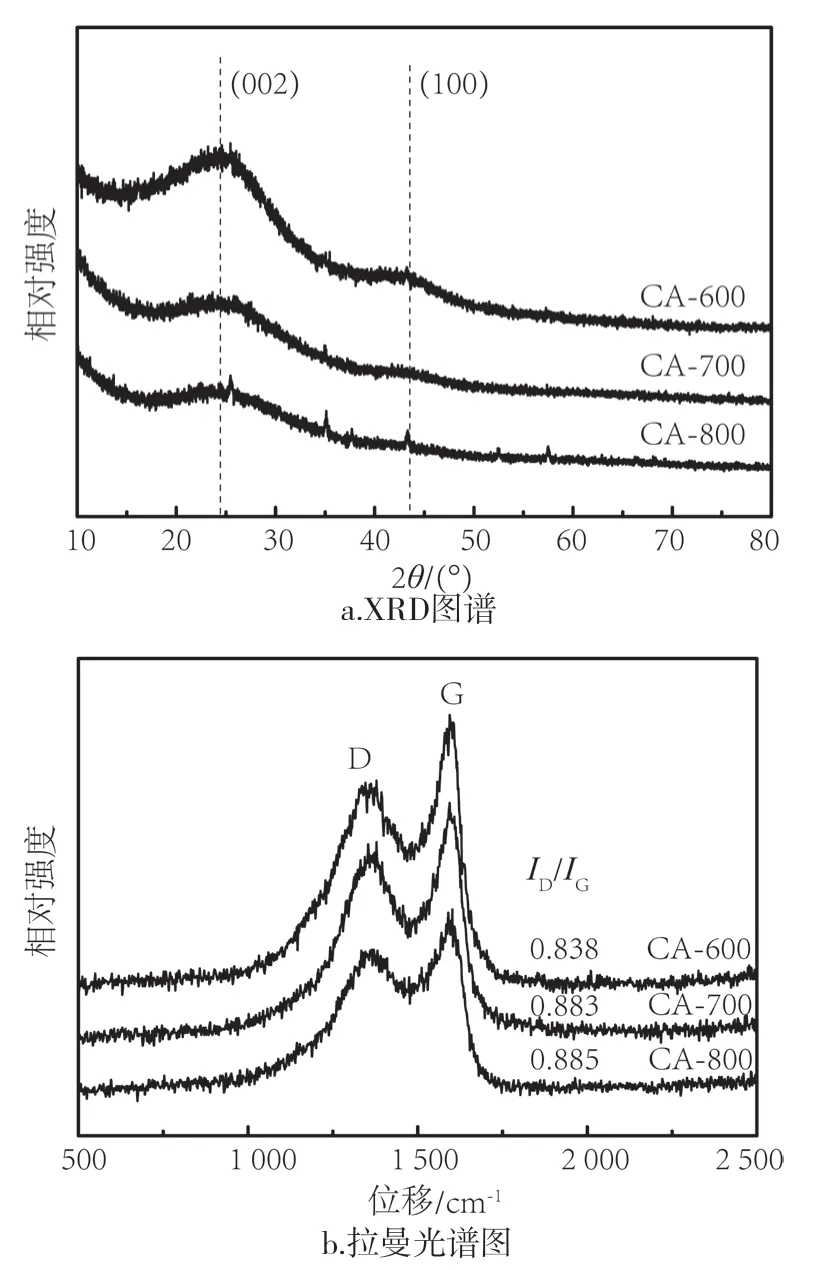
图2 样品的XRD图谱和拉曼光谱图 Fig.2 XRD and Raman spectra of the sample
由表1 可知,样品的氮含量随活化温度升高而下降,说明氮元素不稳定,在活化过程中易被氧化而挥发掉。为进一步研究样品中氮元素的存在状态,对样品进行了XPS测试,如图3 所示。所有样品的氮元素均以吡啶型氮、吡咯型氮和吡啶型氮氧化物的形式存在,且吡咯型氮的含量最高,而吡咯型氮已被证实是最有利于CO2吸附的氮存在形式[16-18],因此这一结果对于CO2吸附是有利的。所有结果表明,活化条件对碳材料中氮的含量和存在形式影响很大。
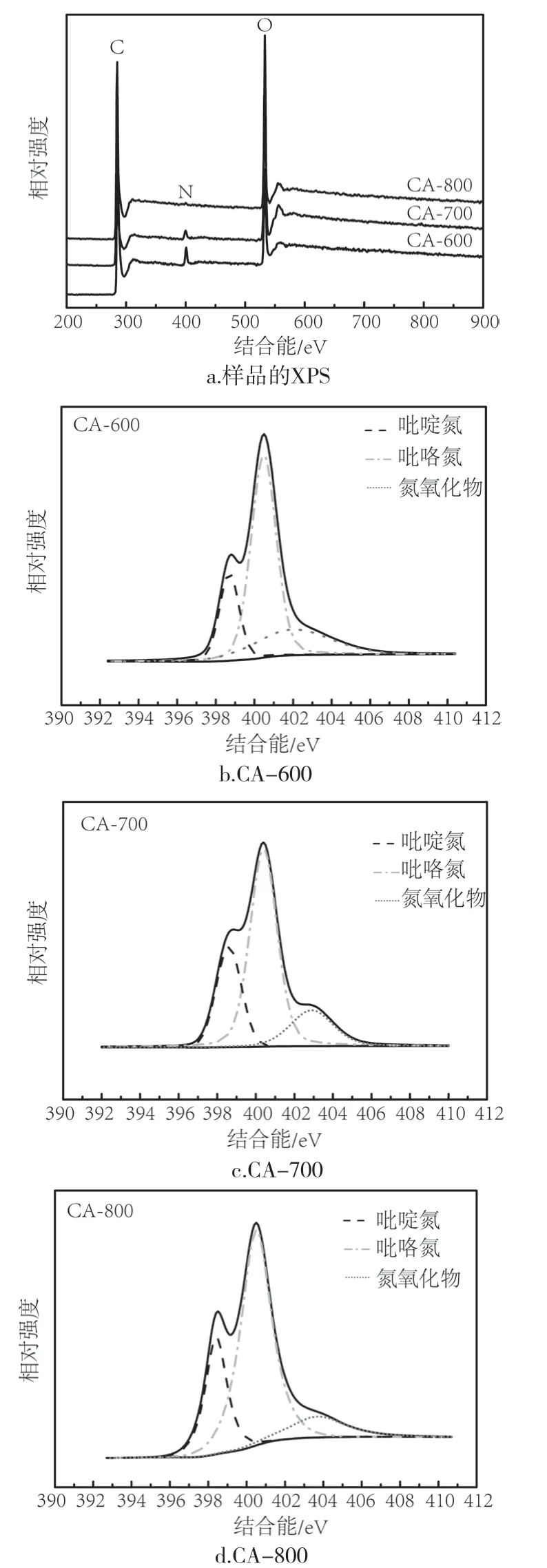
图3 相对强度与结合能的关系 Fig.3 Relationship between relative strength and binding energy
2.2 CO2 吸附性能分析
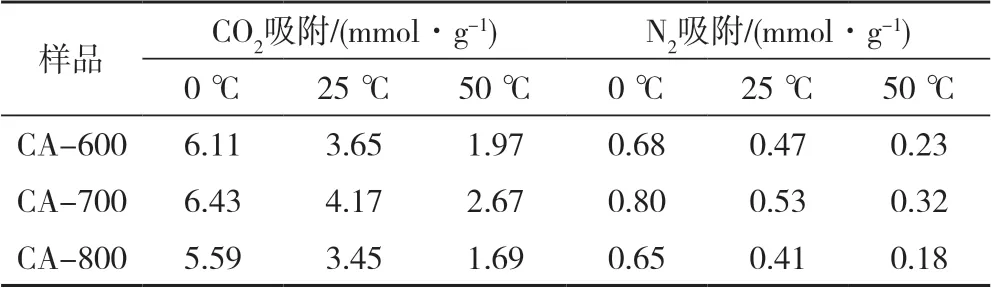
表2 样品在不同温度下的CO2 和N2 吸附性能Tab.2 CO2 and N2 adsorption properties of samples at different temperatures


图4 0、25 ℃和50 ℃下样品的CO2和N2吸附-脱附曲线Fig.4 Adsorption desorption curves of CO2 and N2 at 0,25,50 ℃
表2 列出了样品在不同温度下的CO2吸附性能,可以发现:样品对CO2的吸附性能都是随着温度的升高而减弱,且图4 中CO2的吸附与脱附曲线基本重合,没有回滞环出现,说明样品对CO2的吸附是物理吸附,而非化学吸附,也就是说所有样品可通过简单的抽真空方式脱附气体而实现再生,这对工业化应用是有利的[19]。在所有样品中,CA-700 的CO2吸附性能最好,在0℃时的CO2吸附量为6.43 mmol/g,在25 ℃时为4.17 mmol/g,在50 ℃时仍有2.67 mmol/g的吸附量,远高于商业活性炭在25 ℃下0.89 mmol/g的吸附量[20]。其他碳材料,如Tian等[21]以真菌为前驱体制备的生物质多孔碳材料在25 ℃下的CO2吸附量为3.5 mmol/g;Han等[22]制备的IRMOF-3 在0 ℃和25 ℃下对CO2的吸附量分别为2.38 mmol/g和1.37 mmol/g;Patino等[23]制备的分子筛CReHy在0 ℃和25 ℃下对CO2的吸附量分别为3.70 mmol/g和2.70 mmol/g。这些结果证明:该试验合成的多孔碳对CO2的吸附性能是显著的,是一类有前途的吸附剂。比较发现,样品对CO2的吸附性能与其比表面积、微孔体积及氮含量均不呈线性相关,说明微孔和氮掺杂同时对样品的CO2吸附性能起作用,即样品同时通过微孔填充和酸碱作用来吸附CO2。
对吸附剂来说,不仅需要具有高的CO2吸附量,还需具有优异的循环使用性能才能在工业中得到应用。样品的循环使用性能通过在25 ℃、CO2气氛下吸附和180 ℃、N2气氛中再生测试。如图5 所示,为样品CA-700 在25 ℃下的CO2吸附循环性测试图,经10 次循环后,CO2的吸附量基本不变,说明样品对CO2吸附具有稳定且优异的循环使用性能。

图5 CO2 吸附循环性测试 Fig.5 CO2 adsorption cycle test
等量吸附热(Q)可用于研究CO2与吸附剂表面的相互作用力大小,结合0、25 ℃和50 ℃下CO2的吸附等温线,利用Clausius-Clapeyron方程计算样品对CO2的等量吸附热。Clausius-Clapeyron方程表达式如下[23]:
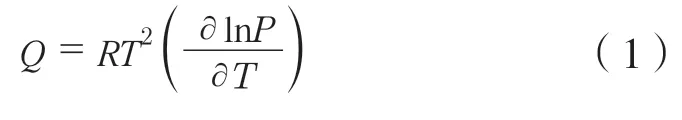
式中:Q ── 等量吸附热,kJ/mol;
T ── 所得吸附曲线的测试温度,K;
R── 理想气体常数,8.314 J/(K· mol);
P── 一定气体吸附量对应的压力,kPa。

图6 样品的CO2 吸附热和CO2/N2 (15 ∶85)选择性 Fig.6 Heat of CO2 adsorption and CO2 /N2 (15 ∶85) selectivity of the samples
计算所得的等量吸附热曲线如图6(a)所示,在CO2吸附起始阶段,样品对CO2的等量吸附热较高,随着CO2吸附量的增加,吸附热迅速降低,是因为含氮的高能吸附位点已逐渐被占据,剩下吸附势能低的吸附位,使得吸附热降低。对于纯碳材料,只能通过物理吸附作用吸附CO2,吸附剂表面与CO2分子间的相互作用力较弱,吸附热一般小于20 kJ/mol,而本文所有样品对CO2的吸附热均高于20 kJ/mol,说明样品与CO2分子之间的相互作用力较强,其中样品CA-600 对CO2的等量吸附热最高,为42.8 kJ/mol,CA-700 次之,为39.2 kJ/mol,CA-800 最弱,为35.4 kJ/mol,与样品的氮含量变化趋势一致,说明氮掺杂可以通过酸碱相互作用力有效促进吸附剂对CO2的吸附作用。
2.3 CO2/N2 分离性能分析
从实际应用角度出发,烟道气中CO2的含量仅占15%左右,其余主要是N2,因此吸附剂除具有较高的CO2吸附量之外,还需具有优异的CO2吸附选择性能。比较图4 和表2 可发现,样品对CO2和N2的吸附性能相差明显,例如CA-700 在25 ℃下对N2的吸附量仅有0.53 mmol/g,约为相同条件下对CO2吸附量的1/8,说明样品可有效分离CO2/N2混合气。Myers和Prausnitz提出的理想吸附溶液理论(IAST)已被广泛用于预测多孔材料对混合气体的分离性能,因此可根据这种方法计算样品对CO2/N2(15∶85)混合气的选择性。首先,利用Langmuir-Freundlich模型拟合样品对CO2和N2的吸附等温线,然后计算样品对CO2/N2的吸附选择性,吸附选择性(Sads)计算公式如下[20-23]:

qi为第i个样品的吸附量,mmol/g,pi为第i个样品的压力,kPa。
样品对CO2/N2(15 ∶85)的选择性计算结果如图6(b)所示,样品CA-600、CA-700 和CA-800 对CO2/N2(15 ∶85)的选择性分别为53、31 和20,与其他固体吸附剂相比,该配比是最佳的,如Ma等[24]用海藻酸钠制备的多孔碳在相同条件下对CO2/N2的选择性为29,Maroto-Valer等[25]制备的IRMOF-3 在相同条件下对CO2/N2的选择性仅为8.6。除此之外,可以发现本文制备的样品对CO2/N2的吸附选择性变化趋势与其氮含量的变化趋势一致,说明氮的掺杂不仅可以影响样品对CO2的等量吸附热,还能影响样品对CO2/N2的吸附选择性。
3 结论
以建筑废料废旧竹木为前驱体,KOH为活化剂,采用简单的碳化-活化法,成功制备了微孔为主的多孔碳。制得的多孔碳中,比表面积最高达1 789.5 cm2/g,由于微孔和氮掺杂的协同作用,样品拥有优越的CO2吸附性能,在0 ℃和25 ℃下的CO2吸附量最高分别为6.43 mmol/g和4.17 mmol/g。此外,样品的循环再生性能良好,对CO2的等量吸附热较高,对CO2/N2(15 ∶85)混合气的选择吸附性能突出,可用于烟道气中CO2的选择性吸附。

