一种简单、高效的二苄胺类化合物合成新途径
徐振华,蒋文佳,王硕文,刘 婷,曾政凯,唐 石
(吉首大学化学化工学院,湖南 吉首 416000)
二苄胺是常见的有机合成中间体[1],可用来合成青霉素和橡胶,塑料固化的熟化剂,还可用来生产高效无毒的硫化促进剂二硫化四苄基秋兰姆(TBZTD)和二苄基二硫代氨基甲酸锌(ZBEC)[2]。另一方面,它的衍生物,包含这些化合物的药物组合物等,可用于提高某些血脂包括高密度脂蛋白-胆固醇的水平,降低某些其他的血脂如LDL-胆固醇和甘油三酯的水平,并因此用于治疗一些哺乳动物包括人的动脉粥样硬化和心血管疾病[3-4]。虽然二苄胺类衍生物在有机合成中间体及药物领域的应用较广泛,但是目前市场购买较为困难,种类较少,且价格昂贵[5]。值得一提的是,芳香醛类化合物广泛存在于植物中[6],且价廉易得,是合成染料、香料及药品的重要中间体[7],具有较高的工业应用价值。另外,芳香苄胺类化合物也是重要的有机原料,广泛应用于染料、医药、农用化学品、添加剂、表面活性剂、纺织助剂、螯合剂、聚合物、阻燃剂等领域[8-11]。醛与胺的还原缩合是化学选择性制备仲胺最便利的途径之一。基于以上背景,我们开展了在硼氢化钠存在下,芳香苄胺与一系列芳醛进行还原缩合反应制备二苄胺的研究。该方法操作简单,反应条件较为温和,具有良好的官能团容忍性,可高效合成一系列的二苄胺类衍生物。此外,我们还开展了二苄胺在氨基酸衍生物合成中的应用探索[12]。
1 仪器和试剂
仪器:ZF-1型三角紫外分析仪,AV ANCE 400MHz超导傅里叶数字化核磁共振仪,集热式恒温搅拌器,RE-52AA 型旋转蒸发仪(,XT5A 型显微熔点仪。
试剂:乙腈、无水乙醇(均需经过进一步干燥除水处理),溴乙酸乙酯、三乙胺、对甲氧基苯甲醛、对甲氧基苄胺、对氟苯甲醛、对氟苄胺、对三氟甲基苄胺、无水硫酸钠、硼氢化钠。
2 合成路线
图1是以芳香苄胺、醛为底物,胺醛缩合产物的合成路线。

图1 胺醛缩合产物的合成路线Fig. 1 Synthesis Route of Amine Aldehyde Condensation Products
图2是胺醛缩合产物与溴乙酸乙酯的反应路线。

图2 应用路线Fig. 2 Application route
3 实验过程
以产物3a为例。取一个干燥、洁净的250mL的圆底烧瓶,加入适当大小的磁力搅拌子,向其中加入0.76g(2倍化学计量)NaBH4和6mL无水乙醇。另取一个干燥的离心管,向其中加入1.38g(10mmol)对甲氧基苄胺、1.63g(1.2倍化学计量)对甲氧基苯甲醛和6mL无水乙醇,混合均匀,放置5min。将圆底烧瓶放在磁力搅拌器上,开动搅拌,逐滴加入混合液,滴加完毕搭好冷凝回流装置,于80℃过夜。反应完毕,加入适量蒸馏水,用乙酸乙酯萃取分液,上层进行干燥,抽滤,旋干得到产物,收率83%。
我们对产品进行了较为简单的应用研究。以产物3f为例,在一个干燥、洁净的250mL的Schlenk反应器中加入适当大小的搅拌磁子,盖上翻口塞子并密封好,充入 N2,取 3.44g(20 mmol)溴乙酸乙酯用注射器注入到反应器,再注入15 mL乙腈。将Schlenk反应器固定在磁力搅拌器上搅拌,冰浴条件下滴加24mmol胺醛缩合产物,待溶液浑浊后,撤去冰浴装置,置于常温下反应24h即可终止反应。将反应后的浑浊液抽滤,滤液先用5%的NaHCO3和NaCl混合溶液洗涤2次,再用去离子水洗涤1次,取有机层干燥、抽滤、旋干得到产物,收率86%。
4 产物的表征数据
产物3a~3f采用熔点测定、核磁共振氢谱和碳谱等手段进行了表征,核磁共振表征谱图详见本文的辅助材料。
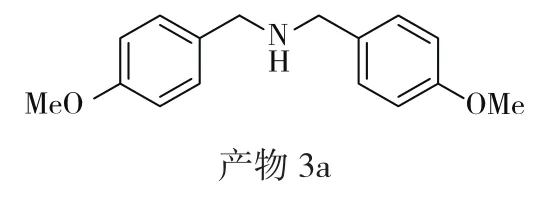
产物 3a:bis(4-methoxybenzyl)amine,黄色油状;产率 83%。1H NMR(400MHz,CDCl3):δ 7.20(d, J=8.6Hz,4H),6.84(d, J=8.6Hz, 4H),4.49(s, 1H),3.74(s, 6H),3.66(s, 4H)。HRMS m/z (ESI):calcd for C16H19NNaO2[M+Na]+280.1308,found:280.1304。
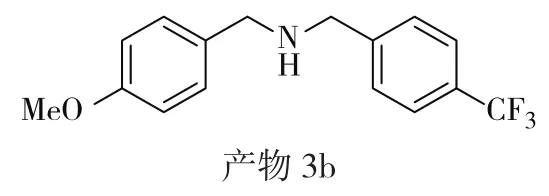
产 物 3b:N-(4-methoxybenzyl)-1-(4-(trifluoromethyl)phenyl)methanamine, 淡黄色油状,产率84%。1H NMR(400MHz, CDCl3):δ 7.57(d,J=8.2Hz, 2H),7.45(d,J=8.0Hz, 2H),7.25 (d,J=8.6Hz, 2H),6.87(d,J=8.6 Hz, 2H),3.84(s, 2H),3.79(s, 3H),3.73(s, 2H),1.80(s, 1H)。HRMS m/z (ESI):calcd for C16H16F3NNaO [M+Na]+318.1076,found:318.1073。
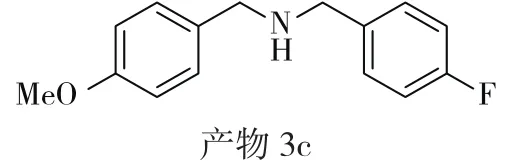
产物 3c:N-(4-fluorobenzyl)-1-(4-methoxyphenyl)methanamine,黄色油状,产率85%。1H NMR(400MHz,CDCl3):δ7.29(t,J=8.4 Hz, 2H),7.24(d,J=8.6Hz,2H),7.00(t, J=8.6 Hz, 2H),6.87(d, J=8.6 Hz, 2H),3.79(s,3H),3.73(d,J=9.4 Hz,4H),1.83 (s,1H)。HRMS m/z (ESI):calcd for C15H16FNNaO [M+Na]+268.1108,found:268.1105.
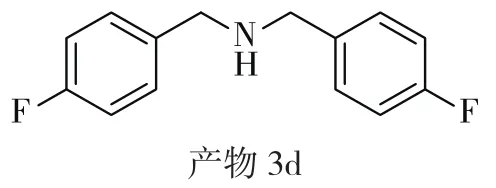
产物 3d:bis(4-fluorobenzyl)amine,淡黄色油状,产 率 80%。1H NMR(400 MHz, CDCl3):δ 7.29(t,J=8.8Hz, 4H),7.01(t,J =8.7Hz, 1H),3.75(s, 4H)。HRMS m/z (ESI):calcd for C14H13F2NNa [M+Na]+256.0908,found:256.0905.
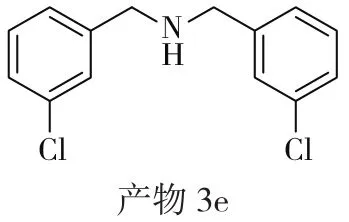
产物 3e:bis(4-chlorobenzyl)amine,黄色油状,产率 83%。1H NMR (400 MHz, CDCl3):δ 7.34(s, 2H),7.28~7.18 (m, 6H),3.76 (s, 4H)。HRMS m/z (ESI):calcd for C14H13Cl2NNa [M+Na]+288.0317,found:288.0315。
产 物 3f:ethyl N-(4-fluorobenzyl)-N-(4-methoxybenzyl)glycinate,黄色油状,产率81%。1H NMR(400MHz,CDCl3):δ 7.36~7.31(m, 2H),7.27(d,J=8.6 Hz, 2H),6.98(t, J=8.6Hz, 2H),6.85(d, J=8.6Hz, 2H),4.14(q,J=7.2 Hz, 2H),3.77(s, 3H),3.73(d, J=9.4Hz, 4H),3.24(s, 2H),1.25(t, J=7.2 Hz, 3H)。HRMS m/z (ESI):calcd for C19H22FNNaO3[M+Na]+ 354.1476,found:354.1472。

5 反应条件探索
为寻求最佳合成路线,提高产物收率,节约药品、试剂及溶剂,我们对二苄胺产物的制备进行了条件筛选。
5.1 胺醛还原缩合反应条件的优化
首先考察了反应底物的投料比(表1) 。以无水乙醇为溶剂,在80℃的反应温度下,等物质的量的芳香胺和芳香醛发生反应,得到了74%的产率。芳香醛提高为1.2当量时,产率达到83%;继续增加芳香醛至1.5当量,产物产率没有提升,说明再增加芳香醛的当量对提高产率无意义。当芳香胺为1.2当量时,得到75%的产率。探索溶剂对该反应的影响,结果表明以四氢呋喃作溶剂,产率高达75%;以乙腈、二氯甲烷为溶剂,均可以得到良好的产率。
在确定最佳投料比和溶剂的情况下,考察了反应时间和温度对产率的影响。在投料比1.2∶1、溶剂为无水乙醇的条件下,逐步提高反应温度,产率并没有明显的提高。但温度降低,反应产率下降到68%。反应时间缩短,产率明显下降,存在原料剩余;反应时间延长,产率并没有明显变化。因此确定该反应的最佳条件为:以无水乙醇为溶剂,芳香胺与芳香醛的物质的量比1∶1.2,在80℃条件下反应10h。

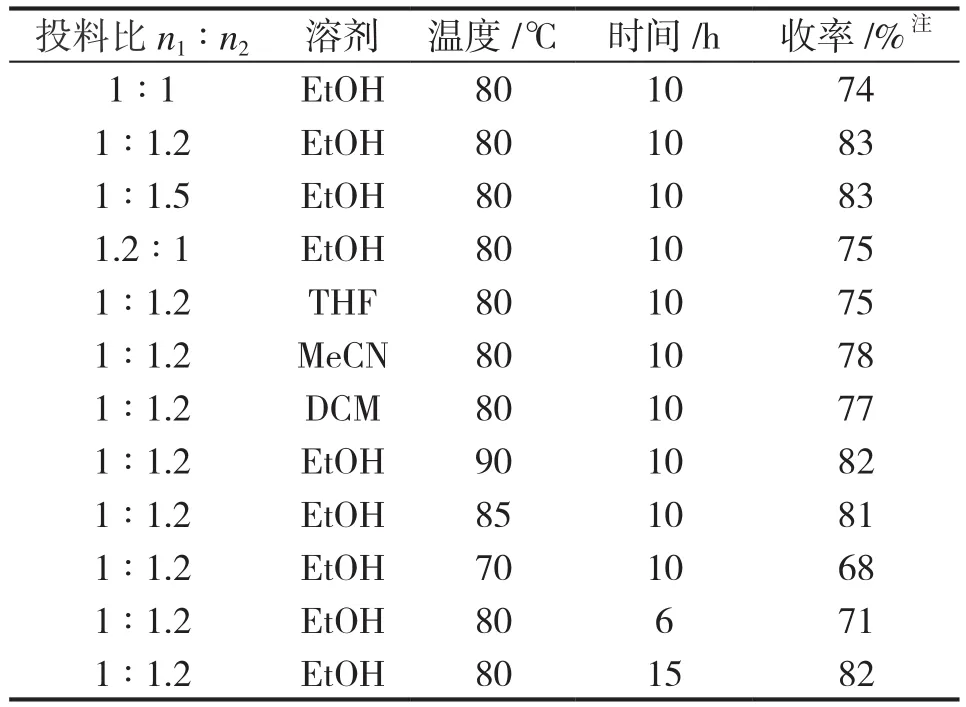
表1 产物合成的条件优化Table 1 Condition Optimization of Product Synthesis
得到最佳反应条件后,考察了反应底物的适用范围(图2)。我们考察了不同的取代基对反应的影响,发现都具有较好的兼容性。芳环上被4-MeO、4-F、4-CF3等取代的苄胺和醛均可发生该反应,与优化条件是兼容的,且能以较高的产率得到相应的产物a~d。值得一提的是,被3-Cl取代的也是可行的底物,并以83%的产率得到产物e。

图2 胺醛缩合底物范围Fig.2 Amino aldol condensation substrate scope
5.2 二苄胺类化合物与烷基溴缩合反应条件优化
考察了反应底物的物质的量比 (表2)。以乙腈为溶剂,等物质的量的溴乙酸乙酯与缩合产物3c反应,得到了74%的产率。溴乙酸乙酯提高为1.5 当量时,产率有了提高;增加缩合产物的当量时,产率有了些许提高;继续增加缩合产物的当量,产物产率没有明显变化,说明再增加胺醛缩合产物的当量对提高产率无意义。
考察溶剂对该反应的影响,结果表明,以乙腈作溶剂,产率高达86%;以四氢呋喃、二氯甲烷、二氧六环为溶剂,均可以得到良好的产率。因此确定该反应的最佳条件为:以乙腈为溶剂,溴乙酸乙酯与缩合产物的物质的量比1∶1.2,在室温条件下反应24h。

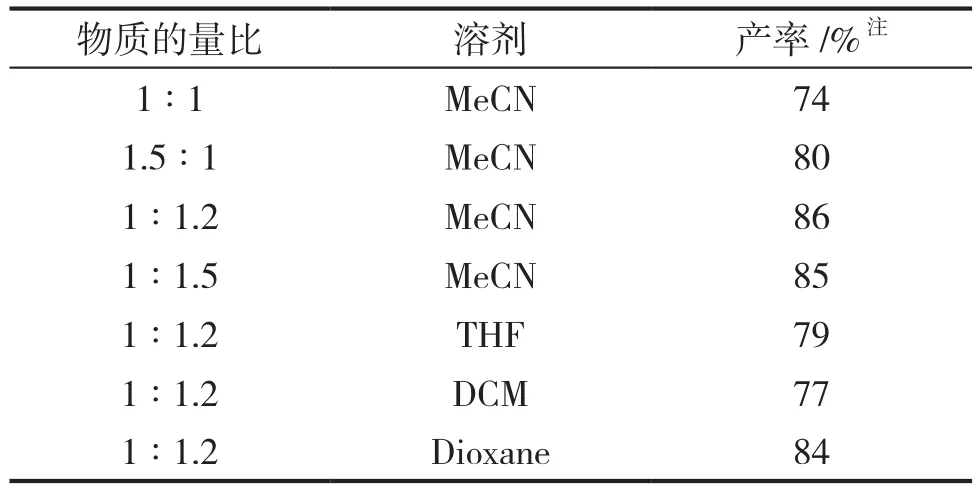
表2 应用反应的条件优化Table 2 Optimization of application reaction conditions
6 结论
本研究建立了一种简单、高效的芳香胺与芳香醛的缩合反应方法,并对温度、溶剂、时间、醛的用量等条件进行了筛选。以无水乙醇为溶剂,芳香胺与芳香醛的物质的量比1∶1.2,80℃条件下反应10h,可以较高的产率得到一系列相应的化合物。此方法为二苄胺类化合物的合成提供了新思路,大大拓宽了二苄胺类化合物的种类。开展了下一步的应用研究,以乙腈为溶剂,溴乙酸乙酯与缩合产物的物质的量比1∶1.2,室温条件下反应24h,可生成氨基酸衍生物含有多种官能团的二苄基甘氨酸乙酯,具有较大的应用价值。

