哈尔滨地区小天蓝绣球白粉病病原菌鉴定
司修洋 张鹏 刘齐月

摘要 小天蓝绣球Phlox drummondii Hook.,又名雁来红、金山海棠、福禄考,是一种极具观赏性的一年生草本植物,在我国北方被用来城市绿化。在小天蓝绣球的生长过程中,白粉病已成为其所患病害中发生最为严重的一种,给小天蓝绣球产业造成了巨大的损失,也使其丧失了美化城市的功能。本研究以東北农业大学园艺实验站的小天蓝绣球病叶为材料,对其病原菌进行形态学和分子生物学鉴定,明确其分类地位,为小天蓝绣球白粉病的科学防治提供依据。结果表明:小天蓝绣球白粉病菌主要侵染叶片,叶片正面布满白色粉层,后期叶片上产生黑褐色的小点,即闭囊壳。闭囊壳直径80~160 μm,附属丝菌丝状,长度30~210 μm,子囊多个,一个子囊内含有子囊孢子2~8个,分生孢子为粉孢子。对病原菌的ITS序列进行PCR扩增,得到561 bp的序列(GenBank登录号:MN209867),在GenBank上进行BLAST比对,确定此病菌为Golovinomyces magnicellulatus。
关键词 小天蓝绣球; 白粉病; 形态学特征; 分子鉴定
中图分类号: S 436.8
文献标识码: A
DOI: 10.16688/j.zwbh.2019396
Abstract Phlox drummondii Hook., also known as Yanlaihong, Jinshanhaitang and phlox, is an annual herbaceous plant used for urban landscaping in the north of China. Powdery mildew has become the most serious disease during the growth of P.drummondii, which could cause huge losses and affect its function. In this study, the pathogen of powdery mildew was identified with the method of morphological and molecular identification, which could provide a basis for the scientific control of this disease. The results indicated that the pathogen mainly infected leaves, and the whole leaf was covered with a white powder layer, then abundant dark brown cleistothecia were formed on the leaf. The diameter of cleistothecia was 80-160 μm, the appendages were mycelioid, with a length of 30-210 μm. One ascus contained 2 to 8 ascospores, and the conidium was oidium. The complete internal transcribed spacer (ITS) region of rDNA of the fungus was amplified and sequenced, and the 561 bp sequence was registered in GenBank (accession no. MN209867). BLAST analysis showed that the rDNA ITS sequence had 99% similarity with that of Golovinomyces magnicellulatus.
Key words Phlox drummondii; powdery mildew; morphological characteristics; molecular identification
小天蓝绣球Phlox drummondii Hook.是花荵科Polemoniaceae,天蓝绣球属Phlox一年生草本植物,原产墨西哥[1],是一种极具观赏性的花卉,具有花期长,花色艳丽且耐寒耐旱的特点,非常适合在干旱少雨的地方种植。因此,已成为我国北方城市园林绿化的优良地被植物[2]。
近年来,新疆地区的小天蓝绣球在生育期频频发生白粉病,国庆节未到就过早染病枯萎,丧失了美化城市的功能,因此,城市园林绿化管理者只能采用矮牵牛代替小天蓝绣球的办法[3]。2017年-2018年,小天蓝绣球白粉病在哈尔滨地区发病率高达90%,且危害严重。本研究通过病原菌形态和ITS序列分析明确了该病原菌的分类地位,为小天蓝绣球白粉病的防治提供依据。
1 材料与方法
1.1 试验材料
试验样本于2018年9月采自哈尔滨市香坊区东北农业大学园艺实验站,现保存于东北农业大学农学院植物病理教研室。
1.2 病害症状观察
对小天蓝绣球白粉病症状进行仔细观察,包括发病部位、病斑颜色、大小和危害程度等[4]。
1.3 病原菌形态学观察
取干净的载玻片滴一滴无菌水于载玻片中心。选取发病症状典型的小天蓝绣球病叶,用无菌针挑取病叶的白粉层和闭囊壳于无菌水中轻微晃动,使其分散,用镊子夹取盖玻片,从一侧轻轻放下,避免出现气泡。将玻片放于显微镜下观察病原菌的分生孢子、闭囊壳、子囊和子囊孢子的形态,并测量相关数据。
1.4 病原菌rDNA ITS片段的PCR扩增和序列测定
白粉菌采用软毛笔刷取法收集[5]。轻轻地将病叶表面的白粉菌刷至硫酸纸上,收集于无菌离心管中。采用CTAB法[6]提取病原菌基因组DNA。利用真菌通用引物ITS1和ITS4进行PCR扩增(ITS1:5′-TCCGTAGGTGAACCTGCGG-3′;ITS4:5′-TCCTCCGCTTATTGATATGC-3′)。PCR反應体系为25 μL,包括DNA模板1 μL,引物ITS1和ITS4(10 μmol/L)各1 μL,Taq-Plus PCR Forest Mix 48 μL,ddH2O 17.2 μL。PCR扩增程序:94℃预变性3 min;94℃变性1 min,56℃退火1 min,72℃延伸50 s,32个循环;72℃延伸10 min。PCR扩增产物在1%琼脂糖凝胶上进行检测,产物送往吉林省库美生物科技有限公司进行测序,然后在GenBank上进行BLAST同源性比对。
2 结果与分析
2.1 小天蓝绣球白粉病的症状
小天蓝绣球白粉病主要危害叶片,叶的正面、背面均可受害。发病初期叶片上产生放射状圆形小斑,然后病斑逐渐扩大,并且连成一片,很快整个叶片上布满了白色粉状物(图1),即病原菌的分生孢子,后期白色粉层上产生了深黄色或黑褐色的小颗粒(图2),即病原菌的闭囊壳。
2.2 病原菌形态特征观察
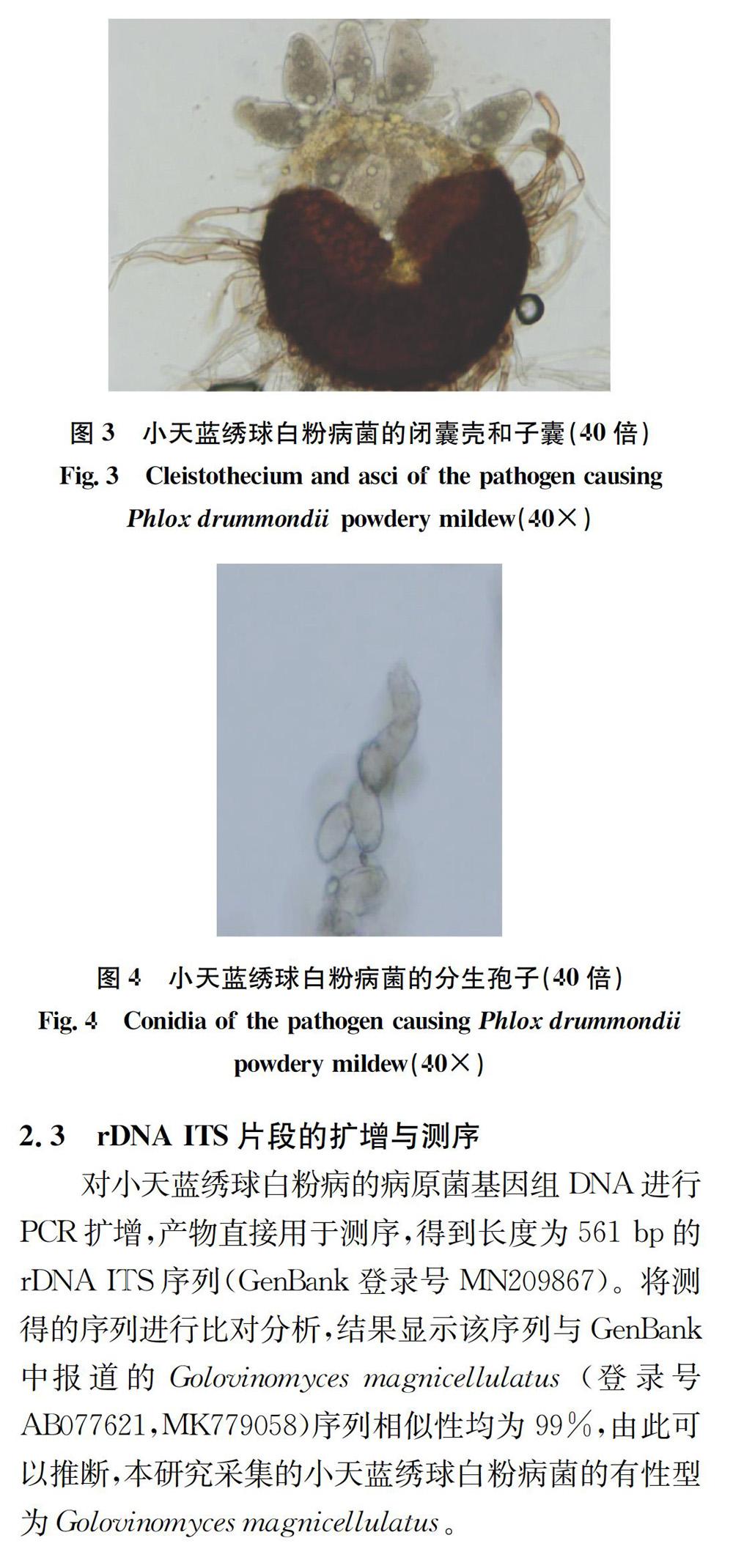
闭囊壳球形,直径80~160 μm,闭囊壳内子囊多个,椭圆形,(50~70)μm×(25~50)μm,1个子囊内通常含有2~8个子囊孢子,子囊孢子圆形或椭圆形。附属丝菌丝状,大多弯曲,少数直立,顶端不分支,长度30~210 μm(图3)。分生孢子为粉孢子,圆形或椭圆形(图4)。
2.3 rDNA ITS片段的扩增与测序
对小天蓝绣球白粉病的病原菌基因组DNA进行PCR扩增,产物直接用于测序,得到长度为561 bp的rDNA ITS序列(GenBank登录号MN209867)。将测得的序列进行比对分析,结果显示该序列与GenBank中报道的Golovinomyces magnicellulatus (登录号AB077621,MK779058)序列相似性均为99%,由此可以推断,本研究采集的小天蓝绣球白粉病菌的有性型为Golovinomyces magnicellulatus。
3 结论与讨论
本研究通过形态学鉴定和ITS序列比对分析,证实引起哈尔滨地区小天蓝绣球白粉病的病原菌为Golovinomyces magnicellulatus。该种为2013年的中国新记录种,在辽宁省首先被发现并鉴定,寄主植物是酸浆Physalis alkengi var.franchetii[7]。G.magnicellulatus不仅侵染小天蓝绣球,在韩国、意大利还侵染同属的天蓝绣球P.paniculata引起白粉病[8-9]。
国内关于小天蓝绣球白粉病病原菌的报道很少。贾菊生等[3]根据病原菌的形态特征,将其有性世代定为福禄考二孢白粉菌Erysiphe cichoracearum DC.f.phlogis Jacz,但未进行相关的分子鉴定。因此,对于不同地域来源的小天蓝绣球白粉病样本,是否存在不同病原菌侵染引起同一种白粉病还有待于进一步研究确认。除新疆地区报道了小天蓝绣球白粉病外,其他地区还没有该病害的报道,这也表明该病害还没有引起人们的足够重视。本研究从形态学和ITS序列两个方面明确了G.magnicellulatus是小天蓝绣球白粉病的病原菌,为病害的防控提供了依据。
参考文献
[1] 方瑞征, 黄素华.中国植物志·第六十四卷第一分册[M].北京: 科学出版社, 1979.
[2] 杨玉想, 刘金涛, 张娟, 等. 北方地区福禄考的栽培管理[J]. 南方农业, 2010, 4(12): 68-69.
[3] 贾菊生, 聂述先.诱发新疆福禄考早期衰败的原因——白粉病[J]. 新疆农业科学, 2000(3): 126-127.
[4] 迟梦宇, 钱恒伟, 赵颖, 等. 刺槐白粉病病原菌鉴定[J]. 植物病理学报, 2016, 46(5): 707-709.
[5] 万三连, 梁鹏, 宋风雅,等. 橡胶树白粉菌收集及DNA和RNA提取方法比较[J]. 广东农业科学, 2013(11): 134-139.
[6] 王文静, 李成伟. 番茄白粉菌的PCR分子检测[J]. 河南农业科学, 2010(5): 72-75.
[7] LIANG C, XING H H, LIU Z, et al. First report of powdery mildew caused by Golovinomyces magnicellulatus var. magnicellulatus on Physalis alkekengi var. franchetii in China [J]. Plant Disease, 2013, 97(10): 1382.
[8] PARK M J, PARK J H, LEE S G, et al. First confirmed report on powdery mildew of Phlox paniculata caused by Golovinomyces magnicellulatus in Korea [J]. The Plant Pathology Journal, 2010, 26(3): 295.
[9] GARIBALDI A, BERTETTI D, FRANCO S, et al. Powdery mildew caused by Golovinomyces magnicellulatus on Phlox paniculata in Italy[J]. Journal of Plant Pathology,2016, 98(1): 176.
(责任编辑:杨明丽)

