深部煤矿降温系统管道腐蚀机理
刘星星,韩巧云,张毅,邹声华
(湖南科技大学 土木工程学院,湖南 湘潭 411201)
煤炭是中国的主要能源.现今煤矿生产处于深部开采阶段,工作面温度可达30~40 ℃[1].高温环境对于井下的生产安全、工人的身体健康及生产效率[2]均有着不利的影响.然而传统的非人工制冷降温措施已不能解决深井的高温热害问题,人工制冷降温技术应运而生[1,3].HEMS系统是以矿井水为冷源的热能转换系统,在江苏、湖南等地的高温矿井得到了成功应用:巷道空气温度降低了5~7 ℃,相对湿度降低了5%~15%[1,3].图1为该系统的技术原理图.

图1 HEMS降温系统技术原理
矿井水具有高硬度、高矿化度、弱碱性等特性[4].系统在现场运行了一段时间后,发现系统管道腐蚀较为严重,如图2所示,大大地降低了系统的稳定性及传热效率[5],威胁着井下的降温安全.因此,研究矿井水中的离子对铁质管道壁面的腐蚀的影响,对于深部煤矿降温系统管道的腐蚀机制研究以及采取相应的防腐措施均具有理论指导意义.许多专家针对地热水管道腐蚀过程进行了研究[6-11].

图2 HEMS降温系统的腐蚀现状
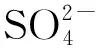
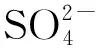
1 化学模型的建立
1.1 腐蚀产物的微观结构
利用X光衍射和扫描电子显微镜(SEM)分析了张双楼煤矿降温系统中的管道沉积物.结果表明,腐蚀产物主要为Fe2O3和Fe3O4,如图3所示,铁氧化物的比例约为17%~20%,其微观形态表现为直线带状或立方体(图3).

图3 腐蚀产物的微观结构及成分
1.2 降温系统管道水化学特性


表1 张双楼煤矿降温系统管道水的离子成分及含量
1.3 化学模型
图4为深井降温系统管道电化学腐蚀过程.电化学反应的阳极反应是从管道中释放的铁离子与水反应形成氢氧化亚铁,O2见式(1)和式(2).电化学反应的阴极反应是溶解在矿井水中的氧气捕获阳极反应释放的电子转化为OH-,见式(3).

图4 深部煤矿降温系统管道电化学腐蚀过程
Fe→Fe2++2e;
(1)
Fe2++2H2O→Fe(OH)2+2H+;
(2)
O2+2H2O+4e→4OH-.
(3)
2 第一性原理计算模型及方法
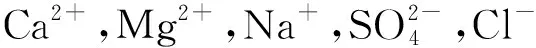
吸附能计算公式[42-44]为
Ead=Eion+H2O/Fe(001)-EH2O-Eion/Fe(001).
(4)
式中:EH2O,Eion/Fe(001)和Eion+H2O/Fe(001)分别为H2O、离子在Fe(001)面吸附体系、离子和H2O在Fe(001)面共吸附体系的能量.
图6、图8和图10中的小图表征的为吸附体系的三维电荷差分密度(3D-CDD),用于直观地描述吸附体系电荷再分配.蓝色部分代表电荷分布的减小(△ρ<0),黄色部分代表区域电荷分布的增加(△ρ>0).计算公式如式(5)所示:
(5)

3 结果和讨论
3.1 单个H2O分子在Fe(001)面的吸附
对单个H2O分子在Fe(001)表面的吸附计算过程中,本文考虑了H2O以水平、竖直向上、竖直向下3种姿态在Fe(001)表面的吸附,主要吸附位置为Fe(001)表面的3个高对称位,Bridge(B),Hollow(H)及Top(T),共计吸附位形为60种.计算结果表明,在Fe(001)表面的top-x位,总存在稳定的吸附态,H2O的分子平面接近平行于金属表面.这些分子吸附态的位形结构和相应参数分别见图5(图中按球体直径从大到小的顺序依次代表铁、氧和氢原子)和表2.在图5中我们定义了两个角度φ和θ,其中φ表示水分子H-O-H的夹角,θ表示水分子相对于Fe(001)表面的倾斜角.弛豫后吸附体系的功函数为4.09 eV,小于清洁铁表面的功函数(4.48 eV),这说明被吸附的H2O和Fe(001)表面有较明显的电荷重新分布.
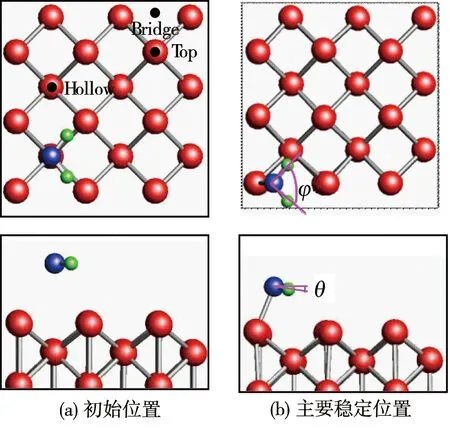
图5 单个H2O在Fe(001)上吸附时最稳定位置的俯视图和侧视图
图6为最稳定吸附态的H2O吸附于Fe(001)面时吸附态水分子、Fe(001)表面原子的分波态密度,其中大图为H2O分子和Fe(001)表面原子的PDOS图,小图为H2O在Fe(001)表面吸附的差分电荷密度,费米能设为零.为了比较,自由H2O分子、清洁表面Fe原子的分波态密度也进行了整理.单个H2O在Fe(001)表面吸附时,弛豫后,吸附体系中水分子的3σ,4σ,5σ和1π分子轨道的能级相对于费米面分别下降了3.25,2.72,4.5和4.5 eV,分子轨道3σ和4σ明显变窄.对Fe而言,H2O分子在其表面的吸附主要是通过3σ,5σ轨道和表面原子的d态相互作用.3D-CDD图表征了水和铁之间存在着明显的电荷积累.

图6 H2O分子和Fe(001)表面原子的PDOS与差分电荷密度图
3.2 离子对铁腐蚀影响机制的第一性原理研究
3.2.1 Ca2+,Mg2+,Na+和H2O在Fe(001)上的共吸附
初始时刻,将H2O置于T位,以平行的姿态置于Fe(001)面上方,离子(Ca2+,Mg2+,Na+)精确地放在3个高对称位上.弛豫后,θ显著增加,Ca2+(Mg2+或Na+)从初始T,B或H位迁移到相邻的H位,Ca2+(Na+)和H2O之间明显成键.
共吸附体系的结构参数及吸附能如表2所示.共吸附体系吸附能远大于单个水分子在Fe(001)面的吸附能,与此同时,φ和θ明显增大.以上差异均表明,Ca2+,Mg2+,Na+对于H2O与Fe(001)的相互作用有明显的促进作用,最稳定的吸附位置为Ca2+,Mg2+,Na+在H位,H2O在T位,如图7所示(图中按球体直径从大到小的顺序依次代表分别代表Ca,Mg,Na,Fe,O,H原子).

图7 共吸附体系最稳定位置的俯视图和侧视图
为了更进一步了解离子的加入对水分子在Fe(001)面的化学吸附态的本质特点,我们计算得到了最稳定吸附态的离子和H2O共吸附于Fe(001)面时吸附态水分子、Fe(001)表面原子与被吸附离子的分波态密度(图8),其中大图为H2O分子和Fe+离子(Ca2+/Mg2+/Na+)的PDOS图,小图为H2O在Fe(001)表面吸附的差分电荷密度,费米能设为零.为了比较,自由H2O分子、清洁表面Fe原子、单个水分子在Fe(001)表面吸附时H2O分子和表面Fe原子的PDOS也显示在图8中.
Ca2++H2O/Fe(001)的共吸附体系中:共吸附体系中水分子的3σ,4σ,5σ,1π和2π轨道能级相对于费米面分别下降了0.75,12.05,4,1.95,6.2 eV.同时从表面Fe原子与Ca2+的PDOS之和来看,吸附H2O分子后明显有新的s态峰值出现,特别是在对应2π,5σ分子轨道的区域,因此H2O分子在其表面的吸附主要是通过2π轨道、5σ和表面原子的s态相互作用,这说明,Ca2+对Fe(001)面H2O分子的吸附具有巨大的影响.通过差分电荷密度图(3D-CDD)来看,当H2O和Ca2+在Fe(001)面共吸附时,H2O分子和Ca2+之间、H2O分子和Fe(001)面之间、Fe(001)面和Ca2+之间均有明显的电荷积累.这说明,H2O分子与Ca2+在Fe(001)面共吸附时,Fe(001)面原子与H2O分子和Ca2+均发生反应,促进了表面腐蚀的产生.综上所述,Ca2+的加入对于铁质管道的腐蚀具有促进作用.
Mg2+H2O/Fe(001)的共吸附体系中:共吸附体系中水分子的4σ和5σ轨道向费米面能相对低的方向移动了0.05,0.75 eV,1π轨道向费米面能相对高的方向移动了1.15 eV.同时从表面Fe原子与Mg2+的PDOS之和来看,吸附H2O分子后明显有s态和d态的变化,特别是在对应1π,5σ,2π分子轨道的区域,因此H2O分子在其表面的吸附主要是通过1π轨道、5σ和表面原子的s态相互作用,2π分子轨道与表面原子的d态发生作用.通过差分电荷密度图(3D-CDD)来看,当H2O和Mg2+在Fe(001)面共吸附时,H2O分子和Fe(001)面之间有明显的电荷积累.这说明,H2O分子与Mg2+在Fe(001)面共吸附时,Fe(001)面原子与H2O分子反应加强,促进了表面腐蚀的产生.综上所述,Mg2+的加入对于铁质管道的腐蚀具有促进作用.
Na++H2O/Fe(001)的共吸附体系中:共吸附体系中水分子的4σ,5σ和1π轨道向费米面能相对低的方向移动了0.45,0.25,0.1 eV.同时从表面Fe原子与Na+的PDOS之和来看,吸附H2O分子后s态和d态发生明显变化,特别是在对应1π,5σ和2π分子轨道的区域,因此H2O分子在其表面的吸附主要是通过1π轨道、5σ和表面原子的s态相互作用以及2π分子轨道和表面原子的d态相互作用.通过差分电荷密度图(3D-CDD)来看,当H2O和Na+在Fe(001)面共吸附时,H2O分子和Na+之间、H2O分子和Fe(001)面之间、Fe(001)面和Na+之间均有明显的电荷积累.这说明,H2O分子与Na+在Fe(001)面共吸附时,Fe(001)面原子与H2O分子和Na+均发生反应,促进了表面腐蚀的产生.综上所述,Na+的加入对于铁质管道的腐蚀具有促进作用.

图8 H2O分子和Fe+离子(Ca2+/Mg2+/Na+)PDOS与差分电荷密度
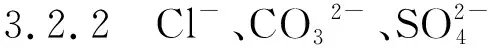

图9 Cl-+H2O/Fe(001)、CO32-+H2O/Fe(001)和共吸附系统最稳定吸附位置的俯视图和侧视图
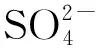
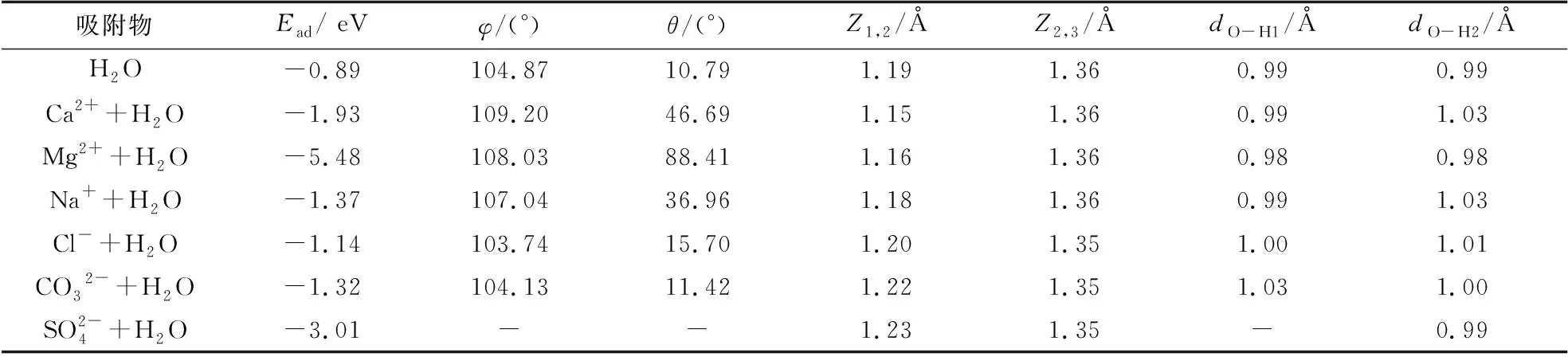
表2 离子+H2O共吸附体系的结构参数、吸附能
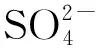

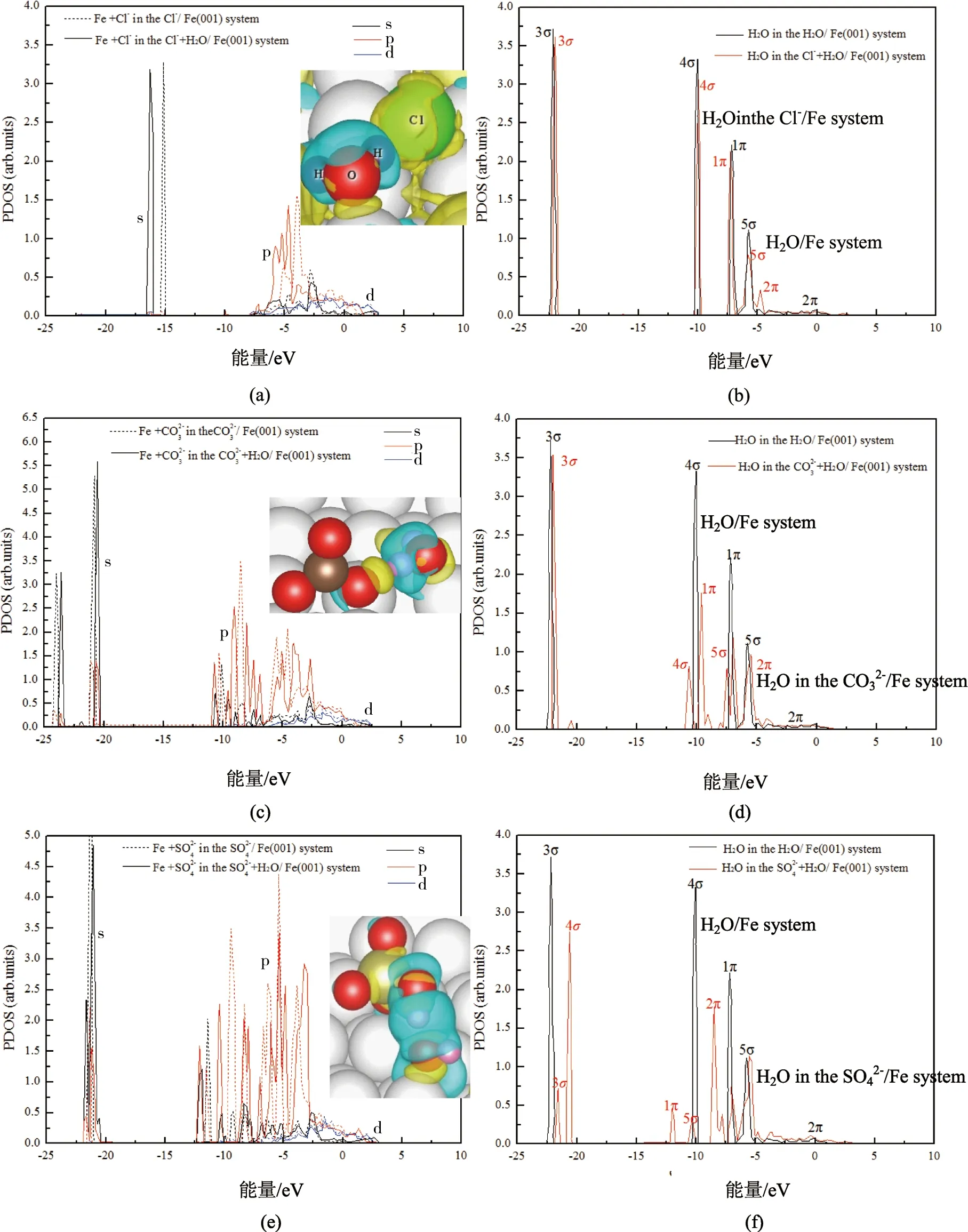
图10 H2O分子和Fe+离子与差分电荷密度
4 结论
1)X-ray,SDM分析结果表明,深井降温系统管道内壁腐蚀物的主要成分为Fe的氧化物.
3)研究结果对于深部煤矿降温系统管道腐蚀机制的研究、防腐措施的研究、系统的优化及井下的生产安全均有着重要的意义.

