Fe3O4@SBc复合材料对甲基橙的吸附去除效果
王向辉,胡可昕,宫旖柔,杨 雪,王 闯,李文丽,符美丽,刘艳玲,游诚航
(海南师范大学化学与化工学院,海南省水环境治理与资源化重点实验室,海口市土壤污染修复与资源化重点实验室,海南海口571158)
随着社会发展和国民生活水平的逐步提高,我国污水处理量迅速攀升。截至2020年1月底,全国核发污水处理厂排污许可证10 113个。污水处理厂产能增加必然导致污水厂的剩余污泥量快速增长,预估2020年污水处理厂产生的剩余污泥(含水率80%以上)将达 6×107t〔1〕。 污泥主要由有机物和无机物组成,以有机成分为主(75%~85%),包括难降解的有机污染物、重金属和病原体、寄生虫等有毒有害物质,随意丢弃或处理不当会给环境和人类健康带来巨大危害〔2〕。
污水处理厂剩余污泥的有机物含量高、产量大,能作为优质的生物质材料制备生物炭,不仅可解决污泥去向问题,还能保证固炭环保〔3〕。已有文献报道污泥生物炭用于水环境污染治理〔4〕。但生物炭颗粒小、质轻,难以通过过滤和沉降的方式去除。将具有磁性的纳米粒子Fe3O4引入污泥生物炭中,制备Fe3O4@SBc复合材料,有利于形成丰富的叠层结构,增加污泥活性炭的比表面积,并在保留生物炭高吸附量的同时克服难以分离的缺点。此外,引入含氧官能团后污泥活性炭表面的活性位点增加,对于吸附有机染料更加有利〔5〕。
笔者采用某污水处理厂剩余污泥热解制备了污泥生物炭(SBc),经共沉淀法将纳米磁性粒子Fe3O4与SBc复合,成功制备了Fe3O4@SBc复合材料,通过甲基橙溶液吸附实验,分析溶液pH、吸附剂添加量、震荡吸附时间和甲基橙浓度等因素对去除效果的影响,并进行吸附动力学和等温吸附模型拟合,分析吸附机理,期望为污泥的资源化利用提供新途径。
1 实验方法
1.1 试剂及仪器
实验所用污泥由海口市白沙门污水处理厂提供;甲基橙,分析纯,上海麦克林生化科技有限公司;FeCl3·6H2O(分析纯)、FeCl2·7H2O(分析纯)、盐酸、氢氧化钠、氢氧化钾,广州化学试剂厂。
OTF1200X管式炉,合肥科晶材料技术有限公司;JSM-7401F扫描电镜,日本JEOL公司;6700红外光谱仪,美国Thermo公司;UItimaⅣX射线衍射仪,日本Rigaku公司;ASAP2460比表面积与孔隙度分析仪,美国MICROMERITICS公司;MPMS-XL-7超导量子磁强计,美国Quantum Design公司;Lambda 750s可见分光光度计,美国PE公司。
1.2 Fe3O4@SBc的制备
污泥生物炭制备:污泥去除大块杂质后自然晾干,粉碎过0.42 mm(60目)筛。取5.0 g污泥粉末、15.0 g KOH、25 mL去离子水置于100 mL玻璃烧杯中,搅拌均匀浸泡24 h,于80℃烘箱中干化24 h,干燥后将活化污泥粉末放入管式炉中,氮气流保护,升温速率设置10℃/min、热解温度设置300~700℃,热解时间270 min,热解结束后降温至室温,用去离子水和稀盐酸溶液交替洗涤样品至中性,真空70℃下干燥过夜,得到污泥生物炭SBc,保存在玻璃样品瓶中待用〔6〕。
Fe3O4@SBc制备:取300 mL去离子水置于三口烧瓶内,通氮气 30 min,量取 2.307 4 g FeSO4·7H2O和4.490 3 g FeCl3·6H2O置于反应瓶中,室温下机械搅拌20 min,溶液呈橙红色;称取SBc缓慢加入上述混合液中,充分搅拌3 h;向反应瓶滴加浓氨水,调节pH至10~11,反应液中有黑色沉淀生成,升温至60℃继续反应4 h;黑色沉淀经磁性分离后,用去离子水、无水乙醇交替洗涤3次,60℃真空干燥20 h,得到污泥生物炭复合材料 Fe3O4@SBc〔6〕。
1.3 Fe3O4@SBc复合材料的表征
采用扫描电镜(SEM)分析材料的外观形貌;用红外光谱仪(FT-IR)分析其材料表面官能团种类;用X射线衍射仪(XRD)分析材料晶体类型和结构;用N2吸附比表面积孔径分布仪(BET)分析材料的孔径分布和比表面积;用超导量子磁强计测定复合材料的磁强度;用可见分光光度计测定溶液中的甲基橙浓度。
1.4 吸附实验
在棕色容量瓶中配制质量浓度为1 000 mg/L的甲基橙溶液,待用。
甲基橙吸附实验:将甲基橙溶液稀释至100 mg/L,准确量取25 mL稀释液置于50 mL三角瓶中,加入20 mg污泥生物炭SBc或复合材料Fe3O4@SBc,恒温震荡240 min,经0.22μm滤膜过滤,稀释10倍后用分光光度计在464 nm处测定滤液吸光度,计算滤液中的甲基橙浓度〔6〕。
pH影响实验:量取25 mL质量浓度为100 mg/L的甲基橙溶液,用稀氢氧化钠溶液(1 mol/L)或稀盐酸溶液(1 mol/L)调节pH,吸附实验同上。
吸附剂投加量影响实验:量取25 mL质量浓度为100 mg/L的甲基橙溶液,分别加入不同质量的吸附剂进行实验,其余吸附条件同上。
通过吸附量(qe)和去除率(E)衡量吸附效果。
1.5 吸附动力学实验
取25 mL质量浓度为100 mg/L的甲基橙溶液,加入20 mg Fe3O4@SBc复合材料,间隔一段时间取样测定溶液中的甲基橙浓度,用拟一级、二级吸附动力学模型分析吸附过程。
1.6 吸附等温线实验
量取一系列质量浓度为10~200 mg/L的甲基橙溶液各25 mL,加入20 mg Fe3O4@SBc,震荡吸附240 min后测定溶液中的甲基橙浓度,用Langmuir、Freundlich吸附等温线模型进行拟合。
1.7 循环性能测试
水洗活化:吸附实验结束后过滤吸附剂,微波洗涤3次,每次1 h,真空干燥,重复5次实验。
热解活化:吸附实验结束后干燥,600℃热解270 min活化,用于下次吸附实验,重复5次吸附活化实验。
2 结果与讨论
2.1 制备条件分析
在污泥生物炭制备过程中,热解温度和Fe3O4理论添加量是影响污泥生物炭材料性能的主要参数。在甲基橙初始质量浓度为100 mg/L、溶液体积25 mL、吸附剂用量为20 mg、吸附240 min条件下,分析热解温度和Fe3O4理论添加量对吸附效果的影响,结果如图1所示。

图1 制备条件对甲基橙吸附效果的影响
由图1(a)可知,SBc对甲基橙的去除率和吸附量随热解温度的升高而升高,但当热解温度达到500℃以后,吸附效果变化不大。可能是由于热解温度低于500℃时污泥生物炭未能充分扩孔,比表面积较小,吸附甲基橙的作用位点少;热解温度超过500℃后形成有效空隙,比表面积增大,有效提高了对甲基橙的吸附效果。当 m(SBc)∶m(Fe3O4)=2∶1,Fe3O4@SBc复合材料的吸附效果随热解温度的升高而升高,热解温度为600℃时复合材料对甲基橙的去除效果最好,去除率为94.24%,吸附量达到117.6 mg/g,明显高于对应的SBc。分析原因应该是负载的Fe3O4呈纳米颗粒状均匀分布,增加了复合材料的比表面积,同时增加了表面的含氧官能团,这对甲基橙的吸附有利,后续SBc制备实验中选取600℃为热解温度。
由图1(b)可知,Fe3O4理论添加量对Fe3O4@SBc复合材料吸附甲基橙的效果有明显影响,甲基橙去除率(吸附量)由高到低依次为 Fe3O4@SBc(2∶1)>Fe3O4@SBc(3∶1)>Fe3O4@SBc(1∶1)>Fe3O4@SBc(1∶2)>SBc>Fe3O4@SBc(1∶3)>Fe3O4。 Fe3O4添加过多时,Fe3O4粒子会堵塞SBc表面空隙,且可能形成团聚,对甲基橙的吸附不利;m(SBc)∶m(Fe3O4)为 2∶1 或 3∶1时吸附效果最好,甲基橙去除率分别为94.24%、93.93%。为减少污泥生物炭的添加量并保证较好的处理效果,后续实验选择 m(SBc)∶m(Fe3O4)为 2∶1。
2.2 吸附条件的影响
实际水体的pH范围较宽,是影响吸附效果的一个重要因素。在pH<3.1的溶液中,甲基橙分子结构为二甲氨基苯基偶氮苯磺酸的内盐型式,呈红色;在pH>4.0的溶液中,甲基橙分子结构为二甲氨基苯基偶氮苯磺酸钠盐,呈黄色〔7〕。调节甲基橙溶液pH,考察溶液pH变化对甲基橙去除效果的影响。实验结果表明,当溶液pH介于4~9时,Fe3O4@SBc对甲基橙的去除率变化不大,保持在94%左右;pH为3时去除效果最佳,去除率为96.41%,吸附量为120.52 mg/g,可能与甲基橙分子的存在形式有关。当pH≥9时,吸附量和去除率有所下降,pH为11时吸附量降到113.28 mg/g,去除率降至90.62%。随着pH的增加,溶液中OH-浓度增大,OH-与甲基橙分子在吸附剂表面产生竞争吸附,导致复合材料对甲基橙的吸附位点减少。
在pH为7条件下考察Fe3O4@SBc用量对甲基橙去除效果的影响。结果表明,增加吸附剂用量,甲基橙的去除率变大,但吸附量降低。Fe3O4@SBc用量为1.0 mg时,吸附量高达627.58 mg/g,去除率仅为25.10%;Fe3O4@SBc用量增至10 mg时,吸附量降为229.10 mg/g,去除率达到91.64%;继续增加Fe3O4@SBc用量至20 mg,去除率高达94.20%,吸附量降至117.76 mg/g。此后Fe3O4@SBc继续增加,甲基橙去除率变化有限,单位质量吸附剂的吸附量大幅减少,原因可能是吸附剂加入过多导致吸附位点过剩。为有效去除甲基橙并提高吸附剂使用的经济性,确定吸附剂用量为20 mg。
2.3 Fe3O4@SBc表征
2.3.1 BET分析
孔径分布曲线表明600℃下制备的污泥生物炭主要存在介孔,平均孔径为33.24 nm,但孔隙结构不十分发达,比表面积只有70.32 m2/g;Fe3O4@SBc的孔隙结构比SBc的发达,虽然平均孔径没有变化,但10 nm以下的介孔明显增多,比表面积可达到394.48 m2/g,说明Fe3O4的引入能够增加小尺寸介孔结构和比表面积,有利于染料分子吸附。
由氮吸附-解吸曲线可知SBc和Fe3O4@SBc的吸脱附等温线均属于Ⅱ型等温线,说明材料为非孔结构或平均孔径>20 nm,同时吸附过程是单层吸附。对比2组吸脱附等温线可发现Fe3O4@SBc的N2吸附量明显增加,说明材料的比表面积增大〔8〕。
2.3.2 SEM分析
图2为SBc和Fe3O4@SBc复合材料的扫描电镜照片。

图2 SBc和Fe3O4@SBc的扫描电镜照片
由图2(a)可以看出,SBc的表面粗糙,有非常多大小不均的颗粒,颗粒未见明显孔洞,仅依靠颗粒相互堆叠形成的缝隙和类孔结构,因此比表面积较小。在SBc表面负载Fe3O4后,Fe3O4纳米粒子在材料表面附着,纳米级颗粒明显增多,表面结构更加丰富,小尺寸缝隙和类孔结构明显增多,比表面积增大。SEM分析结果与BET测试结果相符。
2.3.3 XRD分析
图3为SBc和Fe3O4@SBc的XRD谱图。
从图 3 可见,SBc 在 28.42°、40.53°处的衍射峰对应KCl晶体,与实验中的活化剂KOH相符合。Fe3O4@SBc 在 30.14°、35.19°、43.18°、57.08°、62.70°处出现5个衍射峰,出峰位置和强度可与Fe3O4晶体的(220)、(311)、(400)、(511)、(440)晶面对应,与Fe3O4标准图谱(JCPDS,75-1610)一致。 表明 Fe3O4已成功负载到SBc表面。
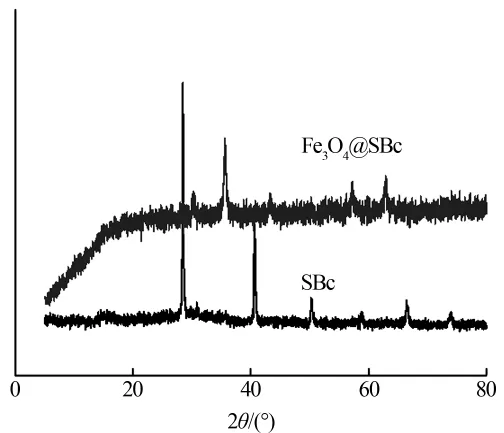
图3 SBc和Fe3O4@SBc的XRD谱图
2.3.4 红外分析
SBc和Fe3O4@SBc的红外谱图中出现大致相同的吸收峰,其中3 419 cm-1处为—OH的伸缩振动峰,2 077 cm-1处为—C≡C—的伸缩振动峰,1 624 cm-1为—C=C—的伸缩振动峰,1 035 cm-1处为醚键的特征吸收峰。与SBc相比,Fe3O4@SBc的吸收峰更加丰富,1 400 cm-1处出现的应为C—OH伸缩振动峰,587 cm-1出现1个弱峰,为Fe—O的典型伸缩振动峰〔9〕,表明 Fe3O4已成功与 SBc 复合,得到磁性污泥生物炭复合材料。
2.3.5 VSM分析
在室温条件下测得Fe3O4@SBc复合材料的磁滞回线,发现其磁滞回线呈S型并经过原点,表明复合材料在无外加磁场时的剩余磁化强度与矫顽力为0。说明制备的Fe3O4@SBc具有超顺磁性,不会发生磁团聚,能够均匀分散在水溶液中。Fe3O4@SBc的饱和磁化强度约为32.38 emu/g,能够在外加磁场作用下有效快速分离〔10〕,克服传统吸附剂不易分离的缺陷。
2.4 吸附机理分析
2.4.1 等温吸附
吸附等温线能够揭示甲基橙溶液的平衡浓度与吸附剂吸附量之间的关联,解释吸附剂与甲基橙之间的相互作用。用Langmuir模型和Freundlich模型对吸附数据进行拟合,结果见图4、表1。
由图4和表1可知,Fe3O4@SBc对甲基橙的吸附数据拟合结果与Langmuir模型、Freundlich模型均比较符合(R2>0.95)。其中 Langmuir模型的相关系数 R2略高,达到 0.996,因此相对 Freundlich模型(R2=0.988),Langmuir模型能更好地描述 Fe3O4@SBc对溶液中甲基橙的吸附行为,说明该吸附以单层吸附为主。

图4 Fe3O4@SBc对甲基橙的等温吸附拟合曲线

表1 Fe3O4@SBc的等温吸附拟合数据
2.4.2 吸附动力学
Fe3O4@SBc吸附甲基橙的吸附动力学模型拟合见图5,相关参数见表2。

图5 Fe3O4@SBc对甲基橙的吸附动力学拟合

表2 Fe3O4@SBc吸附动力学拟合数据
由图5、表2可知,拟二级动力学模型计算值qe(120.11 mg/g)与实验值 qe,exp(120.20 mg/g)基 本 一致,拟二级动力学模型拟合参数(R2=0.959)比拟一级动力学模型拟合参数(R2=0.635)高,可见拟二级动力学模型可以解释Fe3O4@SBc吸附甲基橙的过程,Fe3O4@SBc对甲基橙的吸附主要是化学吸附。
2.5 循环性能测试
采用微波水洗和再次热解2种方法对Fe3O4@SBc进行活化,考察活化方法和循环次数对吸附效果的影响。结果表明,Fe3O4@SBc具有良好的重复利用性能,用微波水洗方法活化后重复使用5次,甲基橙去除率仍能达到75.76%,但相比活化前降低了近20%,说明复合材料表面有部分活性位点对甲基橙吸附稳定,采用水洗方法不能使甲基橙脱附。在600℃热解活化270min后,Fe3O4@SBc重复使用5次时,对甲基橙的去除率高达93.01%,相比活化前下降了2.40%,表明热解的活化效果更加突出,可将使用后的复合材料集中收集后进行热解活化处理,吸附的甲基橙发生碳化,这样能够降低能耗,同时不造成二次污染。
3 结论
利用污水处理厂剩余污泥制备SBc生物炭,然后用共沉淀法将纳米磁性粒子负载到SBc表面制备复合材料 Fe3O4@SBc,采用 SEM、BET、FT-IR、XRD和VSM对该材料进行表征,并考察Fe3O4@SBc对溶液中甲基橙的吸附性能。
(1)在热解温度为600℃、活化剂KOH(浸渍质量比3∶1)、升温速率10℃/min条件下制备的污泥生物炭有较大的比表面积;共沉淀法操作简单,能成功制备Fe3O4@SBc复合材料。
(2)Fe3O4@SBc的比表面积明显大于 SBc,达到394.48 m2/g,平均孔径与SBc的相当,充分说明比表面积的增加与纳米Fe3O4的复合有直接关系,间接说明材料表面为粒子堆积形成的缝隙或类孔结构;Fe3O4@SBc具有超顺磁性,在外加磁场作用下可快速从溶液中分离。
(3)pH为 3时 Fe3O4@SBc对溶液中甲基橙的吸附效果最好,甲基橙去除率为96.41%,吸附量为120.52 mg/g,pH≥9后降低;去除率随着吸附剂用量的增加而增大。
(4)Fe3O4@SBc对溶液中甲基橙的吸附符合拟二级动力学模型,主要为化学吸附;吸附等温线符合Langmuir模型,为单分子层吸附。
(5)Fe3O4@SBc经600℃热解活化,重复使用5次甲基橙去除率依然高达93.01%,说明热解活化更有利于复合材料的重复使用。

