肝移植术后胆道并发症的处理经验分析
王秋果,王冠武,董文婧,肖湘月,李亭(中南大学湘雅二医院肝脏移植科,湖南长沙410011)
自1963年世界首例肝移植于临床开展以来,肝移植术已然成为治疗肝功能衰竭、肝硬化、肝脏恶性肿瘤等终末期肝病的最有效外科治疗手段。当前在我国每年逾30 万等待器官移植患者中,据国际器官捐献和移植登记处(International Registry In Organ Donation And Transplantation,IDODaT) 数据显示,2018年仅20199例患者接受器官移植手术,其中完成肝移植(包括尸肝及活体肝移植)仅6 279例。Nemes等[1]在纳入14 411例肝移植患者的研究中指出,移植后胆道并发症(biliary complications,BC) 平均发生率高达23%,其中胆漏发生率为8.5 %,胆道狭窄发生率为14.7 %,病死率为1%~3%,在器官严重短缺的时代背景下,肝移植术后BC犹如“阿喀琉斯之踵”严重威胁患者心理及生理健康[2-3]。因此,提高对肝移植后BC危险因素、诊治措施认识,对于提高肝移植患者生存期限及生活质量具有重要意义。现就本中心2 例肝移植后典型BC病例(发生胆道狭窄1例、胆漏1例)进行如下探讨分析。
1 资料与方法
1.1 病例1:患者男性,44 岁,酒精性肝硬化(失代偿期),术前总胆红素(total bilirubin,TBil)为277 μmol/L、终末期肝病模型(model for end-stage liver disease,MELD)评 分 为31分。于2019年2 月1日行经典原位肝移植术(orthotopic liver transplantation,OLT),术中胆道吻合方式为胆道端端吻合,吻合口处胆管外径约2.5 mm,肝脏二次热缺血时间为40 min,供肝热缺血时间为0 min,冷缺血时间为7.2 h,术后供肝病理检查无肝细胞脂肪样变等病理改变。
术后14 d,患者肝功能检验结果提示碱性磷酸酶(alkaline phosphatase,ALP)、谷氨酰肽转移酶(gumatyl transpeptidase,GGT)激增,天冬氨酸转氨酶(aspartate aminotransferase,AST)、丙氨酸转氨酶(alanine aminotransferase,ALT)、TBil、直接胆红素(direct bilirubin,DBiL)进行性增高,巨细胞病毒(cytomegalovirus,CMV)-DNA 106 copies/ml,患者伴随尿黄、巩膜黄染、陶土样便症状加重,遂于术后20 d 行磁共振胰胆管成像(magnetic resonance cholangiopancreatography,MRCP)检查,提示胆管吻合口处狭窄(图1)。结合患者症状、实验室及影像学检查,移植后BC诊断明确,给予DNA多聚酶抑制药物抗病毒治疗,于术后24 d行内窥镜逆行胰胆管造影(endoscopic retrograde cholangiopancreatography,ERCP)+塑料支架置入治疗,术中见胆管吻合口处狭窄、肝内胆管扩张明显,手术效果满意,支架置入后胆汁引流通畅,术后未见胰酶增高等并发症。患者尿黄、皮肤巩膜黄染、陶土样便症状逐渐消失,定期复查肝功能检查结果提示各项指标逐渐降至正常水平,CMV核酸检测转阴,复查增强CT(图1)提示未见明显扩张胆管,患者顺利出院。

图1 病例1的影像学检查
1.2 病例2:51岁男性患者,诊断“慢加急性肝衰竭、肝炎后肝硬化(失代偿期)”,术前MELD评 分 为35分、TBiL 为785.5 μmol/L,于2017年8月22 日行OLT,术中胆道采用端端吻合方式重建、肝脏二次热缺血时间为85 min;供肝热缺血为0 min、冷缺血时间为8.2 h,供肝术后病理检查无肝细胞脂肪样变等病理改变。
患者术后15 d 出现右下腹痛、发热,伴腹膜炎体征,文氏引流管引流液增多,呈胆汁样,术后16 d 予查MRCP,提示胆漏(图2);患者系治疗配合欠佳,难以进行ERCP 治疗,安排经皮肝穿刺胆道引流(percutaneous transhepatic cholangial drainage,PTCD)治疗首次失败后于术后23 d 再行PTCD,手术顺利、建立充分外引流,且术中造影可见胆总管中段吻合口造影剂外溢,进一步证实胆漏,患者胆漏治愈,顺利出院。
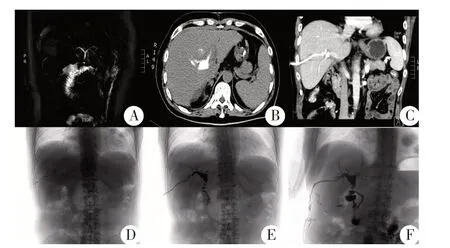
图2 病例2 的影像学检查
2 结果
病例1患者术后3月余,行ERCP 支架顺利取出;病例2患者术后3月余复查,经PTCD管造影显示造影剂未见外溢、胆漏愈合,成功拔出置管。两例患者经ERCP、PTCD治疗后TBil、DBil、GGT、ALP、AST 及ALT 等血生化指标定期复查结果如图所示(图3、图4),未见异常增高,2 例患者在后续随访及复查中均未出现胆道狭窄等BC临床症状,移植后BC得以缓解。
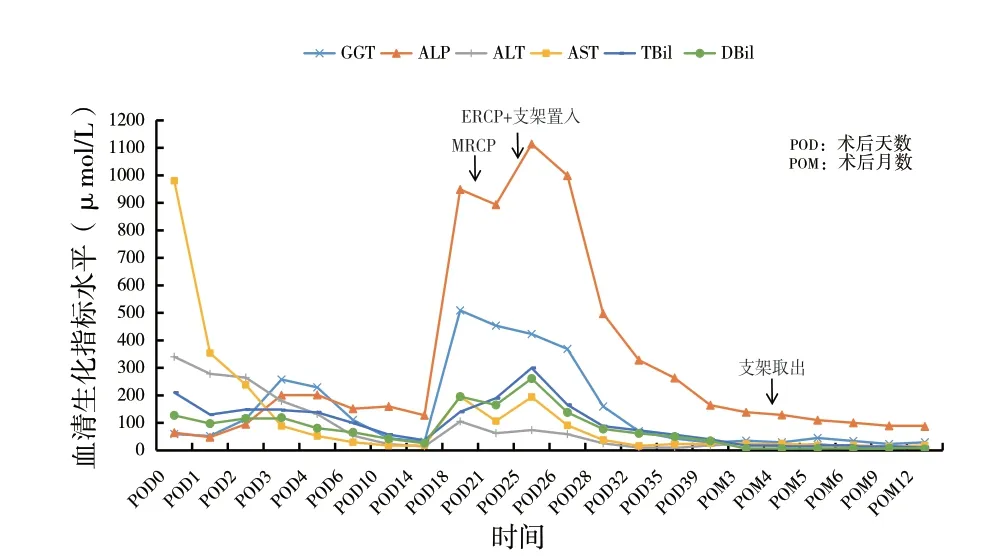
图3 例1患者围术期及术后随访生化指标
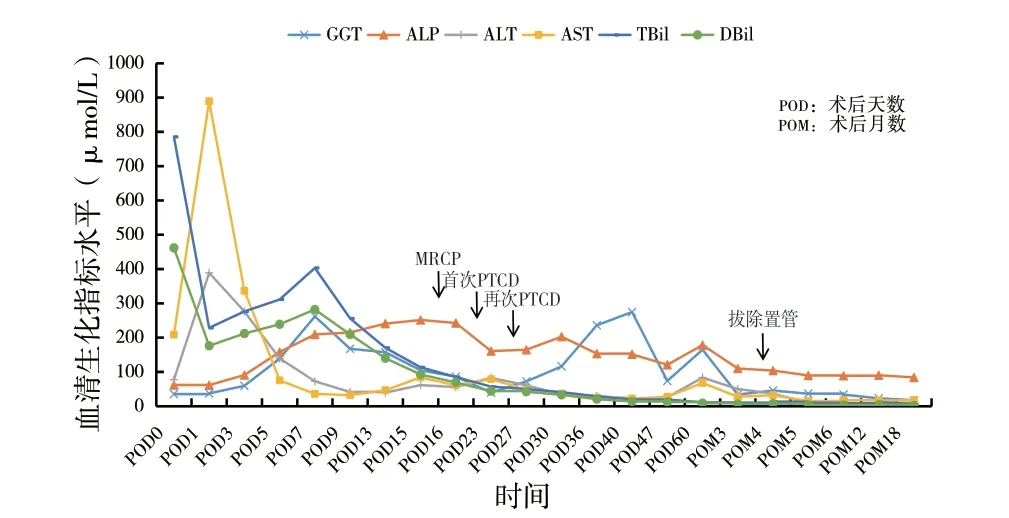
图4 例2 患者围术期及术后随访生化指标
3 讨论
自Starzl医生首次成功开展肝移植手术至今,一方面随着手术技术发展、免疫抑制方案不断改进、围术期护理精化、器官保存手段持续优化,提高肝移植手术疗效及受体围术期生存率;另一方面John 等[3]在一项探讨影响肝移植后患者远期(术后20 年)预后及生活质量的前瞻性横断面研究中指出,BC 可显著影响患者预后、生理及心理健康,进一步对患者社会功能产生不同程度消极影响。因此,BC的早期诊断、及时干预对于改善肝移植远期预后具有重大意义。
3.1 危险因素:有文献报道指出,供体来源因素诸如供体年龄、脂肪肝、肝动脉变异,手术相关因素诸如冷缺血>12 h、二次热缺血时间>50 min、胆道灌洗不足、无肝期时间、T 管、胆道重建方式等可能与移植后BC发生相关[1,4]。同时,受体移植前MELD>25 分、血清胆红素水平高,术后急性排斥反应、CMV感染等与BC发生可能相关。并且有研究进一步指出二次热缺血时间>50 min 是胆漏发生的独立危险因素[4],肝脂肪变性(>25%)是胆道狭窄发生的独立危险因素[5],肝动脉变异是发生胆道狭窄及胆漏的独立危险因素[6]。
3.2 临床特征:肝移植后BC以胆道狭窄及胆漏最为常见。据国外研究报道,尸肝肝移植后胆道狭窄发生率为13%,胆漏发生率为5%~10%,活体肝移植后受体胆道狭窄发生率为19%,胆漏发生率为10%~15%[7-9]。胆漏多发生于术后早期,患者常表现不同程度腹痛,同时伴有腹膜刺激征,腹腔引流管引流液性质呈胆汁样改变,甚至出现胆汁经切口渗出情况。胆道狭窄发生通常迟于胆漏,其可分为吻合口狭窄及非吻合口狭窄,吻合口狭窄通常于术后早期出现,多由于吻合口血供不良及胆漏引起炎性狭窄或者瘢痕愈合引起,非吻合口狭窄出现较晚,多与免疫相关性或缺血相关性因素相关。胆道严重狭窄患者多以梗阻性黄疸为主要特征,表现为尿黄、皮肤巩膜黄染、陶土样便、胆红素进行性增高及肝功能受损等。BC患者临床表现差异大,部分患者可无明显症状,仅存在胆红素及相关肝功能指标异常[10]。
3.3 检查及诊断方法:血清ALP、GGT 是早期发现BC的重要指标,发生BC时,往往较血清胆红素及肝酶指标更早出现异常。当血生化指标ALP、GGT、肝酶及胆红素指标异常增高时,应早期行影像学检查排查BC。当前B超、MRCP、CT 及胆道造影技术是应用于临床诊断移植后BC主要影像技术。胆道造影是诊断BC金标准,能够明确显示胆道病变类型、部位以及程度。MRCP 作为一种术日趋成熟的无创检查手段,对发现肝内外胆道系统有无狭窄、扩张及探查发生部位、评估病变程度,具有较高的敏感性、特异性(敏感性98%、特异性94%),已成为移植后诊断BC首选检查手段[10-11]。B 超在术后早期发现BC敏感性及特异性仅为77%、67%,但因其简便、高时效性,是肝移植术后首选常规影像学检查[12]。
3.4 治疗措施:随着内镜、介入技术飞速发展,移植后BC的治疗措施由手术治疗主导型逐渐过渡至以内镜、介入治疗为主。Sarhan 等[13]在单中心回顾性研究中指出,ERCP、PTCD介入手段可成功治疗约2/3活体肝移植后BC,对于难治性复杂BC患者适用开腹手术治疗。ERCP 是当前BC非手术治疗的首选方式,集诊断、治疗于一体,包括oddi括约肌切开、球囊扩张及支架置入治疗手段,在术后早期治疗胆漏、吻合口狭窄相关BC具有较大优势,而对于与缺血因素等相关非吻合口狭窄患者,ERCP 疗效受限。对于良性胆道狭窄可予塑料支架治疗,因塑料支架易发生堵塞可能需多次扩张胆道及置入支架,金属支架口径较大且长期支撑的优势被用于恶性胆道狭窄的治疗。且移植后发现胆道狭窄等BC愈迟,成功率愈低,因此,尽早进行ERCP 治疗是改善肝移植后BC患者预后之关键。当ERCP 导管无法顺利进入狭窄胆道、患者无法耐受难以进行ERCP 等意外情况发生时,PTCD可作为BC有效补救治疗方案,且有移植中心指出可作为肝肠吻合后发生BC有效替代治疗方案[14];PTCD常用于缓解急性胆道梗阻的患者,也可用于胆漏患者,具有创伤小、安全性高的相关特点,针对部分胆漏的患者,可以考虑早期行PTCD予胆汁充分外引流,以减轻胆道压力,促进胆道愈合。
本报道病例1中,患者胆管吻合口处外径细窄、术后发生CMV感染,在早期抗CMV治疗纠正BC相关危险因素及ERCP 支架置入扩张狭窄胆道后,患者预后良好。病例2 胆漏患者,术中肝脏二次热缺血时间长可能作为胆漏发生主要原因之一,患者术后精神状态差、难以耐受ERCP,及时进行PTCD建立外引流后,感染、精神等并发症状缓解,胆漏治愈,患者远期预后良好。此经验可借鉴于精神状态差、配合欠佳等部分特殊移植后BC患者治疗。本中心认为早期BC预防和处理在于:① 尽可能减缩供肝冷、热缺血时间及二次热缺血时间、精细吻合;受体MELD评分高、CMV感染,供肝脂肪样变、肝动脉变异等BC发生相关危险因素可作为早期预测指标,加强常规检查手段,早期干预;② 术后常规复查ALP、GGT、AST、ALT、胆红素等血生化指标可评估疗效及辅助诊断,适时进行超声、MRCP 等影像学检查,也可帮助临床医生早期诊断、准确评估病情及疗效;③ 早期纠正胆道狭窄病因并行支架植入可有效解决部分肝移植术后胆道狭窄,PTCD建立充分外引流可作为部分移植术后胆漏的主要治疗手段。并且通过提高手术熟练度、提升操作技术、及时纠正相关危险因素、加强术后随访及复查评估,也是预防远期BC的关键所在。
总之,肝移植术后BC严重影响肝移植患者的生活质量及生存期限,是导致肝移植术后患者再次移植甚至死亡的最不利因素之一。有必要对其危险因素、临床特征、诊治措施进行深入综合研究,进一步提高肝移植术后围术期及远期疗效。

