阿托伐他汀联合氯吡格雷对脑梗塞二级预防患者颈动脉斑块的影响
邸春钰,刘 欣,马连未,刘登军
(1.保定市第四中心医院,河北 保定 072350; 2.浙江大学明州医院,浙江 宁波 315100)
脑梗塞是神经内科常见疾病之一,动脉阻塞后其局部脑组织受损,引发缺血、缺氧、坏死以及神经功能障碍,其中老年人是该病多发群体[1]。脑梗塞患者发病急骤,治疗周期较长,发病率、病死率、致残率和复发率均较高[2]。复发性脑梗塞可引发严重残疾,且预后较首次发病更差[3],因此必须实施有效的二级预防。动脉粥样硬化(AS,atherosclerosis)是脑梗塞的重要致病因素,其中血栓形成与颈动脉粥样斑块破损被认为是引发脑梗塞的重要机制[4]。研究证实卒中复发率高与未能有效控制并稳定颈动脉斑块有关[5],因此有必要对动脉粥样硬化形成进行针对性干预。他汀类药物是一种3-羟基-3 甲基戊二酰辅酶 A还原酶抑制药,具有强力降脂和抗炎作用,主要用于治疗胆固醇升高,尤其是低密度脂蛋白胆固醇(LDL-C,low density lipoprotein cholesterol)明显升高的患者,是预治心脑血管疾病的有效药物[6]。研究发现他汀类药物可使颈动脉粥样硬化斑块保持稳定,在脑卒中的预防和治疗中发挥着关键作用[7],其与抗血小板药物联用已被多项临床指南列为缺血性卒中二级预防的推荐方案,但何种他汀类药物联合氯吡格雷能更有效的缩小及稳定颈动脉斑块尚无定论。鉴于此,研究通过对比分析不同他汀类药物(阿托伐他汀、瑞舒伐他汀)联合氯吡格雷对脑梗塞二级预防患者颈动脉斑块及临床疗效的影响,并探讨其药理作用机制,旨在为临床干预提供理论依据。
1 资料与方法
1.1 一般资料
选取2018年6月—2020年6月入保定市第四中心医院神经内科治疗的128例急性脑梗塞患者为研究对象。纳入标准:①符合《中国急性脑梗塞诊治指南2018》中相关诊断标准[8]并经临床或影像学检查确诊为急性脑梗塞,并经头颅MRI检查确诊,颈部彩超及能谱CTA检查明确存在颈动脉斑块(见图1~图4);②年龄42~85岁,且均为恢复期及后遗症期进行二级预防的脑梗塞患者;③首次发病且发病时间大于4周;④NIHSS评分≤23分;⑤存在高血压、糖尿病或高脂血症等一种以上可干预危险因素;⑥入组前2周未接受他汀类或抗血小板药物治疗;⑦血小板计数为150×109~500×109L;⑧签署知情同意书。排除标准:①对研究拟采用药物过敏者或初始静态下合并氯吡格雷抵抗者;② NIHSS评分>23分;③近期曾因严重外伤或其他疾病接受手术治疗者;④近期曾服用质子泵抑制剂者;⑤合并严重心、肺、肝、肾等重要器官疾病、精神疾病或恶性肿瘤者;⑥合并凝血功能障碍、心房纤颤或室间隔缺损者;⑦依从性差或不遵医嘱者;⑧临床资料不全或拒绝参与研究者。采用随机信封法将患者分为A、B两组,每组64例,其中A组男41例,女23例;年龄42~82(65.48±5.52)岁;基础疾病:合并高血压42例,糖尿病15例,高脂血症29例。B组有男40例,女24例;年龄44~84(64.79±5.83)岁;基础疾病:合并高血压40例,糖尿病16例,高脂血症30例。两组一般资料差异无统计学意义(P>0.05),具有可比性。该研究经医院伦理委员会审核批准。
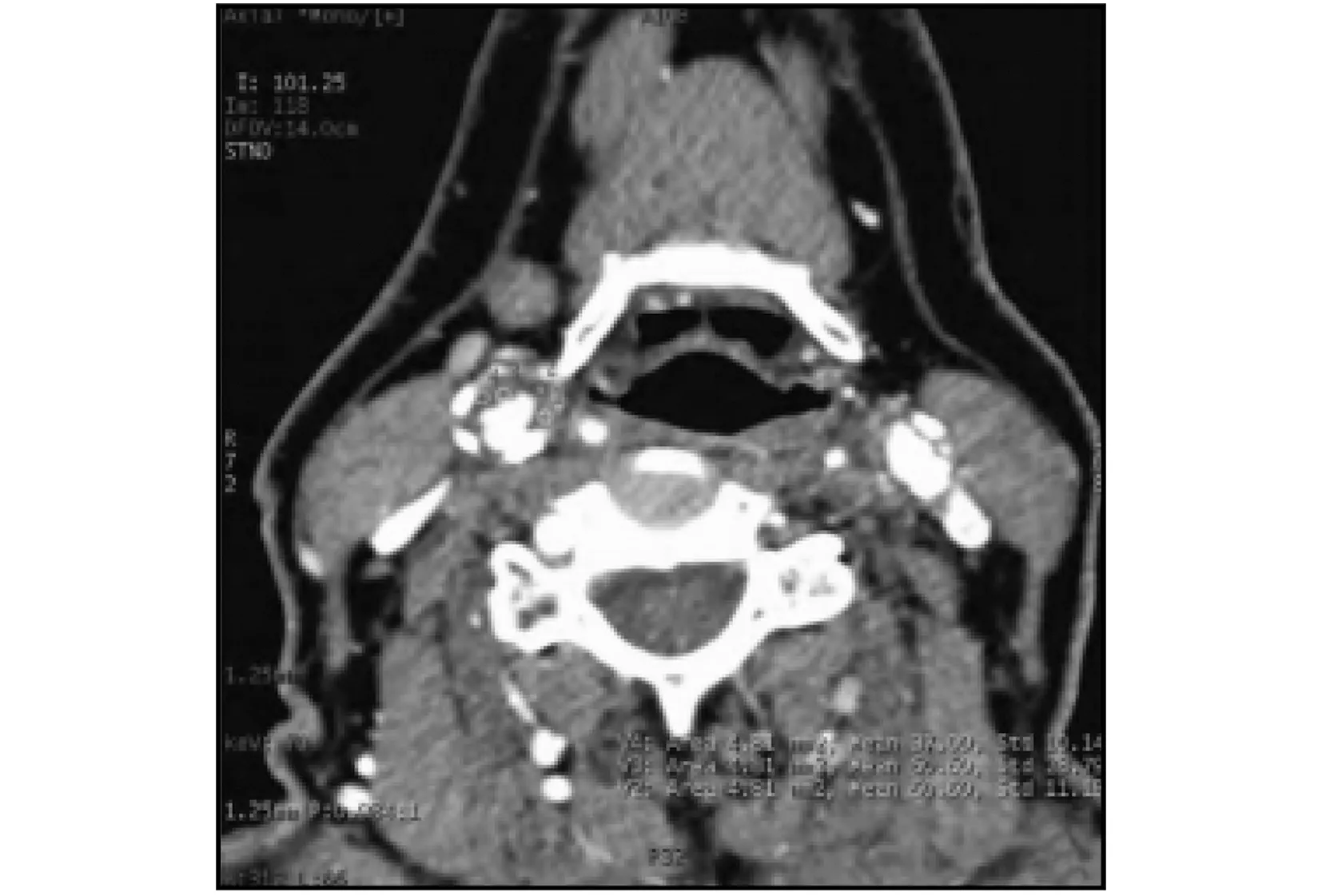
图1 颈部斑块CT冠面图Fig.1 CT coronal view of neck plaque
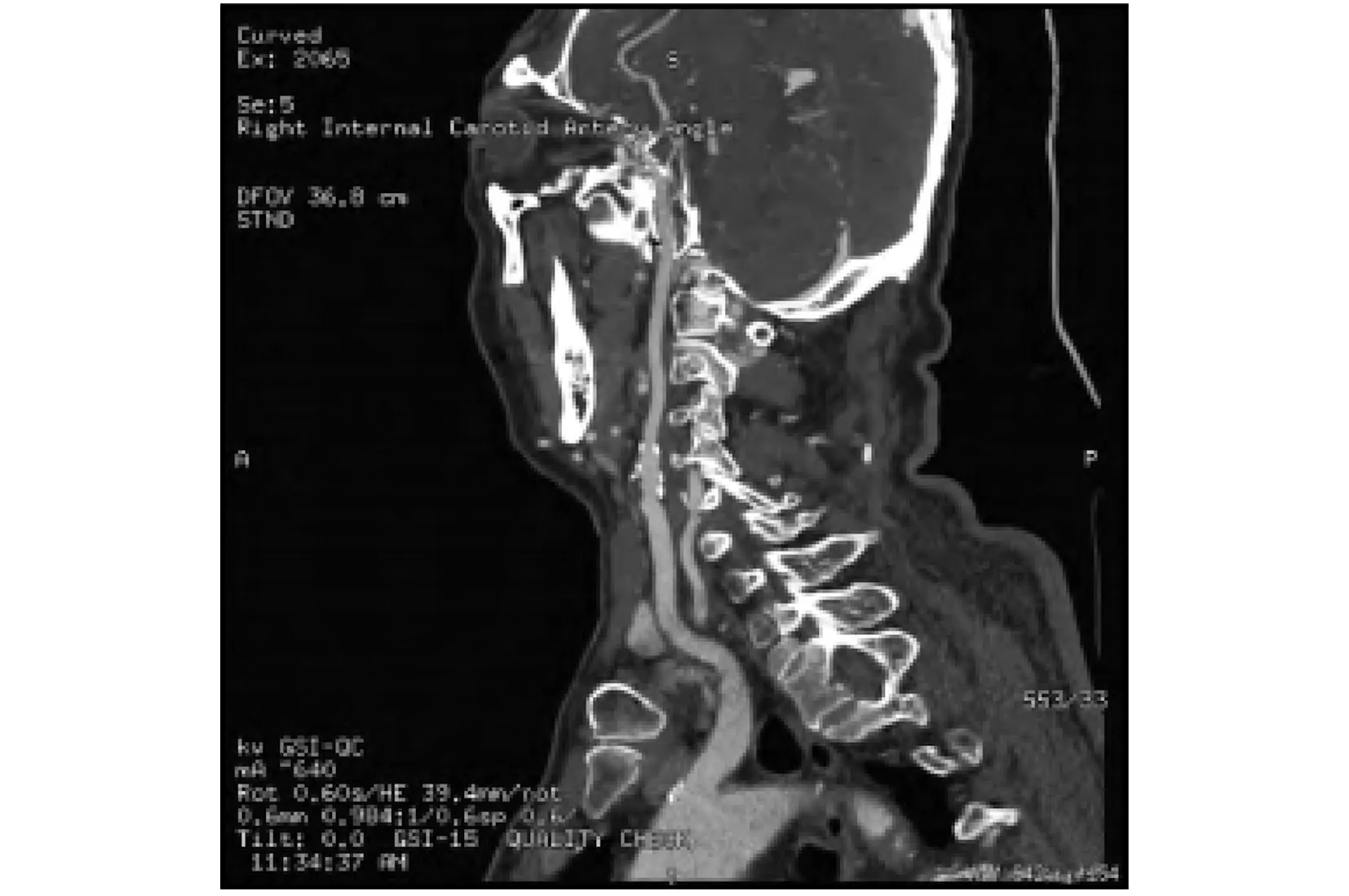
图2 颈部斑块CT立体图Fig.2 CT stereogram of neck plaque
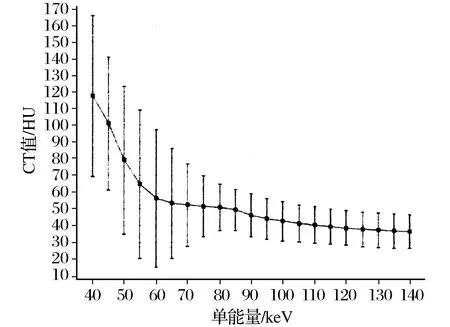
图3 脂肪斑块能谱曲线Fig.3 Energy spectrum curve of fat plaque
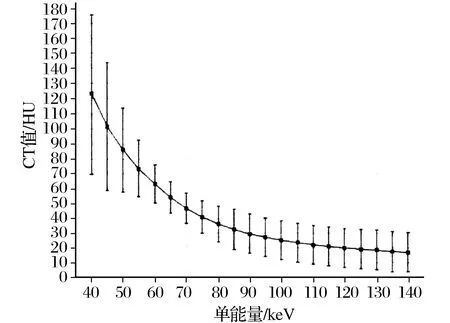
图4 纤维斑块能谱曲线Fig.4 Energy spectrum curve of fiber plaque
1.2 方法
两组均口服氯吡格雷(赛诺菲(杭州)制药有限公司,国药准字H20056410,规格:75mgx7片/盒,用法:75 mg/次,1次/日),A组联合使用阿托伐他汀(辉瑞制药有限公司,国药准字H20051408,规格:20 mg×28片,用法:60 mg/次,1次/日)治疗,B组联合使用瑞舒伐他汀(阿斯利康药业(中国)有限公司,国药准字J20170008,规格:10 mg×7片,用法:20 mg/次,1次/日),两组均连续给药6个月后进行疗效评价。所有患者均根据病情开展合并症治疗,使用降压或降血糖药物控制血压、血糖等,治疗期间勿使用其他抗血小板药物、非甾体抗炎药物或具有抗凝、降纤作用的药物。
1.3 颈动脉彩超检查方法
检查前仔细询问患者病史和近期临床症状,及时了解既往检查情况,注意对比前后结果。采用多普勒超声诊断仪(飞利浦IU22),选择5~10 MHz线阵探头,如血管位置较深,颈部肥胖、粗短或颈动脉分叉较高很难显示血管者选用2~5 MHz线阵探头。检查时患者取仰卧位,头后仰以充分暴露颈前区,如暴露不满意可于颈后垫枕。检查时注意观察颈动脉走形、管腔及管壁结构,测量颈动脉内中膜厚度(IMT,intimal medial thickness),观察管腔内径是否均匀、有无局部狭窄或扩张现象、与周围组织器官的关系、是否受压变窄等。彩色多普勒注意观察血流方向、充盈状态、速度分布及类型等,准确测量血流频谱及参数。观察颈动脉内膜状况(是否光滑、有无增厚或斑块形成)和斑块性质(内部是否均质、回声强度与形态、斑块稳定性、管腔狭窄状况、血流动力学改变等)。取适量耦合剂涂抹于探头处,后置于颈根部近锁骨处,以横、纵断面连续扫查颈部动脉,努力探查至颈部最高点。检查时可通过血流频谱及分支血管情况区分颈内动脉与颈外动脉,超声检查均由同一名医师完成。
1.4 观察指标
(1) IMT、斑块面积(PA,plaque area)、不稳定性斑块数目和动脉狭窄率:于治疗前后采用彩色多普勒超声行颈动脉超声检查,IMT为超声测得局部颈总动脉结构显示最清晰处,测5次取均值。内膜增厚:颈动脉IMT≥1.0 mm且分叉处IMT≥1.2 mm。IMT局限性≥1.5 mm定义为斑块,其形成时间、组织结构存在差异,特征与稳定性也不尽一致。测量斑块的3条直径,以数值相对较大的2条作为斑块的长度与宽度,二者相乘即为PA。以病变远端颈内动脉直径为参照,颈动脉直径减小低于30%视为轻度狭窄,减小30%~69%为中度狭窄,减小70%~99%为重度狭窄,100%提示完全闭塞。
(2) 血脂水平:于治疗前和治疗6个月后采用全自动生化分析仪检测并记录两组血清总胆固醇(TC,total cholesterol)、甘油三酯(TG,triglyceride)和低密度脂蛋白胆固醇(LDL-C,low-density lipoprotein cholesterol)水平。
(3) 血液流变学指标:于治疗前和治疗3个月后测定低切全血粘度(LBV,low-cut whole blood viscosity)、全血黏度(WBV,whole blood viscosity)、纤维蛋白原(FIB,fibrinogen),采用半自动血液流变分析仪(赛科希德型 SA-5000)检测血液流变学指标,试剂盒为仪器配套试剂,严格依据说明书操作。
(4) 血小板聚集率:于治疗前和治疗后1个月、3个月、6个月采集空腹肘静脉血,于2 h内送至检验科,采用PL-11多参数血小板分析仪检测不同时期血小板聚集率。
(5) 不良反应:统计两组治疗期间药物不良反应(肝酶升高、肌酶升高或肌肉疼痛、肾功损害)发生情况。
(6) 复发:均随访12个月,参照Sacco等[9]报道的标准判断并统计两组复发情况。
1.5 统计学方法
2 结果分析
2.1 128例脑梗塞患者颈部斑块分析
128例脑梗塞患者共检出纤维斑块62块,占48.44%;血栓斑块39块,占30.47%;脂肪斑块27块,占21.09%。CT图像和能谱曲线图如图1~图4所示。
2.2 两组治疗前后颈动脉斑块评估指标比较
治疗6个月后A、B两组患者IMT均较治疗前明显缩小(P<0.05),斑块面积均较治疗前明显缩小(P<0.05),A组治疗后斑块面积明显小于B组(P<0.05)。治疗后两组不稳定性斑块数目较治疗前明显减少(P<0.05)。治疗后A、B两组颈动脉狭窄率均较治疗前下降(P<0.05),A组颈动脉狭窄率低于B组,但差异无统计学意义(P>0.05),数据详见表1。
表1 两组颈动脉斑块评估指标比较Table 1 Comparison of carotid plaque indexes between the two groups before and after
2.3 两组治疗前后血脂指标比较
治疗前两组患者血脂指标无明显差异(P>0.05),治疗后两组血脂指标较治疗前明显下降(P<0.05),但组间差异无统计学意义(P>0.05),数据详见表2及图5~图7。
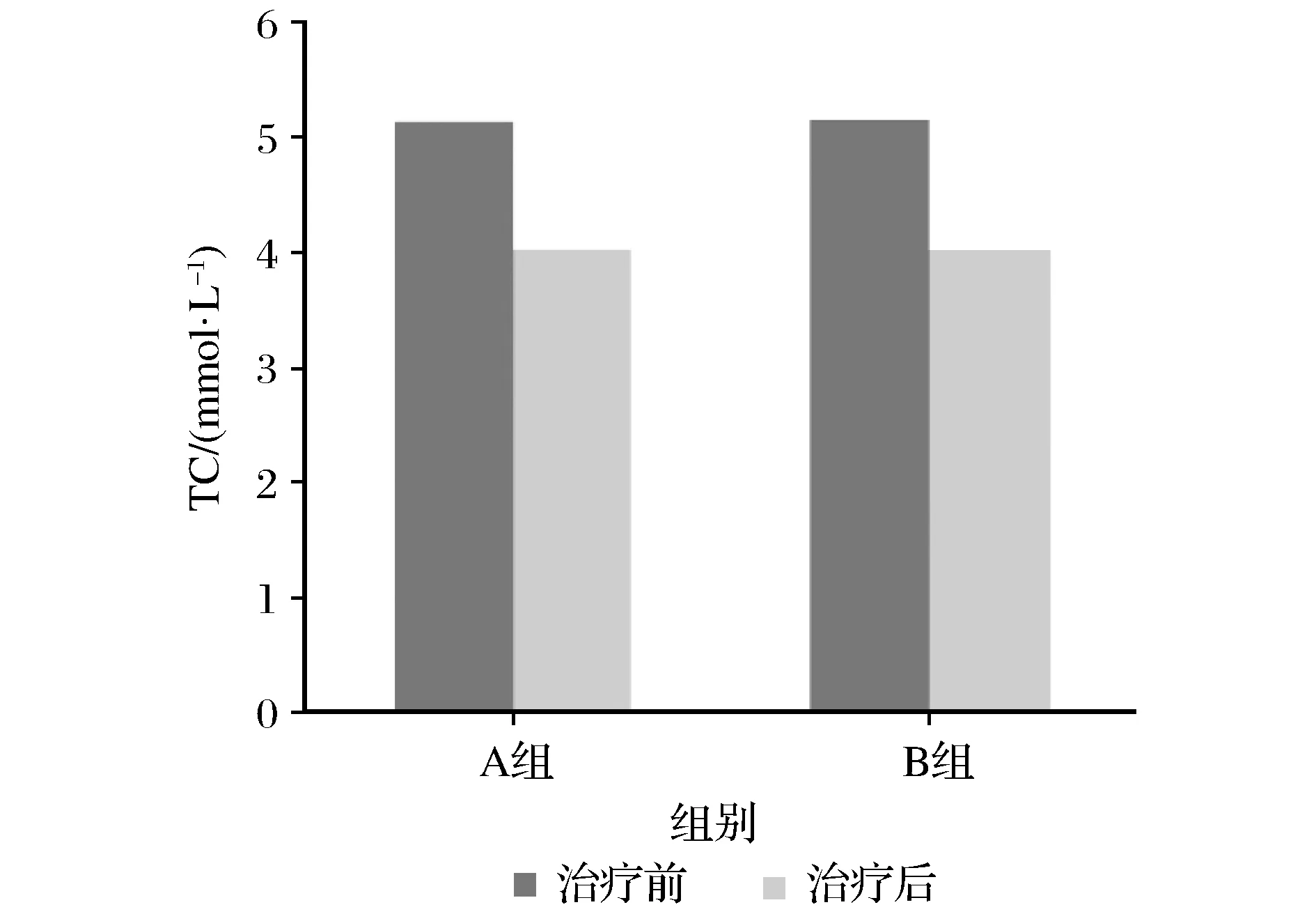
图5 两组TC水平比较Fig.5 Comparison of TC levels between the two groups before and after
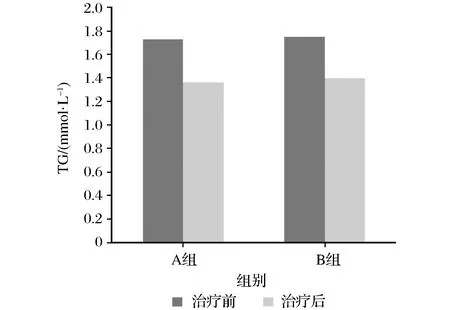
图6 两组TG水平比较Fig.6 Comparison of TG levels between the two groups before and after
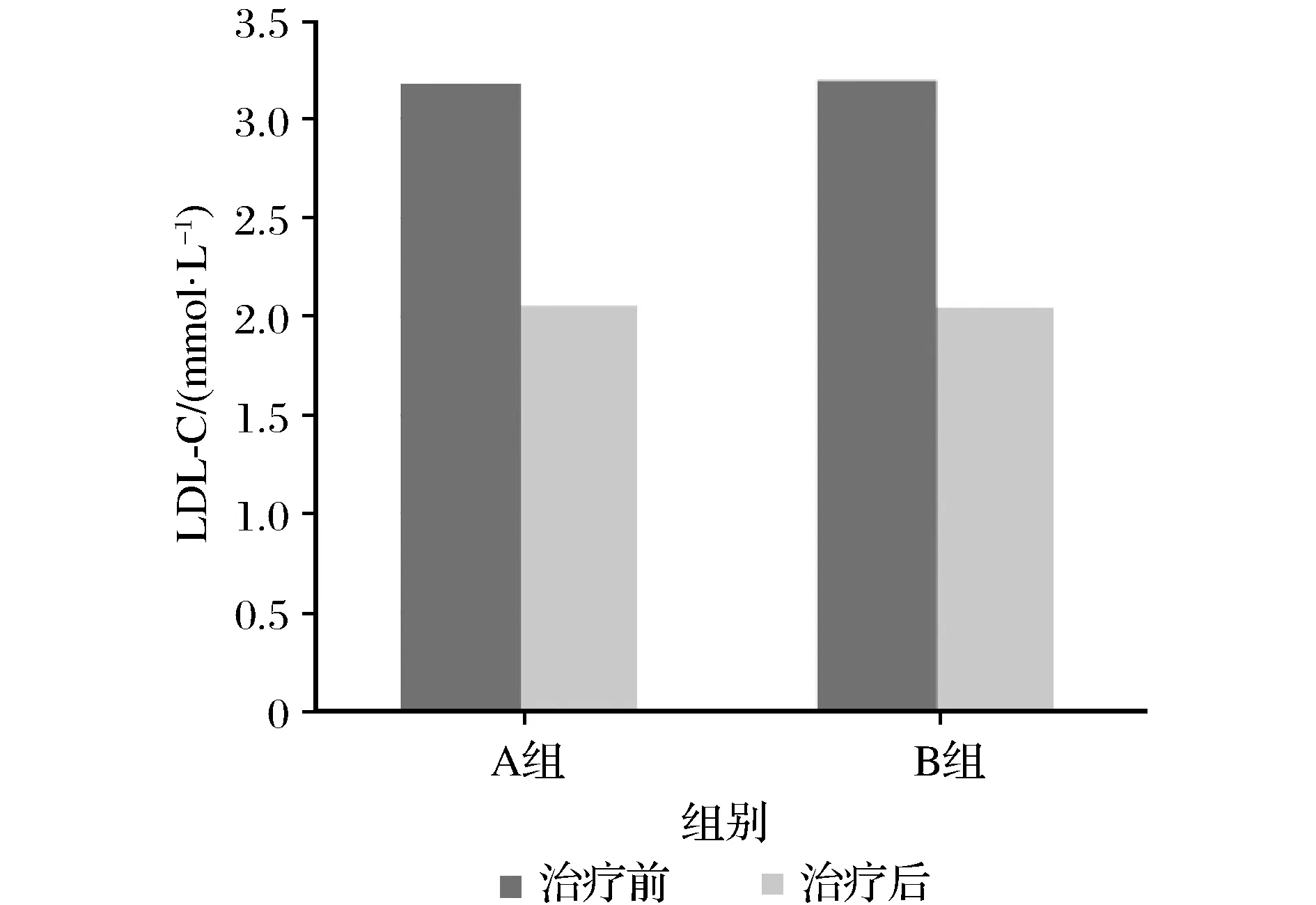
图7 两组LDL-C水平比较Fig.7 Comparison of LDL-C levels between the two groups before and after
2.4 两组治疗前后血液流变学指标比较
治疗前两组患者血液流变学指标无明显差异(P>0.05),治疗后两组血液流变学指标较治疗前下降(P<0.05),但组间差异无统计学意义(P>0.05),数据详见表3及图8~图10。
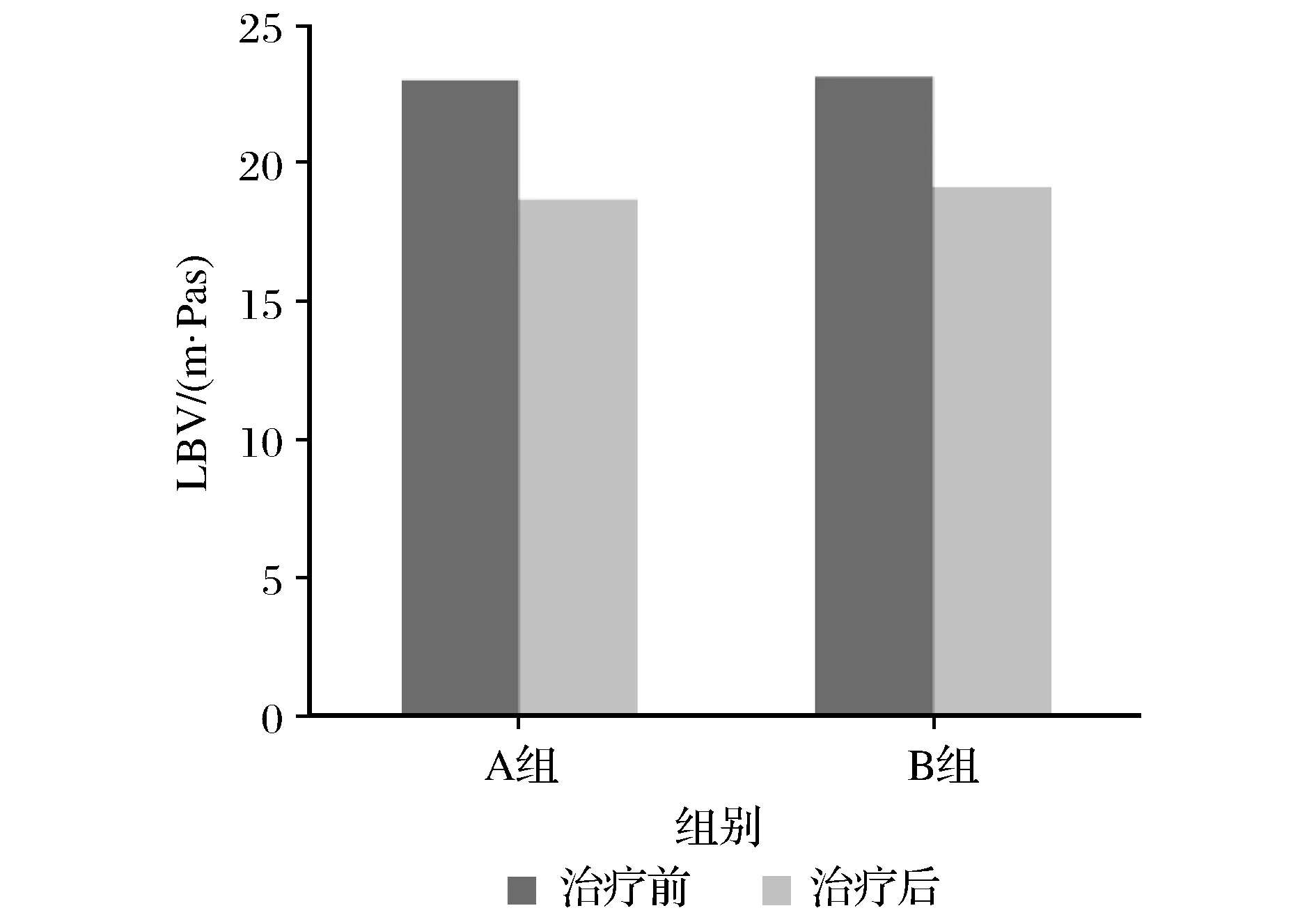
图8 两组LBV水平比较Fig.8 Comparison of LBV levels between the two groups before and after
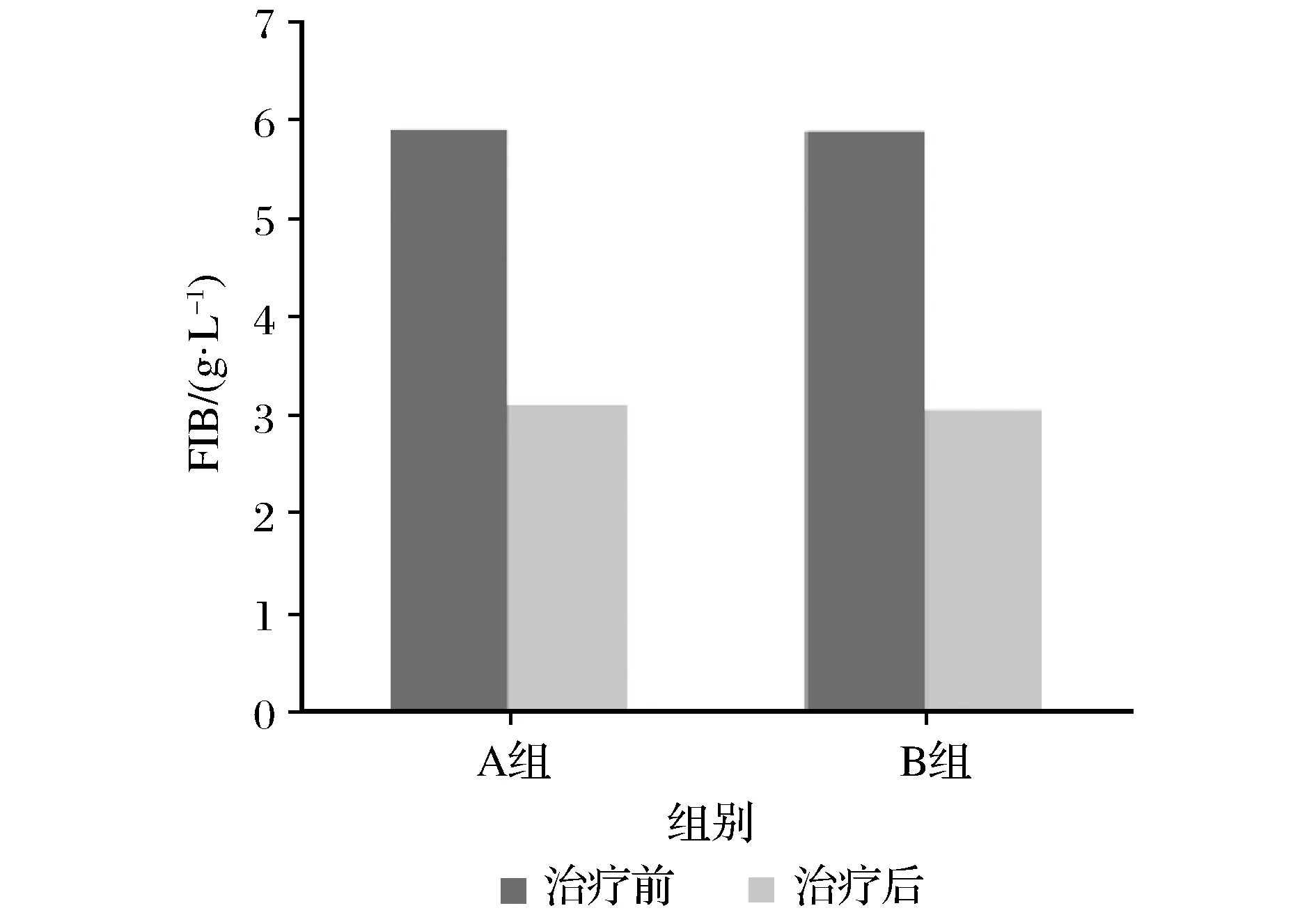
图10 两组FIB水平比较Fig.10 Comparison of FIB levels between the two groups before and after
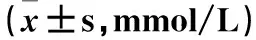
表2 两组血脂指标比较Table 2 Comparison of blood lipid indexes between the two groups before and after
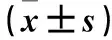
表3 两组治疗前后血液流变学指标比较Table 3 Comparison of hemorheology indexes between the two groups before and after
2.5 两组治疗前后血小板聚集率比较
治疗前A、B两组患者血小板聚集率差异无统计学意义(P>0.05),治疗1个月、3个月、6个月后A、B两组的血小板聚集率均明显下降(P<0.05),但组间各时点差异均无统计学意义(P>0.05),数据详见表4及图11。
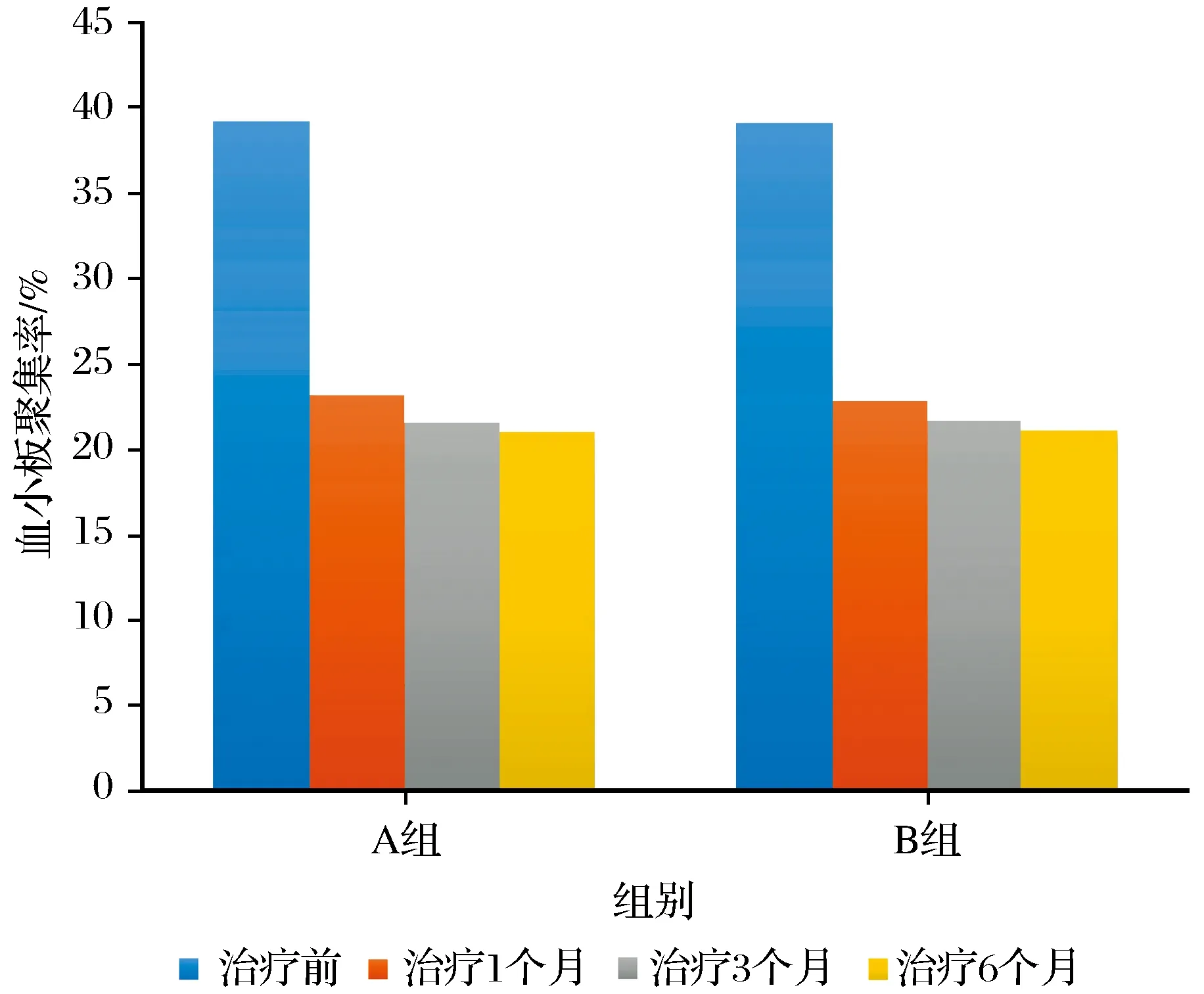
图11 两组血小板聚集率比较Fig.11 Comparison of platelet aggregation rate between the two groups before and after 1 month, 3 months, 6 months
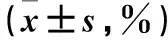
表4 两组血小板聚集率比较Table 4 Comparison of platelet aggregation rate between the two groups
2.6 两组不良反应发生情况和卒中复发率比较
A组出现肝酶升高1例,肌酶升高或肌肉疼痛2例,不良反应发生率为4.69%;随访复发7例,占10.94%。B组出现肝酶升高5例,肌酶升高或肌肉疼痛6例,不良反应发生率为17.19%,随访复发6例,占9.38%。A组不良反应发生率低于B组,差异有统计学意义(χ2=5.133,P=0.024),复发率高于B组,但差异均无统计学意义(χ2=0.086,P=0.770)。
3 讨论
他汀类药物可在有效控制血脂的前提下通过抑制内皮祖细胞功能障碍及凋亡、降低同型半胱氨酸水平等机制延缓动脉粥样硬化的发生发展[10]。IMT是衡量早期颈动脉硬化程度的重要指标,而PA则是观察动脉粥样硬化的直接指标[11]。有研究[12]指出,阿托伐他汀联合氯吡格雷抗动脉粥样硬化的作用强于单一他汀类药物,能更好地改善急性脑梗死患者的IMT和PA。另有研究[13]发现氯吡格雷加用阿托伐他汀能提高脑梗死伴斑块患者的临床治疗效果,认为二者联合在抗动脉粥样硬化方面的效果优于单用氯吡格雷。此次研究发现,治疗6个月后A、B两组患者IMT均明显下降,PA缩小,不稳定性斑块数目较治疗前明显减少,颈动脉狭窄率均较治疗前下降。这提示阿托伐他汀或瑞舒伐他汀联合氯吡格雷治疗均可缩小颈动脉斑块面积,降低颈动脉内膜中层厚度,减轻动脉狭窄程度,并可在一定程度上提高颈动脉斑块的稳定性。此次研究还发现,A组治疗前后PA的降幅较B组更大,且A组治疗后斑块面积明显小于B组,这提示在缩小斑块面积方面使用阿托伐他汀联合氯吡格雷获益更明显。不稳定斑块通常称为“软斑”,它含有较大的脂质核心,且浸润着大量炎性细胞,易出现纤维帽破裂,引发斑块内出血[14]。研究发现经治疗后不稳定斑块数目明显减少,说明采用阿托伐他汀或瑞舒伐他汀联合氯吡格雷在抗颈动脉粥样硬化方面效果显著,其可能机制在于:(1)阿托伐他汀或瑞舒伐他汀均有较强的调脂作用,能有效降低LDL-C、TG以及血浆极低密度脂蛋白(VLDL)浓度,这可能是上述药物能促进斑块消退的重要原因。研究结果支持该结论,通过为期6个月的中等强化他汀治疗后A、B两组患者的血脂指标均较治疗前明显下降,且治疗期间未见心肌梗死、脑梗死等严重不良反应,仅有肝酶、肌酸激酶等轻度升高,提示在脑梗塞二级预防中使用中等强化剂量的阿托伐他汀或瑞舒伐他汀能取得理想降脂效果,且兼具安全性。(2)他汀类药物能抑制黏附分子表达和细胞因子分泌,进而降低炎症因子浓度,减轻或消除血管炎症反应[15]。(3)他汀类药物可通过激活NO合成酶促进内皮细胞NO生成,进而发挥保护内皮细胞的作用。(4)他汀类药物能激发SOD活力,显著提升血管抗氧化能力,抑制氧化的LDL-C合成,进而延缓动脉粥样硬化病变。(5)他汀类药物能抑制基质金属蛋白酶活性,减少其分泌,进而抑制血管平滑肌细胞迁移增殖,实现稳定动脉硬化斑块的目的。(6)他汀类药物能有效抑制血小板活性,减少或延缓血栓形成,进而减轻动脉粥样硬化病变。(7)氯吡格雷是一种新型强效血小板抑制剂,可抑制血小板激活,并能竞争性抑制ADP所诱导的血小板聚集。它的抗血小板作用能抑制IFNc、ICAM-1等细胞因子与黏附分子的基因表达,同时还能抑制特定系统的炎症信号通路,抑制基质金属蛋白酶表达,减轻炎症反应,发挥抗动脉粥样硬化作用[16]。
经过治疗后,A、B两组患者的血脂指标、血液流变学指标均显著改善,提示在脑梗塞的二级预防中应用阿托伐他汀或瑞舒伐他汀联合氯吡格雷能降低血脂与血液流变学指标,并能抗血小板聚集,这对减少和防治缺血性脑血管事件有重要意义,同时也为脑梗塞的二级预防提供了更多治疗手段。
文献[17]中指出,服用他汀类药物后在体内出现的代谢产物、可能造成的肝功能损伤均可致血小板聚集率升高。阿托伐他汀是一种应用广泛的亲脂性他汀类药物,可与氯吡格雷竞争性结合CYP3A4进而影响激活,引发氯吡格雷抵抗,影响其抗血小板聚集作用。文献[18]中则发现氯吡格雷抵抗与他汀类药物代谢类型是否有差异无关,这可能与人体内存在多种代谢代偿机制有关。此次研究所选取对象均已排除初始静态下合并氯吡格雷抵抗者,治疗结果显示治疗1个月、3个月、6个月后A、B两组患者的血小板聚集率均较治疗前明显下降,但组间无明显差异,提示是否经CYP3A4代谢并不会影响抗血小板药物对于改善血小板聚集的作用,其原因主要与他汀类药物亦具有抗血小板聚集作用以及氯吡格雷因CYP3A4代谢途径受阻时可经其他酶代谢途径实现代偿有关。
既往研究证实他汀类药物可致横纹肌溶解,出现新发糖尿病、肝肾损害或认知功能损害等不良反应,其中肝毒性、肌肉毒性最为常见且程度较重。目前他汀类药物引发肝毒性的作用机制仍不明确,对于治疗前肝酶偏高者给予强化降脂治疗可使其恢复正常,但是否增加肝损伤风险仍需大样本、长时间研究以待证实。此次研究发现治疗期间A组仅出现肝酶升高1例,肌酶升高或肌肉疼痛2例;B组出现肝酶升高5例,肌酶升高或肌肉疼痛6例,A组不良反应发生率明显低于B组,结合既往研究并考虑此次研究样本量偏小等因素,可能提示20 mg瑞舒伐他汀不良反应的发生风险高于60 mg阿托伐他汀,尤其是肝毒性方面仍需进一步研究证实。研究还发现,两组患者均无肾功能损害(肌酐水平明显升高)或新发糖尿病等副作用,两组肝酶、肌酶升高幅度不大,肌肉疼痛症状均较轻微,提示阿托伐他汀在缺血性卒中二级预防中的安全性优于瑞舒伐他汀,但二者的远期预防效果相当,与既往研究结论一致[8]。
综上所述,阿托伐他汀或瑞舒伐他汀联合氯吡格雷用于脑梗塞的二级预防均能有效缩小颈动脉斑块面积,降低颈动脉内膜中层厚度,减轻动脉狭窄程度,改善血液流变学和血脂水平,二者疗效相当。在缩小颈动脉斑块面积方面,选用阿托伐他汀治疗获益更大,且安全性较好,临床上可结合患者自身耐受性和个体情况等因素合理选择应用。

