糖尿病自身抗体微阵列芯片检测试剂盒的研制与初步评价*
胡纪文,陈卓诚,张大准,段江磊,高 龙,林 珊,黄日雄,张秀明△
(1.广东省深圳市罗湖医院集团医学检验中心,广东深圳 518001;2.广东省深圳市伯劳特生物制品有限公司,广东深圳 518054)
1型糖尿病(T1DM)包括免疫介导和特发性两种亚型[1]。自身免疫性糖尿病(免疫介导型)是以胰岛β细胞自身免疫破坏为重要病因的一种疾病,患者体内存在一种或多种针对胰岛β细胞胰岛素合成、转运和分泌的关键酶的自身抗体,这些自身抗体在糖尿病的预测、诊断、分型及治疗方面具有重要意义[2-3]。本研究参照文献[4]建立微阵列芯片(Array-ELISA),用于联合检测T1DM组谷氨酸脱羧酶抗体(GADA)、酪氨酸磷酸酶抗体(IA-2A)、锌转运体8抗体(ZnT8A)、胰岛细胞抗体(ICA)、胰岛素抗体(IAA)5种抗体。研究报道如下。
1 资料与方法
1.1标本
1.1.1参考品血清标本来源与制备 本研究参考品原材料为不同阳性程度的血清标本和体检者血清标本,经乙型肝炎病毒抗原、丙型肝炎病毒抗体、艾滋病病毒抗体检测均为阴性,用斯德润(北京)医疗诊断用品有限公司生产的糖尿病自身抗体谱检测试剂盒[免疫印迹法(IBT)]检测,阳性参考品和精密度参考品按照检测结果选择合适的阳性血清标本混合,必要时可用阴性血清标本稀释。阴性参考品用阴性血清标本混合。
10份阳性参考品抗体型别包含GADA、IA-2A、ICA、ZnT8A、IAA,10份阴性参考品GADA、IA-2A、ICA、ZnT8A、IAA抗体全部为阴性。2份精密度参考品为R1(GADA/IA-2A/ICA/ZnT8A/IAA)、R2(GADA/IA-2A/ICA/ZnT8A/IAA)。检测限参考品1系列用于对GADA、IA-2A、ZnT8A的最低检测限评价,2系列用于对ICA和IAA的最低检测限评价。检测限参考品L3为混合阳性血清标本,必要时可用阴性血清标本稀释,其相应抗体阳性指数(PI)范围为1.8~2.4;L3用阴性血清标本稀释1倍后得到对应的L2,其相应抗体PI范围为0.9~1.2;L2用阴性血清标本稀释1倍后得到对应的L1,其相应抗体PI范围为0.4~0.6。
1.1.2临床比对血清来源 选取2018年1月至2019年12月在深圳市罗湖区人民医院和罗湖区中医院门诊就诊的T1DM患者的42份血清作为T1DM组,另选取同期在罗湖区中医院门诊就诊的2型糖尿病(T2DM)患者的30份血清、体检健康者的54份血清分别作为T2DM组、对照组。
1.2仪器和试剂
1.2.2试剂及试剂盒 96孔板(Biomat公司);GAD65抗原/IA-2抗原(菲鹏生物);ICA抗原/ZnT8抗原(北京华信行公司);insulin抗原(Lee Biosolutions,Inc.);人IgG(Equitech-Bio,Inc.);兔抗人IgG(Jackson ImmunoResearch Inc.);抗人IgG-HRP(百美瑞生物);HRP结合物稳定剂(Surmodics,Inc.);The Blocking Solution/Liquid Plate Seal(Candor Bioscience);TMB沉淀型底物(英创生物);其它化学试剂均为AR级。斯德润(北京)医疗诊断用品有限公司生产的糖尿病自身抗体谱检测试剂盒(IBT),批号:010306D/0A。
1.3方法
1.3.1Array-ELISA设计 按照图1模式图的布局进行Array-ELISA设计,PR点为位置参考点,PC点为阳性对照点,NC点为阴性对照点,CO点为临界值对照点,SC点为标本对照点,GAD、IA2、ICA、ZnT8、INS分别为抗原点。
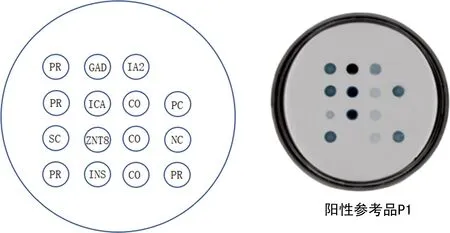
图1 糖尿病自身抗原Array-ELISA模式和实物图
1.3.296孔Array-ELISA制备 上述各芯片点点样液配制,用PBS(0.01 mol/L PBS,含15%甘油、10%海藻糖,pH值7.2)配制40 μg/mL的GAD抗原、60 μg/mL的IA-2抗原、10 μg/mL的ICA抗原,用Tris(0.02 mol/L Tris,含15%甘油、10%海藻糖,pH值8.5)配制20 μg/mL的ZnT8抗原,用CB(0.05 mol/L CB,含15%甘油、10%海藻糖,pH值9.6)配制80 μg/mL 的INS抗原、2 μg/mL的RAH作SC点、2 μg/mL的IgG作PR及PC点、0.12 μg/mL的IgG作CO点、0.05 μg/mL的IgG作NC点。使用BioDot AD6020芯片点样仪按照图1模式以每点20 nL在96孔板底部点样,点样结束后放入冰箱(2~8 ℃)固定16 h。次日洗板2次,加入2%的酪蛋白室温封闭1 h,吸干封闭液,在37 ℃烘箱中干燥2 h。密封后置于4 ℃保存待用。
1.3.3检测试验 96孔Array-ELISA平衡至室温后,用Tris样品稀释液稀释血清26倍,取稀释液100 μL加入反应孔中,室温反应60 min;洗涤3次;将0.3 mg/mL的抗人IgG抗体稀释2 000倍,每孔加入50 μL,室温反应30 min;洗涤液3次;每孔加入TMB芯片底物50 μL,室温反应30 min,吸取底物后,将96孔芯片放入生物芯片阅读仪,用DM-5Abs程序进行扫描判读,软件统计各抗体的PI,PI≥1.0为阳性,PI<1.0为阴性。
1.3.4性能评价
1.3.4.1符合率 检测10份阳性参考品和10份阴性参考品PI值结果,计算符合率。
1.3.4.2重复性 分别检测R1、R2批内10次PI值结果,计算变异系数(CV)值。
本项目系统地研究了一系列可适用于野外现场分析的快速、简单、高效的样品分离富集前处理技术与便携式钨丝电热原子吸收光谱仪联用,在一定程度上提高该仪器的分析性能,对于推动该仪器走向现场快速分析起到了较为积极的作用,同时通过这些研究工作也进一步加强了新型分离富集技术及其与钨丝电热原子吸收光谱法、火焰原子吸收光谱法乃至分光光度法联用方面的理论和应用研究。
1.3.4.3最低检出限 L1相应抗体检测结果应为阴性,L2相应抗体检测结果可为阴性或者阳性,L3相应抗体检测结果应为阳性。
1.3.5临床应用评价 以Array-ELISA为试验方法,糖尿病自身抗体谱检测试剂盒(IBT)为比对方法,同步检测3组血清标本,计算各抗体阳性符合率、阴性符合率、总符合率,Kappa值。以总符合率大于90.00%为符合率可接受的标准,Kappa值>0.75,P>0.05时为一致性较好。根据检测结果,统计灵敏度、特异度,评价方法的临床适用性。
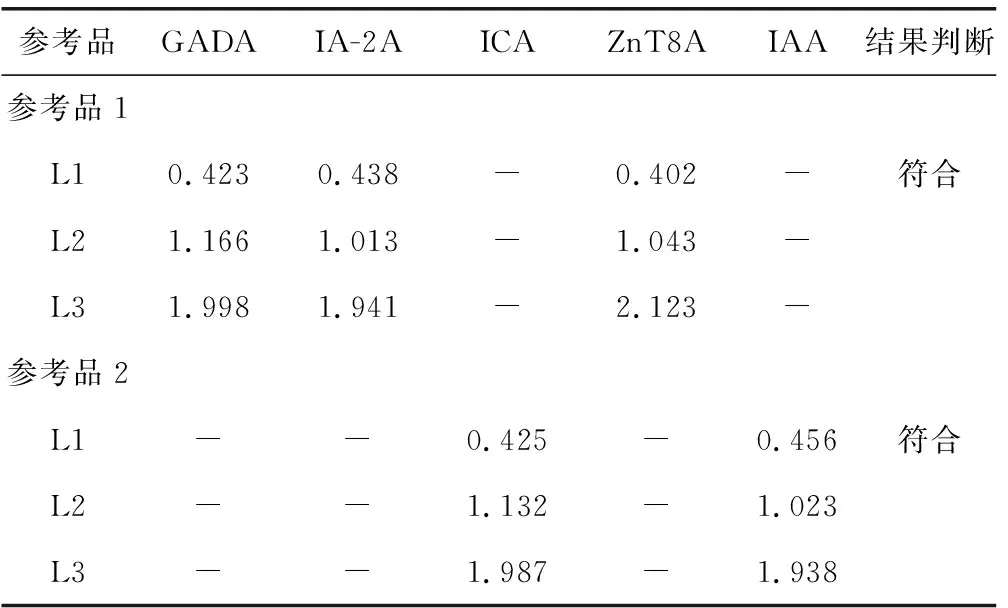
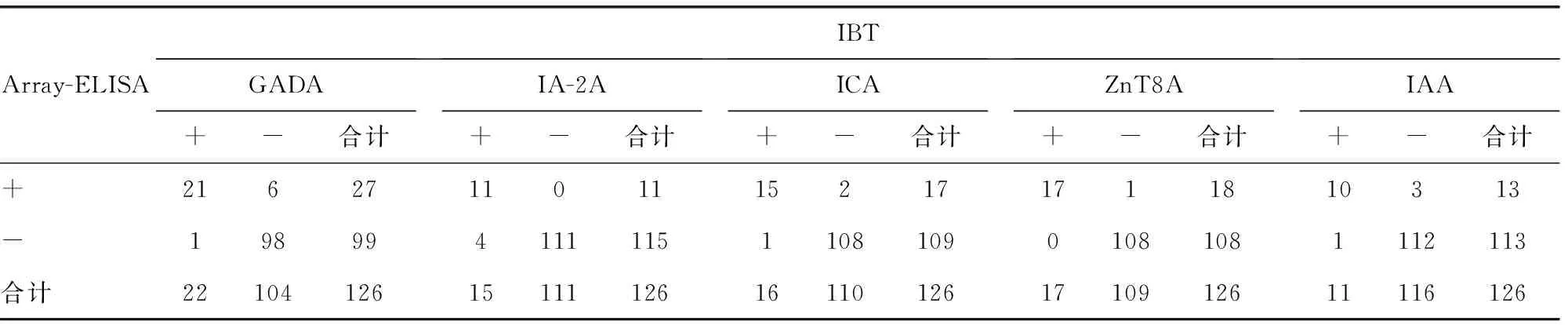
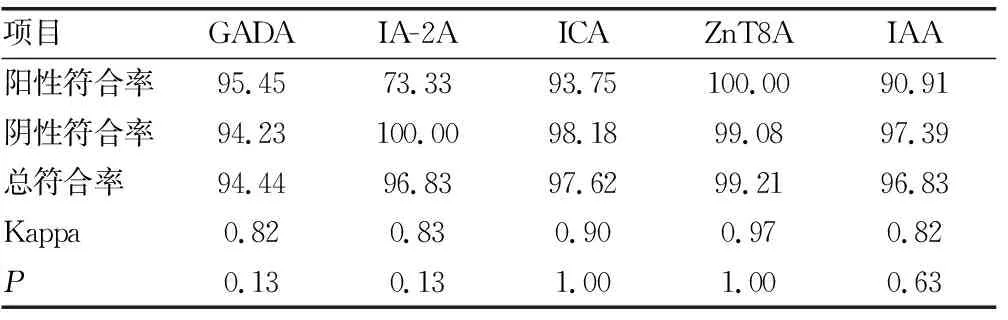
1.3.6统计学处理 采用SPSS22.0软件进行数据统计和分析。一致性分析采用Kappa一致性检验,0.0≤Kappa≤0.2为微弱一致性,0.2 2.1阳性参考品符合率 试验结果显示10份阳性参考品检测均为阳性,符合率为100.00%。 2.2阴性参考品符合率 试验结果显示10份阴性参考品检测均为阴性,符合率为100.00%。 2.3重复性检测 试验结果显示,样品各抗原的批内重复性CV均小于15.00%。 2.4最低检测限检测 分别用检测限参考品1系列、2系列进行5种糖尿病自身抗体检测,各抗体PI结果显示,L1均为阴性,L2、L3均为阳性。见表1。 2.5方法学比较 采用Array-ELISA与IBT法同步检测T1DM组、T2DM组和对照组血清标本,GADA阳性符合率95.45%,阴性符合率94.23%,总符合率94.44%;IA-2A阳性符合率73.33%,阴性符合率100.00%,总符合率96.83%;ICA阳性符合率93.75%,阴性符合率98.18%,总符合率97.62%;ZnT8A阳性符合率100.00%,阴性符合率99.08%,总符合率99.21%;IAA阳性符合率90.91%,阴性符合率97.39%,总符合率96.83%。5种抗体的总符合率均大于90.00%。5种抗体Kappa值统计均大于0.75,P值均大于0.05,两种检测方法具有高度的一致性。见表2、3。 表1 最低检测限检测结果(PI) 表2 Array-ELISA与IBT法检测血清5种抗体结果(n) 表3 Array-ELISA与IBT法检测血清5种抗体结果一致性比较(%) 2.6临床应用评价 使用本研究所建立的糖尿病自身抗体Array-ELISA检测试剂盒对3组血清5种抗体进行检测,T1DM组5种抗体的阳性率高于T2DM组及对照组,差异有统计学意义(P<0.05),见表4。Array-ELISA检测T1DM 5种抗体的灵敏度除GADA为59.52%较高外,其余4种自身抗体指标的灵敏度均低于50.00%。但5种抗体联合检测T1DM的灵敏度达88.10%,特异度为90.70%,见表5。 表4 Array-ELISA检测3组血清5种抗体的结果[ n(%)] 表5 Array-ELISA检测T1DM 5种自身抗体的效果评价(%) 在T1DM发病前、发病早期和发病后会产生许多自身抗体,直到目前为止,与T1DM相关的自身抗体仍不断被发现。通过大量的研究,人们已经清楚地认识到,要确切地诊断T1DM,仅一种自身抗体指标的预测能力是非常有限的。研究表明,联合多种抗体测定可提高胰岛自身抗体的检出率[5]。谢志国等[6]报道,在新诊断的T1DM患者中,单独检测GADA阳性率为70.2%(144/205);联合检测GADA+IA-2A,任一抗体阳性者166例,阳性率提高至81.0%(与GADA单独检测相比,P<0.05);在检测GADA和IA-2A的基础上,进一步联合检测ZnT8A,任一抗体阳性者为170例,阳性率进一步提高至82.9%,但与 GADA+IA-2A联合检测相比,阳性率差异无统计学意义(P>0.05)。研制并应用可实现多种胰岛自身抗体联合检测的方法有重要的临床意义,可减少T1DM尤其是临床特征不典型的T1DM患者的漏诊[7]。本研究研制的糖尿病自身抗体检测试剂盒Array-ELISA可同时检测ICA、IAA、GADA、IA-2A和ZnT8A 5种抗体,对42例临床确诊T1DM患者血清标本进行检测,5种抗体联合检测的灵敏度为88.10%,特异度为90.70%,阳性检测结果可以有效鉴别诊断T1DM,指导临床精准治疗。 糖尿病自身抗体的测定方法主要包括免疫组化法、放射免疫分析法(RIA)、ELISA、IBT、化学发光法(CLIA)、放射配体分析法(RBA)等。其中免疫组化法具有准确度高、特异度强、重复性好且直观的特点,但由于操作繁琐耗时已逐渐被ELISA替代。RIA是一种十分经典的方法,较早应用于胰岛自身抗体的测定,具有较高的灵敏度和特异度,但是由于存在放射性污染,目前临床已经很少使用。ELISA是应用较成熟的一种方法,可得到较可靠的结果,但利用该法进行多指标联合测定则存在检测费时、报告周期较长等不足。IBT结合了聚丙烯酰凝胶电泳的高分辨率和免疫标记技术的高特异度及灵敏度的优点,近年来开始应用于胰岛自身抗体的测定,该方法简便,可一次同时测定几种自身抗体,其特异度好,但灵敏度也有待提高[8-9]。CLIA是近年发展起来的检验方法之一,具有高通量、高特异度及灵敏度、检测速度快等优点,但一次只能检测一个抗体。多年来的标准化工作证实,RBA因其灵敏度和特异度高,结果重现性好,检测线性范围宽,被欧美发达国家认定为胰岛自身抗体检测的参考方法(金标准)[10],但该方法操作复杂,检测步骤多,影响因素多,并不适合临床检测。因此,发展准确快速、灵敏特异、并可以同时测定多指标的新技术和新方法非常必需。本研究研制的糖尿病自身抗体检测试剂盒Array-ELISA与IBT相比,两种方法均可以检测5种自身抗体,同时对临床标本进行检测,5种自身抗体的总符合率均在90.00%以上,Kappa值均大于0.75,两种方法具有高度一致性。 目前有部分检测试剂可以在诊断DM基础上初步分型,如英国RSR(GADA、IA-2A、ZnT8A)免疫放射IRMA试剂盒、德国MedipanGmbh(GADA、IA-2A)ELISA检测试剂盒、美国Biomerica(GADA、IAA、ICA)ELISA检测试剂盒,国内深圳市伯劳特公司糖尿病分型试剂盒(IBT法)、深圳赛尔(GADA、IAA、ICA)ELISA检测试剂盒、斯德润(北京)医疗诊断用品有限公司生产的糖尿病自身抗体谱检测试剂盒。相比于现有试剂盒,本研究制备的试剂盒采用Array-ELISA技术,应用标准96孔板作为固相,兼容各种酶标洗板机及自动酶免分析系统,解决了手工操作印迹膜条的操作复杂、重复性差、均一性差等问题,同时又具有高通量的特点。检测结果由生物芯片阅读仪自动判读,检测结果客观,避免人工肉眼判断的主观性,更加适用于临床上对糖尿病自身抗体的检测,有效辅助糖尿病的分型诊断,从而实现T1DM患者的早期正确诊断。2 结 果


3 讨 论

