腹腔镜技术在T1b和T2期胆囊癌根治术中的安全性及有效性研究
高 伟,李 涛,席 锐
陕西省汉中市中心医院肝胆外科,陕西汉中 723000
胆囊癌是胆道系统恶性程度最高的肿瘤,早期诊断困难,5年生存率低,文献报道为5%~14%[1-2]。尽管新辅助放化疗对提高胆囊癌的疗效起到一定的作用,但对部分患者行根治性手术切除仍是提高其长期生存率的唯一手段。随着手术技术的提高及腹腔镜学习曲线的完成,腹腔镜技术在消化道肿瘤治疗中的安全性及有效性已得到认可[3-5]。由于胆囊癌根治术涉及肝切除、淋巴结清扫及肝外胆道的处理,腹腔镜技术能否像在胃癌、结直肠癌中取得类似甚至优于开腹手术的治疗效果尚存在争议。本文以美国癌症联合委员会(AJCC)第7版胆囊癌分期系统为基础,回顾性分析本院2013年9月至2016年9月诊断为T1b和T2期胆囊癌患者的临床资料,评估腹腔镜根治术与开腹根治术的手术安全性,1年及3年生存率有无差异。
1 资料与方法
1.1一般资料 选择2013年9月至2016年9月本院收治的T1b期和T2期胆囊癌患者72例为研究对象,根据手术方式将患者分为两组,腹腔镜组(n=33)和开腹手术组(n=39)。腹腔镜组中男12例,女21例;年龄36~72岁,平均(45.00±10.60)岁;既往病史:胆囊息肉7例,胆囊腺肌症10例,胆囊结石伴慢性胆囊炎6例,胆囊结石合并急性胆囊炎10例。开腹手术组中男15例,女24例;年龄39~70岁,平均(48.00±9.00)岁;既往病史:胆囊息肉9例,胆囊腺肌症12例,胆囊结石伴慢性胆囊炎10例,胆囊结石合并急性胆囊炎8例。两组患者性别、年龄、既往病史等一般资料比较,差异均无统计学意义(P>0.05)。
1.2纳入及排除标准 纳入标准:术前增强MRI检查提示胆囊癌侵犯浆膜,术中胆囊癌组织经冰冻切片活检证实,术中通过超声检查证实为胆囊癌,所有病例最终经术后石蜡切片证实为T1b和T2期的胆囊癌患者。排除标准:术中诊断为T1b和T2期胆囊癌,家属拒绝行根治术,仅行胆囊切除术者;术中发现已有远处转移不适宜行根治术者;术后因非肿瘤性原因死亡者;术后随访资料不全者。
1.3方法
1.3.1手术方式 常规消毒铺巾,腹腔镜组行腹腔镜胆囊癌切除术,建立CO2气腹,术中注意避免胆囊破裂,术中超声再次确认胆囊癌分期后,采用四孔法置入腹腔镜设备,分离腹腔内粘连,依次探查腹腔、盆腔各脏器有无转移灶,重点探查腹腔干、肠系膜根部及腹主动脉旁淋巴结有无转移。肝切除的范围:常规行胆囊及胆囊床周围2 cm的肝脏契型切除,如果肿瘤浸润肝脏深度超过2 cm,则行肝S4b+S5切除;如肿瘤浸润过深,行右半肝及右三叶切除以保证切缘阴性;对于T2期和淋巴结转移的患者需进行淋巴结清扫,淋巴结清扫范围:清扫肝十二指肠韧带、肝总动脉、胰头周围淋巴结,如术中肝总动脉、胰头周围淋巴结活检阳性,则扩大清扫腹腔干周围淋巴结;肝外胆道的处理:不常规切除肝外胆管,仅在肝外胆管受侵犯无法获得切缘阴性或区域淋巴结与肝外胆管致密粘连无法分离者做肝外胆管切除+胆管空场吻合术。术后常规于Winslow孔处放置腹腔引流管一根。开腹手术组行开腹手术胆囊癌根治术,右上腹肋缘下斜切口长约15 cm,探查范围、切除区域以及清扫淋巴结同腹腔镜组,术后肝断面常规放置导管引流。
1.3.2观察指标及随访 (1)手术情况:观察并记录两组患者的手术时间、术中出血量、术后住院时间及住院费用。(2)术后并发症情况:采用Clavien-DIndo分级对两组患者术后并发症进行分级,Clavien-DIndoⅠ级:在未经任何特殊干预的前提下,发现微小吻合口漏或引流液性质异常或吻合口周围置管时间>7 d,但无明显的临床表现;Clavien-DIndoⅡ级:需要特殊干预(抗菌药物或完全肠外营养时间>7 d);Clavien-DIndoⅢ级:应行穿刺或在全麻下进行冲洗、引流、造口或重新吻合[6-8]。(3)术后生存率:术后随访时间3年,每6个月对患者定期门诊检查和电话随访,了解患者的术后生存情况。

2 结 果
2.1两组手术情况对比 腹腔镜组患者的手术时间、术中出血量、术后住院时间、住院费用显著短于或少于开腹组,差异有统计学意义(P<0.05),见表1。

表1 两组手术情况对比
2.2两组并发症发生情况对比 与开腹手术组相比,腹腔镜组术后Clavien-DIndoⅢ级并发症的例数更少,差异有统计学意义(P<0.05)。见表2。
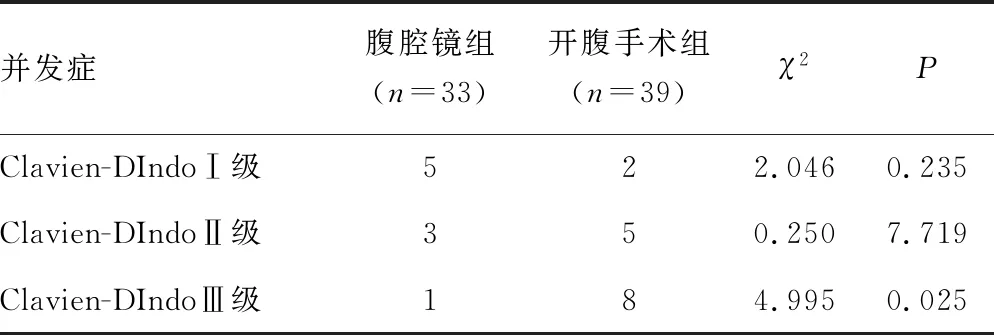
表2 两组并发症发生情况对比(n)
2.3两组术后生存率对比 开腹组患者术后1年、3年生存率分别为 82.1%和48.7%,腹腔镜组分别为84.8%和57.6%,组间比较差异无统计学意义(P<0.05),见图1。

图1 两组患者生存曲线对比
3 讨 论
胆囊癌根治术是胆囊癌患者唯一可获得长期生存的治疗方式,但这一术式涉及肝切除、淋巴结清扫及胆肠重建多种技术,手术操作复杂,预后较差。早期的研究认为胆囊癌根治术不宜使用腹腔镜,尤其是对腹腔镜下胆囊破裂、胆汁外流所致穿刺孔及腹膜腔的肿瘤种植的担忧更是限制了腹腔镜技术在这一疾病中的应用,或是因为行腹腔镜手术前气腹可能会导致患者术后免疫力降低,从而使腹腔内恶性肿瘤细胞扩散增加或者转移扩散[9-10]。手术仍是目前治疗胆囊癌最有效的治疗手段,近年来腹腔镜手术在消化道肿瘤尤其是在结直肠癌、胃癌中取得与开腹手术相似的疗效,已被广泛应用于可行腹腔镜胆囊癌根治术患者的治疗中,临床疗效较好,安全性较高,受到了临床医生的认可,且已逐渐地取代了传统的开腹手术,已成为胆囊相关疾病的首选治疗方式[11]。关于T1b和T2期胆囊癌是否应行腹腔镜手术存在争议,但是研究发现对于T1b和T2期胆囊癌患者行胆囊癌根治术可以显著提高患者生存率[12]。因此,本研选取了T1b期和T2期患者,采用腹腔镜技术进行胆囊癌根治术以探讨其安全性和有效性。
胆囊癌根治术手术范围的选择应该根据病理分期进行,同时术前增强MRI,术中超声等影像学检查对于胆囊癌的确诊和分期均有一定的辅助作用,当术前诊断不明确时,可以根据术中快速冰冻病理检查或者术后常规病理检查再次进行确证以决定是否进行胆囊癌根治手术。目前,腹腔镜技术在T1b和T2期胆囊癌根治术的治疗中取得了与开腹胆囊根治术相同甚至更好的疗效,也是目前治疗胆囊癌最有效的治疗方式,不仅能够彻底清除恶性组织,而且延长了患者的生存时间,为患者提供了可能治愈的机会。本研究选取了T1b期和T2期胆囊癌患者分别进行腹腔镜胆囊癌根治术和开腹手术,对两种术式进行对比分析,结果显示:腹腔镜组患者的手术时间、术中出血量、术后住院时间、住院费用显著短于或少于对照组;腹腔镜组术后Clavien-DIndoⅢ级并发症的例数更少。说明腹腔镜胆囊癌根治能够有效缩短手术时间和患者住院时间,减少术中出血量,不增加术后并发症的发生率,从而降低患者住院费用。徐益萍等[13]报道的腹腔镜胆囊癌根治术能够有效改善患者手术相关指标,主要包括手术时间、术中出血量以及并发症的发生率,术后随访3年患者生存率明显较高。
腹腔镜胆囊癌根治术是否能取得与开腹胆囊癌根治术一样的远期生存率是腹腔镜技术能否应用及推广的最大问题。本研究结果显示,开腹组患者术后1年、3年生存率分别为 82.1%和48.7%,腹腔镜组分别为84.8% 和57.6%,组间比较,差异均无统计学差异(P<0.05 )。张成等[14]对两组患者分别采用腹腔镜胆囊癌根治术和开腹胆囊癌根治术,术后发现两组患者1年、3年和5年的生存率差异均无统计学意义。分析这一结果可能的原因:(1)本研究样本量较少。(2)可能与肿瘤所在位置有关,一项多中心研究统计了252例T2期的胆囊癌患者的临床资料发现,99例肿瘤位于肝脏面的患者无论是血管侵犯、神经浸润还是淋巴结转移率都要高于肿瘤位于腹腔面,两组患者3年、5年生存率分别为52.1%vs. 73.7%,42.6%vs. 64.7%,差异有统计学意义(P<0.05)[15]。由于本研究中样本量有限,而且临床上影响胆囊癌根治术术后疗效的因素较多,因此将在下一步研究中进一步扩大样本量,收集患者临床资料,分析影响胆囊癌患者生存率和临床疗效的相关因素。
综上所述,腹腔镜技术在胆囊癌根治术中是安全、有效的,能够有效缩短手术时间和患者术后住院时间,减少术中出血量,不增加术后并发症的发生率,降低患者住院费用,术后1年、3年患者生存率与开腹胆囊癌根治术基本一致。

