68例新型冠状病毒肺炎患者治疗药品不良反应分析
李冬艳,张锦文
(华中科技大学同济医学院附属同济医院药学部,武汉 430030)
自新型冠状病毒肺炎(coronavirus disease 2019,COVID-19)疫情发生至今,我国先后制定更新了七版《新型冠状病毒肺炎诊疗方案》[1]。在对新型冠状病毒认识不足、缺乏有效治疗药物的疫情阶段,诊疗方案推荐了多个试用药物。药品具有双重性,既可以起到治疗疾病的作用,又可能产生药品不良反应(adverse drug reaction,ADR)。ADR是临床患者主要死因之一,目前已成为医药护共同关注的重要问题[2]。合理评价分析药物不良反应,提高不良反应的信息利用度,有利于发挥药品不良反应监测促进临床合理用药的作用。本文对华中科技大学同济医学院附属同济医院(简称同济医院)2020年2月—5月上报的COVID-19患者治疗药物ADR报告进行回顾性分析,总结COVID-19患者治疗药物ADR发生的特点,为临床用药提供参考。
1 资料与方法
1.1资料来源 资料来源于同济医院不良反应监测办公室收集的2020年2—5月的68例COVID-19患者治疗药物ADR报告表。数据纳入标准:①新冠肺炎确诊或疑似病例;②药品名称、ADR名称、性别、年龄、ADR发生时间、处置及转归等相关信息清晰明确;③ADR关联性评价为可能、很可能或肯定。数据排除标准:重复报告、待评价、无法评价及ADR评价可能无关的数据。
1.2标准 ①新的和严重ADR标准:根据2011年中华人民共和国卫生部令第81号《药品不良反应报告和监测管理办法》,新的药品不良反应是指药品说明书中未载明的不良反应,药品严重ADR是指因服用药品引起以下损害情形之一的反应:引起死亡;致癌、致畸、致出生缺陷;对生命有危险并能够导致人体永久的或显著的伤残;对器官功能产生永久损伤;导致住院或住院时间延长;导致其他重要医学事件,如不进行治疗可能出现上述所列情况的。
②超说明书用药标准:根据国家药品监督管理局批准的最新版药品说明书,从适应证、单次剂量、给药频次、给药途径、溶媒、用药人群及相互作用等方面,对每份 ADR 报告的每条医嘱逐条判断其是否与说明书相符,若一种药物根据适应证或疾病严重程度有不同的给药剂量,则以最高的给药剂量为准,若不相符则判断为超说明书用药,如同一条用药医嘱中存在多个超说明书用药类型均做记录[3]。
1.3方法 回顾性分析68例COVID-19患者治疗药物的ADR报告,按照国家药品不良反应监测中心的《药品不良反应报告和工作手册》[4]中的药品不良反应/事件报告表内容、严重ADR的标准、关联性评价的五个原则(有无合理的时间关系、是否符合药物已知的ADR类型、停药或减量后症状是否消失或减轻、再次使用是否出现同样的反应事件、反应事件是否可用并用药作用、病情进展及其他治疗的影响来解释),运用Excel对ADR报告中患者性别、年龄、药品种类、ADR类型、发生时间、累及器官和(或)系统及主要临床表现、转归及关联性评价(肯定、很可能、可能、可能无关、待评价、难以评价)等信息进行统计分析。
2 结果
2.1ADR报告类型分布 一般的ADR 42例,占61.76%,新的一般的ADR 7例,占10.29%。严重的ADR 26例,占38.24%,新的严重的ADR 2例,占2.94%,新的/严重的35例,占总ADR的51.47%。
2.2发生ADR患者性别与年龄分布 男29例,占42.65%,女39例,占57.35%;年龄31~84岁,平均年龄为57.5岁,61~80岁38例,占总ADR的55.88%(表1)。

表1 ADR患者年龄、性别分布
2.3ADR给药途径、联合用药和发生时间 给药途径最多见口服给药(73.53%),余为静脉给药(23.53%)、鼻饲给药(1.47%)和雾化吸入给药(1.47%)。7例存在联合用药,其中包括两种中药联用1例,中西药联用1例,两种抗病毒药物联用2例,抗病毒药物与糖皮质激素联用1例,糖皮质激素与抗生素联用1例,保肝药与降压药联用1例。68例ADR病例均为首次用药即发生不良反应,发生在用药后1 h以内1例,占1.47%,用药1 h~1 d发生ADR 23例,52.94%患者ADR发生在用药1~7 d,见表2。
2.4ADR大于2例的药品品种与主要临床表现 涉及ADR大于2例的药品共8种,抗病毒药物居首位,其次为免疫抑制剂和抗感染药物。ADR的临床表现以胃肠道不适、肝功能异常等消化系统损害为主,见表3。

表2 ADR发生时间
2.5引起严重ADR的药品品种与主要临床表现 对26例严重ADR涉及到的药品进行统计,位于前5位的分别是硫酸羟氯喹片5例(19.23%)、托珠单抗注射液3例(11.54%)、洛匹那韦/利托那韦片2例(7.69%)、盐酸莫西沙星氯化钠注射液2例(7.69%)及注射用硫酸多粘菌素B 2例(7.69%),共涉及药物品种16种。严重ADR临床表现以肝功能异常(7例)、血液系统异常(6例)为主,见表4。
2.6ADR累及器官/系统及临床表现 68例ADR报告中,累积器官或系统合计80例次,消化系统损害最多,共37 例(46.25%),主要表现为恶心、呕吐等,其次为皮肤损害,共17例(21.25%),主要表现为皮肤发黑、皮疹(红斑疹、荨麻疹),见表5。
2.7ADR涉及的药品超说明书用药情况 发生ADR的超说明书用药涉及的药品、占比及超说明书用药类型见表6。68例不良反应报告中,36例(52.94%)存在超说明书用药,发生ADR的患者用药均存在超适应证用药,硫酸羟氯喹还存在超剂量使用的情况。
2.8ADR处理、转归及关联性评价 68例中,35例(51.47%)停药并经抗过敏、护胃、抑酸、护肝、升白细胞、止泻、菌群调节等对症治疗后好转;27例(39.71%)仅停药出现好转;2例(2.94%)未停药出现好转;2例(2.94%)未停药,分别经护肝、抗过敏治疗后好转;1例(1.47%)减量并予以护胃对症处理后好转;1例(1.47%)未停药,结果不详。根据国家药品不良反应监测中心使用的Karch和Lasagna评价方法[5-6]对ADR进行因果关系评价,很可能43例(63.24%),可能25例(36.76%),肯定0例。
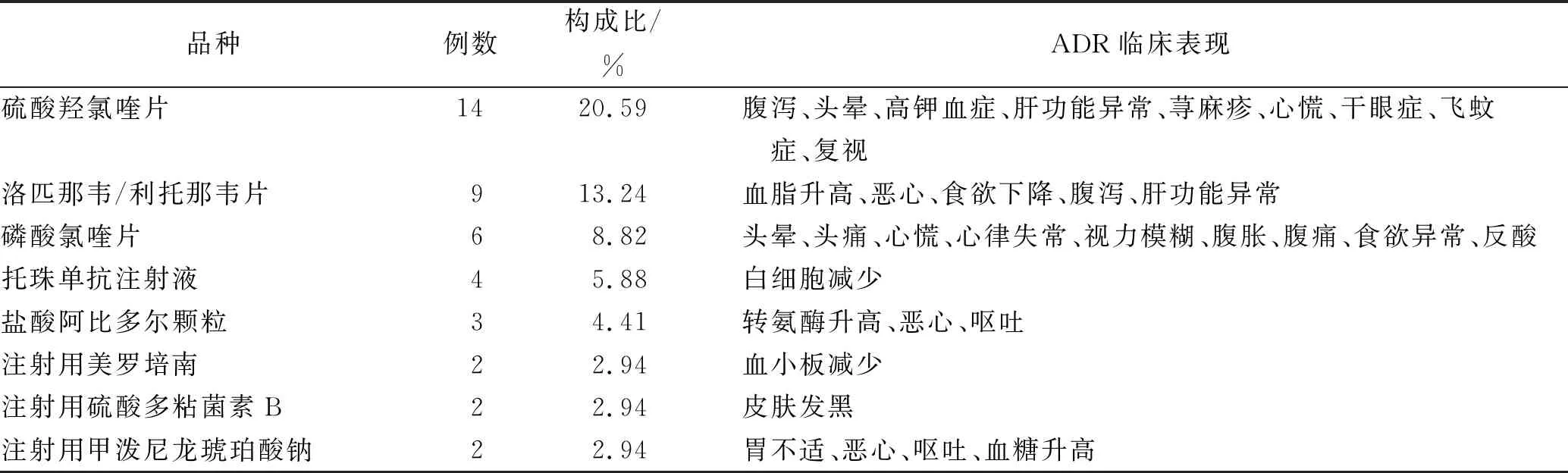
表3 8种ADR大于2例的药品及主要临床表现

表4 严重的ADR涉及药品及临床表现

表5 ADR累及的器官或系统分布和临床表现

表6 ADR涉及的超说明书用药的药品及类型
3 讨论
3.1重视新的和严重ADR的监测 依据世界卫生组织发布的《药品不良反应监测和报告指南》,若通过多份报告发现病例报告事件与某药品之间有必然联系,且是先前未知或未被描述过的,那么便获得了一个有效“信号”,ADR信号的获得取决于AE的严重程度和报告中所含信息的质量。由此可见,新的和严重的报告是有效预警信号的来源。因此,新的和严重的ADR是药品ADR监测的重点,其比例是衡量ADR报告质量和可利用性的一个重要指标[7]。2020年2—5月,我院COVID-19患者共上报不良反应68例,其中新的ADR报告9例,比例为13.24%;严重的(包括严重的、新的严重的) 报告26例,比例达到总ADR报表数的38.24%,比我院非疫情时期上报的新的/严重的不良反应比例大幅度增加,这主要与疫情期间我院ADR监测模式及疾病治疗药物有关。一方面,COVID-19疫情期间我院ADR监测除自主呈报方式外,临床药师还对有潜在风险的药物进行了重点监测,发挥了其专业敏感性,也更加关注新的和严重的ADR的监测。另一方面,COVID-19作为一种新发传染病,暴发初期其发展进程相当迅猛,对其发病机制缺乏充分的了解,进行防治时缺乏针对性的抗病毒治疗药物,不可避免地存在超说明书用药现象。一项研究表明,超说明书用药与ADR的发生率有关,超说明书用药的ADR发生率远高于按说明书用药[8]。由表6可以看出,总的不良反应病例中,一半以上(52.94%)的病例存在超说明书用药。因此,超说明书用药的潜在风险可能是新的严重的ADR发生的不容忽视的原因。当临床治疗需要超说明书用药时,应权衡患者治疗风险与获益,并进行ADR的严密监测,尤其重视新的和严重的ADR监测。
3.2严重ADR涉及的药品种类及临床表现 如表3所示,我院此次的ADR报告中严重ADR共涉及16种药物,硫酸羟氯喹片ADR发生比例最高(20.59%)。表5显示硫酸羟氯喹致5例严重ADR,其中包括1例出现严重胃肠道反应。国家卫生健康委员会发布的各版《新型冠状病毒肺炎诊疗方案》均未推荐羟氯喹的使用。虽然目前羟氯喹对新冠肺炎的疗效及安全性尚未得到一致的结论,但我院的ADR监测结果提示临床应尽可能避免使用疗效及安全性未经证实的治疗药物(包括适应证、用法、用量等)。此外,因皮肤与胃肠道系统的临床表现较为直观、容易被发现,而肝、肾、血液系统等损害需要进行相关的实验室检查方可确定[9]。我院此次监测到的严重ADR临床表现以肝功能异常、血液系统异常为主,提示临床医师使用这些药物时需注意密切监测相关实验室指标,降低用药风险。
3.3重视老年人ADR监测 由表1可知,我院收集的68例COVID-19患者ADR报告中,发生ADR最多的年龄段为61~80岁,占总ADR的55.88%,这与文献[10]报道的老年人用药ADR的构成比是一致的。一方面,老年患者和有基础疾病的COVID-19患者相对年轻人预后不良[1],病情危重的患者中老年患者数量相对较多,我院为COVID-19重症患者定点医院,因此接诊的老年患者数量较多,发生ADR的老年患者比例较大。另一方面,中老年人ADR发生率高与中老年患者基础疾病较多,病情复杂,用药品种较多,肝肾功能降低,药物消除减慢相关[11]。因此,提示临床医师对于老年人的药物治疗需格外谨慎,须详细了解患者既往病史、过敏史、用药史,结合患者实际制定个体化方案,同时加强用药监测,减少ADR的发生。
由于药物的双重性,药物的ADR不可避免,同时ADR的发生也与多种因素有关,但合理用药是一种减少ADR发生的有效手段。通过对我院2020年2—5月COVID-19患者ADR报告的分析,提示临床用药应严格把握适应证和用法用量,超说明书用药应特别加强ADR监测,详细询问患者既往用药史及不良反应史,同时要注意加强对老年人的用药监护,根据患者的病情制定个体化用药方案。此外,ADR的监测模式可多种方式相结合,此次我院临床药师参与临床实践,重点监测有潜在风险的超说明书用药,从而及早发现ADR尤其是严重的和新的ADR并反馈给临床,最大限度地减少、避免类似ADR再次发生,促进临床合理用药。

