微波消融联合经皮椎体成形术治疗椎体转移性肿瘤的疗效观察
杨 威,胡婷业,陆玉和,王 凯,张劲松,夏 磊,周晓星,曹惠玲,张珊珊
随着肿瘤治疗技术的不断提高,患者的预期寿命延长,使得转移性肿瘤的发病率明显提高,骨骼是继肺部和肝脏之后第三常见转移部位[1],而椎体是骨转移最好发的部位[2]。肿瘤转移常见于胸椎、腰椎和颈椎。 经皮椎体成形术(percutaneous vertebroplasty,PVP)是一种微创介入治疗方法,经过20 余年的发展已经成为治疗椎体血管瘤、骨质疏松性椎体压缩性骨折和椎体恶性肿瘤的可靠方法。 PVP 治疗椎体转移性肿瘤可迅速缓解患者的疼痛,加固病变椎体并防止其进一步塌陷[3],因不能控制肿瘤的生长[4],常联合其它治疗方法,如联合125I 粒子[5]、射频消融(RFA)[6-9]等,来提高治疗效果。 我院自 2017年1月以来,将微波消融(microwave ablation,MWA)联合PVP 术治疗椎体转移性肿瘤40 例,取得较好的临床效果,现报道如下。
1 材料与方法
1.1 材料
1.1.1 临床资料 2017年1月 1 日至 2019年1月31 日在我科住院治疗的椎体转移性肿瘤患者80例,随机分为对照组和研究组各40 例,对照组40例患者48 节椎体,研究组40 例患者45 节椎体,对照组采用PVP 术,研究组采用MWA 联合PVP 术,两组患者的年龄、性别、原发肿瘤见表1。

表1 两组椎体转移性肿瘤患者一般临床资料比较
1.1.2 纳入标准 ①椎外明确的恶性肿瘤病史;②预期生存期>6 个月;③CT 显示为溶骨型和混合型(溶骨型和成骨型)病变,椎体后缘完整;④MRI 显示骨破坏区T1 加权像为低信号的肿瘤组织,T2 加权像为高信号;⑤有明显的神经根压迫症状和体征;⑥患者神志清楚,有正常的沟通能力。
1.1.3 排除标准 ①经CT、MRI 诊断或病理学确诊椎体转移性肿瘤,但无神经根压迫症状;②曾使用大剂量放疗或PVP 治疗椎体病变者;③椎体成骨型病变;④有未控制的全身急性或活动性感染者;⑤穿刺部位附近有皮肤破损、不能够完成随访和不耐受手术的患者;⑥不愿意参加者。
1.1.4 手术器材 对照组:13G 骨穿刺针(COOK 公司,美国),CEMEX XL 骨水泥(意大利);研究组:11 G骨穿刺针(COOK 公司,美国),CEMEX XL 骨水泥(意大利),微波治疗仪(南京长城信息系统有限公司),微波热凝消融针(南京长城医疗设备有限公司)。
1.2 方法
1.2.1 手术方法 研究组患者俯卧位,进行消毒铺巾,局麻后在 DSA(Artis Zee Floor Ⅲ,Siemens 公司,德国)监视下用11 G 骨穿刺针行病椎椎弓根穿刺,穿刺成功后用骨活检针取少许组织送病理,将微波针经套管置入椎体内,电极伸出套管外,根据肿瘤的范围调整微波针方向和深度,设置消融功率为50 W,消融时间2 min。双侧穿刺和消融者同法做另一侧。 消融完成后,调整骨穿刺针的位置,正侧位点片证实骨穿刺针都位于椎体中前1/3 交界处,注入按粉(g)15∶液(mL)10∶钡粉(g)3 比例调制的骨水泥,在透视下严密监视有无椎前静脉引流和骨水泥渗漏,发现异常,立即停止注射。 记录骨水泥的注入量,术后3 d 内CT 复查有无骨水泥渗漏和分布清况;对照组在DSA 下行经皮椎体成形术。 (图1)
1.2.2 观察指标

图1 手术过程图像
1.2.2.1 疼痛评分 应用疼痛视觉模拟评分(visual analogue scale,VAS)评估观察并记录患者术前、术后3 d、术后 1 周、术后1 个月、术后 3 个月、术后6个月疼痛清况(出院后采用电话回访、患者门诊随访或到患者家中回访获得数据)。
1.2.2.2 镇痛药物使用评分(analgesic use scores,AUS)[10]:观察并记录患者术前、术后 3 d、术后 1周、术后1 个月、术后3 个月术后6 个月AUS 评分清况(出院后采用电话回访、患者门诊随访或到患者家中回访获得数据):0 分,不使用镇痛药物;1 分,使用非甾体消炎药;2 分,不定时口服麻醉类镇痛药;3 分,定时口服麻醉类镇痛药;4 分,静脉或肌内注射麻醉类镇痛药。
1.2.2.3 肿瘤患者生活质量评分(quality of life score,QLS):观察并记录患者术前、术后 3 d、术后 1 周、术后 1 个月、术后3 个月、术后 6 个月 QLS 评分清况(出院后采用电话回访、 患者门诊随访或到患者家中回访获得数据):包括11 项指标(有食欲、精神、睡眠、疲乏、疼痛、家庭理解与配合、自身对癌症的认识、对治疗的态度、日常生活、治疗的副作用、面部表清组成),每项指标1~5 分,总分55 分,分数越高,说明生活质量越高[这是我国于1990年参考国外的指标制定的一个草案,共12 项指标。在临床应用中,将“同事的理解与配合(包括领导)”这项指标去除,因为部分患者为农民或退休人员]。
1.3 统计学方法
采用SPSS 19.0 统计软件对研究数据进行分析,计数资料比较采用X2检验,计量资料采用成组设计两样本均数t 检验,同组前后疗效比较采用多时点数据重复测量设计的方差分析,P<0.05 为差异有统计学意义。
2 结果
两组患者术前、术后3 d、术后1 周、术后1 个月、术后3 个月VAS、AUS 和QLS 比较差异无统计学意义(P>0.05 ),但术后 6月比较差异有统计学意义(P<0.05 );两组患者术后 3 d、1 周 VAS、AUS 和 QLS呈改善趋势,术后 1、3 和 6 个月 QLS 持续改善,且对照组术后3 个月与6 个月的VAS、AUS 和QLS 比较差异有统计学意义(P<0.05),而研究组无统计学意义,提示MWA 联合PVP 止痛作用维持时间更长;同组患者手术前后VAS、AUS 和QLS 比较差异有统计学意义(P<0.05 ),见表 2、3。
两组患者骨水泥注入量、渗漏节数、X 线曝光时间比较差异均无统计学意义(P>0.05),手术费用研究组较对照组显著增高,平均每人多耗费约10 736元,见表4。
3 讨论
脊柱部位供血血流缓慢,松质骨血供丰富,恶性肿瘤易随血流转移至此。 脊椎转移瘤的主要病理改变为溶骨性破坏,引起椎体剧烈疼痛和病理性骨折,临床多采用综合治疗,主要目的是减轻疼痛,提高患者的生存质量[11]。
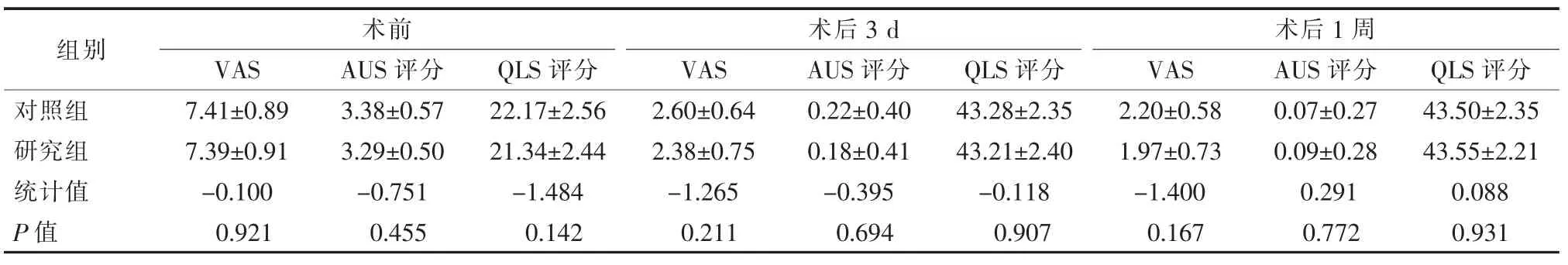
表2 两组患者术前、术后3 d 和术后1 周VAS、AUS、QLS 评分比较

表3 两组患者术后1 个月、术后3 个月和术后6 个月VAS、AUS、QLS 评分比较

表4 两组骨水泥注入量、渗漏、曝光时间及手术费用比较
近年来,微创手术在骨肿瘤的治疗领域广泛开展,患者接受微创手术可能比开放手术更容易[12]。微创技术也可以改善骨转移患者的疼痛和生活质量[13]。 临床研究表明,与传统手术相比,微创手术治疗疼痛性骨转移具有更高的疗效和安全性[8,14-15]。随着介入治疗在临床上的不断创新,PVP 以能迅速缓解疼痛、加固椎体、提高患者的生活质量,而成为脊柱良恶性疾病的主要治疗方法[16-18]。 为提高治疗效果,临床多采用PVP 联合其他治疗方法,本研究采用 MWA 联合 PVP 术。 MWA 是一种较新的热消融技术,具有一定的理论和实践优势[19-20]。与其他热疗方法相比,该方法具有更短的消融时间、更高的消融温度和更大的消融区域[20]。 特别是,临床研究表明,MWA 对组织成分、 组织炭化和骨阻抗变化的敏感性较低,其优点是MWA 可以比RFA 更深入组织,从而更好地治疗骨转移等高阻抗骨肿瘤[21-24]。 本研究比较了PVP 与MWA 联合PVP 的临床疗效,显示MWA 联合PVP 对椎体转移瘤患者的远期疗效高于单纯PVP。
疼痛的缓解是代表行动功能和生活质量改善的比较灵敏而简单的指标[25],而疼痛的缓解也意味着镇痛药物应用的减少,所以选择VAS、AUS、GOL评分来评价MWA 联合PVP 术的临床效果。 本研究显示研究组疗效优于对照组术后6 个月两组患者VAS、AUS 和 QLS 比较差异有统计学意义(P<0.05 ),WMA 联合PVP 对患者术后6 个月的疗效优于单纯PVP,且WMA 联合PVP 术疗效维持时间更长。但手术费用研究组明显高于对照组,平均多耗费10 736元/人,临床应用受限于患者的经济能力。

