铜冶炼产物中金属铜量测定方法的探讨
傅 饶,杨 林,周 婷,杨炳红,喻 星
(长沙矿冶研究院有限责任公司,湖南 长沙 410012)
铜是人类生产生活中占有极其重要地位的一种金属,由于长期的开采,铜矿资源已经日益枯竭。金属铜相作为铜冶炼过程中一个重要的相态,测定其含量对于铜冶炼工艺改进和尾渣回收利用都具有重要意义。
传统的金属铜测定方法为用盐酸羟胺溶液浸取铜的氧化物后,使用加入少量单硫醇及鞣酸的巯基乙酸氨性溶液来分离金属铜和铜的硫化物。反应过程不但复杂难以控制,而且其中有机试剂难以购置,并容易挥发毒害健康。基于此,我们对传统方法进行了一些改进,采用了较为安全易得的试剂浸取分离金属铜,并对分离中的一些关键的影响因素进行了条件探讨。
1 实验部分
1.1 仪器与试剂
火焰原子吸收光谱仪(普析公司),带铁空心阴极灯;筛式振荡器;科尔顿纯水机(湖南科尔顿水务有限公司)。
硝酸(ρ=1.42 g/ml);盐酸(ρ=1.19 g/ml);氨水 ;硫酸肼;碳酸铵。以上试剂均为分析纯。
纯铜粉(试剂,含铜99.99%);黄铜矿(含铜32.70%);铜 蓝(CuS,含 铜64.58%);Cu2S(含铜71.29%);冰铜(44.54%);斑铜矿(含铜66.81%);铁酸铜(含铜25.22%);CuO(含铜79.25%);Cu2O(含铜83.44%)。以上化合物均经显微镜鉴定和X-射线结构分析。
铜标准溶液:称取0.1000 g纯铜(纯度99.99%以上),加入15 ml硝酸(ρ=1.42 g/mL)溶解,将溶液蒸发至体积约为20 mL。冷却后,移入1000 ml容量瓶中,以水稀释至刻度,此溶液1 ml含0.10 mg铜。
实验用水均为三级纯水,电阻率为18.25MΩ·cm。
1.2 仪器工作条件
FAAS:波长为283.3 nm,灯电流:6 mA,光谱通带宽度为0.2nm,乙炔流量为1.5 L/min,空气压力为0.2 Mpa,燃烧器高度为7mm。
1.3 实验方法
氧化铜的测定:称取0.1g~1g试样(准确到0.0001g)于干燥的300ml碘量瓶中。加入50ml 30g/L盐酸羟胺-30g/L NH4Cl溶液(事先加热至沸腾)于沸水浴中浸取5min,迅速过滤,于滤液中测定氧化铜。
金属铜的测定:把滤渣连同滤纸移入原碘量瓶,加入100ml20%氨水-40g/L碳酸铵-10g/L硫酸肼溶液,震荡45min,迅速过滤,用5 g/L硫酸肼溶液洗涤碘量瓶和滤纸,在滤液中测定金属铜。
硫化铜的测定:把滤渣连同滤纸移入原碘量瓶,加入100 ml饱和溴水振荡1h,过滤,在滤液中测定硫化铜。
铁酸铜等其他铜的测定:把滤渣放入马费炉中灰化,用混合酸溶解后测定铜含量。
2 结果与讨论
2.1 氧化铜浸取溶剂的选择
有资料指出[1],30g/L的盐酸羟胺溶液是浸取氧化铜的理想试剂,在沸水浴中浸取5min,CuO及Cu2O均溶解完全,金属铜的溶解率在12%左右,其他铜矿物溶解率较小,此方法不适合金属铜含量高的试样。有研究表明[1],加入适量的NH4Cl,能抑制金属铜的溶解,并加速CuO的溶解。我们对此做了NH4Cl用量试验,结果见表1(数据采用4组数据的平均值):
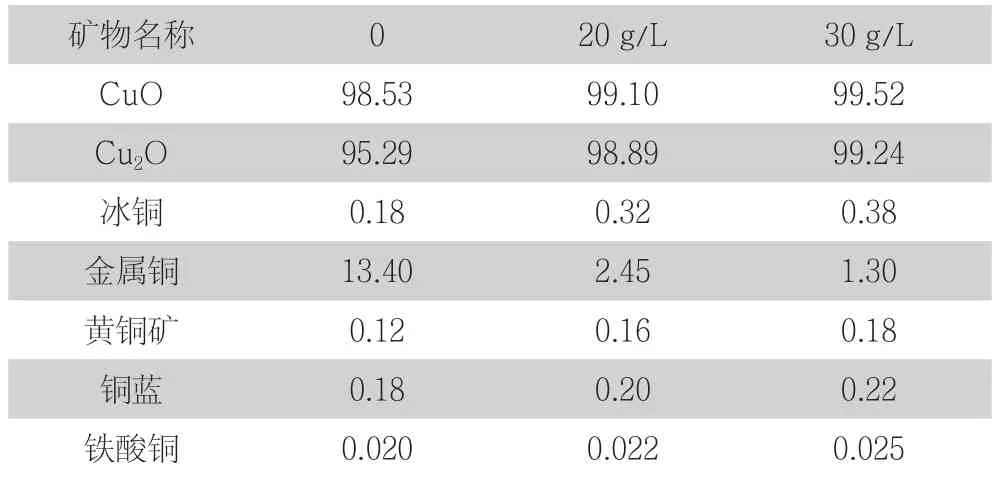
表1 NH4Cl用量的影响(浸取率,%)
结果表明,30g/L盐酸羟胺-30g/L NH4Cl溶液在沸水浴中能够完全浸取铜冶炼产物中的CuO及Cu2O,其他铜矿物的溶解较少,我们选用它来分离试样中的铜的氧化物。
2.2 金属铜浸取溶剂的选择
在过去的研究中[1],常常使用加了单硫醇的巯基乙酸氨性溶液对试样进行处理,抑制金属铜的溶解,再进去部分硫化铜的同时,使部分白冰铜转换为方黄铜矿型结构,从而在接下来浸取金属铜时这部分白冰铜不被浸取,然后用含盐酸羟胺的HgCl2-乙醇溶液浸取金属铜,最后用溴-甲醇溶液浸取剩下的硫化铜。
由于上述方法中的HgCl2,巯基乙酸,单硫醇都难以购置,且都带有毒性,污染环境,危害操作人员身体健康。我们考虑用一种易得低害的溶剂来浸取分离金属铜。
有报道[2]曾使用硫酸肼在沸水浴中浸取测定合金相中的铜,但在实际中发现,浸取效果并不理想,尤其在金属铜含量较高的铜冶炼中间产物中,浸取率常常在50%以下,其原因可能是粒度的影响,铜的良好延展性使其破碎难度加大,常含有颗粒较大的片状金属铜,导致浸取不完全。
碳酸铵的氨性溶液对金属铜有良好的溶解性,黄铜矿和斑铜矿的浸取率也较小,但是铜蓝和冰铜的浸取率较高。在碳酸铵的氨性溶液中加入一定量的硫酸肼,对硫化铜的溶解有明显的的抑制作用,还能使金属铜更好的溶解。根据生产经验,我们使用20%氨水-40g/L碳酸铵溶液浸取铜冶炼中间产物中的金属铜,硫酸肼用量影响结果见表2。
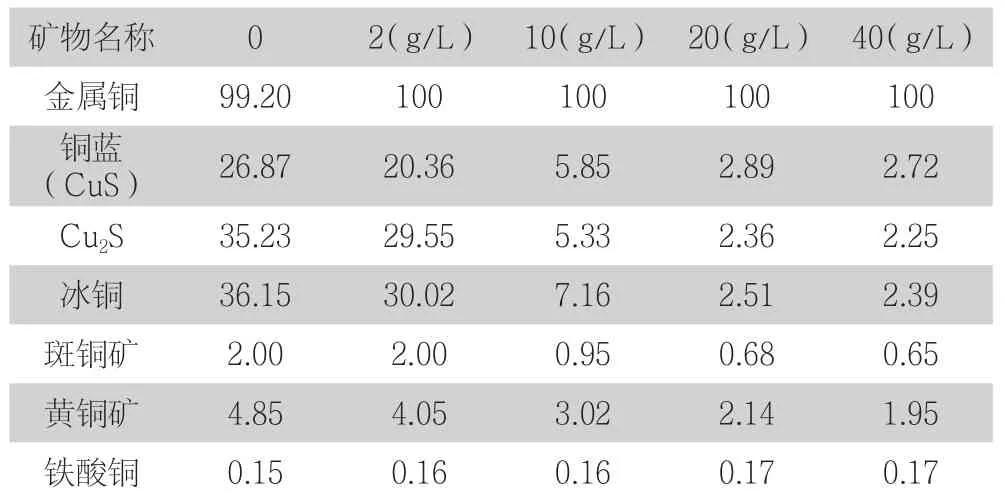
表2 硫酸肼用量的影响(浸取率,%)
表2的结果表明,硫酸肼的加入确实对铜硫化物的溶解有较强的抑制作用。当硫酸肼的用量在20 g/L以上时,铜硫化物的浸取率变化已经平缓,2%左右的浸取率也能满足物相分析方法要求,所以我们选择20%氨水-40 g/L碳酸铵-20 g/L硫酸肼溶液来浸取铜冶炼中间产物中的金属铜。
2.3 浸取时间的选择
确定浸取溶剂后,为了探讨最佳浸取时间,我们用20%氨水-40 g/L碳酸铵-20 g/L硫酸肼溶液做了浸取时间条件实验,结果见表3。表3的结果表明,在15 min时,金属铜基本已经溶解完全,而随着浸取时间的增加,其他铜矿物的溶解度呈现增加趋势,考虑到粒度原因,我们认为浸取30 min既能满足分离金属铜的需要,又能防止其他铜矿物浸取增多。
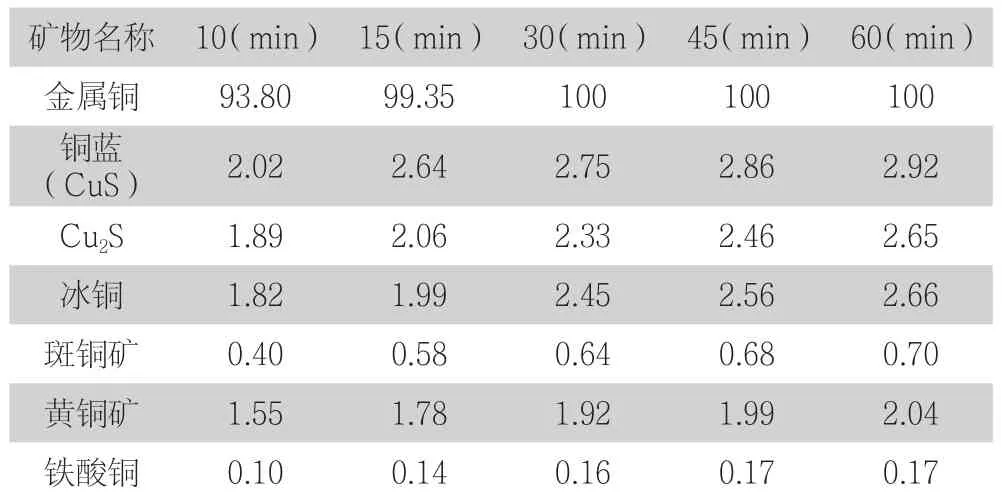
表3 浸取时间的影响(浸取率,%)
2.4 粒度对金属铜浸取的影响

表4 粒度浸取试验(浸取率,%)
上面已经提到,由于金属铜良好的延展性,所以当金属铜含量较高时,试样破碎的粒度对浸取结果有很大影响,为此我们特地做了粒度实验,把含量98.82%的粗铜破碎后分别过筛,分别用20%氨水-40 g/L碳酸铵-20 g/L硫酸肼溶液对通过150目、180目、200目的试样浸取30 min,结果见表4。

表5 合成样品成分及回收率(含铜量,%)
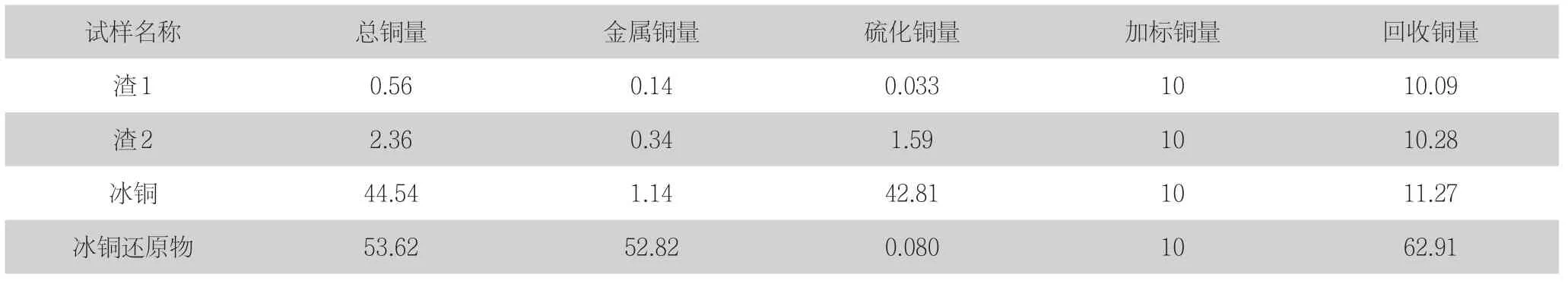
表6 生产样品及加标回收实验(每100mg试样含铜量,mg)
试验结果表明:金属铜的粒度对浸取结果影响非常大,在200目时,金属铜基本浸取完全,而在粒度最大的150目,金属铜的浸取率仅有52.12%,可见试样的颗粒大小对金属铜的浸取至关重要,因此制样时,试样最少要能通过180目筛,最好达到200目。
2.5 合成样品回收试验
把基准矿物CuO、Cu2O、纯铜粉、铜蓝(CuS)、Cu2S、冰铜、斑铜矿、黄铜矿、铁酸铜按1:1:2:1:1:1:1:1:1的比例均匀混合,制得合成样品,然后按照实验步骤分离测定铜含量,结果见表5。
回收率试验表明,用本方法测定基准矿物合成样品中金属铜含量,回收率约为102.9%,是一个较为理想的结果。
2.6 实际生产样品测定结果
为了验证本方法在实际生产中的效果,我们选用了几个铜冶炼过程中的中间产物及冶炼渣来做浸出实验,并使用了加入定量金属铜粉的方法来验证,其结果见表6。
由表6可见,生产样品中的金属铜回收较为理想,需要特地指出的是,在冰铜样品中,由于经过显微镜鉴定和X-射线结构分析,金属铜含量是微量的,样品分析中得到的金属铜量,是硫化铜矿物溶解所致,所以当硫化铜矿物量远远高于金属铜量时,所得到的金属铜量是不准确的,必须经过修正得到一个参考值。
3 结论
本文研究了以20%氨水-40 g/L碳酸铵-20 g/L硫酸肼溶液作为溶剂分离测定铜冶炼产物中的金属铜量。用30g/L盐酸羟胺-30g/L NH4Cl溶液预先浸取铜的氧化物,过滤分离,滤渣用20%氨水-40 g/L碳酸铵-20 g/L硫酸肼溶液振荡30 min浸取金属铜,铜的硫化物浸取率在3%以下,铁酸铜基本不溶解。
探讨了硫酸肼用量、浸取时间和金属铜粒度对浸取结果的影响,确定了粒度在180目以下,用20%氨水-40 g/L碳酸铵-20 g/L硫酸肼溶液作为溶剂,振荡浸取15 min的最佳试验条件。
用本法测定不同类型铜冶炼产物中金属铜量,结果相对稳定,对于铜的硫化物远高于金属铜的试样,需要用硫化铜浸出2.5%进行修正。

