四氧化三钴的制备及应用研究进展
汤春妮
(陕西国防工业职业技术学院化学工程学院,陕西 西安 710300)
过渡金属氧化物具有金属氧化物丰富的价态,在许多领域有着重要的应用。其中,四氧化三钴(Co3O4)为典型半导体,具有成本低、来源广、稳定性好和催化活性高等优点,广泛应用于超级电容器、锂离子电池、催化剂、气体传感器、压敏陶瓷、磁性材料和颜料等领域[1]。因此,制备形貌新颖和性能优越的Co3O4材料一直是科学家研究的热点。作者在此介绍Co3O4的基本性质,对Co3O4的制备方法及其应用进行综述,以期为Co3O4材料的开发和应用提供参考。
1 四氧化三钴的基本性质
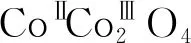
2 四氧化三钴的制备方法
根据制备 Co3O4原料的状态,可将其制备方法分为三大类,即固相法、气相法和液相法;根据制备 Co3O4步骤的多少,可将其制备方法分为直接法和组合法。
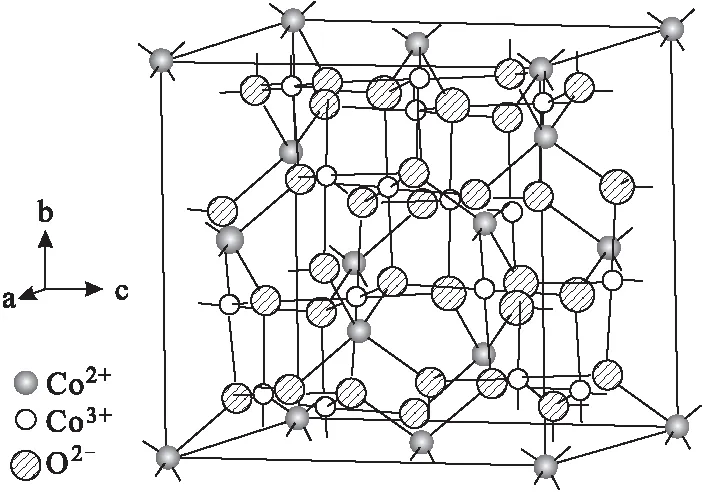
图1 Co3O4的尖晶石结构
2.1 固相法
固相法是利用固体原料发生化学反应制备材料的方法,具有操作简单、无溶剂参与的特点。固相法分为直接高温固相法和室温固相反应-热分解法,其中直接高温固相法主要包括热分解法和灼烧氧化法。热分解法是在高温条件下将钴盐(如硝酸钴、硫酸钴、氯化钴、碳酸钴、草酸钴、醋酸钴、氢氧化钴等)加热分解得到Co3O4;灼烧氧化法是在高温条件下将单质钴氧化为Co3O4。这两种直接高温固相法存在产物易团聚、颗粒粒径分布不均匀和产物形貌不易控制等不足,目前研究很少。室温固相反应-热分解法是在室温条件下或者近室温条件下将固体原料通过化学反应转变为前驱体再进行热分解得到产物。王坤[3]以钴盐与氟化铵或者草酸为原料,采用固相反应-热分解法制备了3种不同形貌(八面体状、片状和棒状)的Co3O4纳米材料,探究了反应条件对产物形貌的影响,并推测了不同形貌产物的固相形成机理。
2.2 气相法
气相法是直接利用气体或通过各种手段将含钴化合物转变为气体,使其在气体状态下发生化学反应而形成产物,该方法对反应物的要求比较苛刻。常见的制备Co3O4的气相法主要包括化学气相沉淀法和喷雾热分解法。
2.2.1 化学气相沉淀法
化学气相沉淀法是指加热使物质直接汽化后再发生化学反应,最后结晶沉淀。该方法具有产物粒径和涂层密度可调、产物粒径分布均匀等特点,但也存在沉积速度慢、具有安全隐患等不足。Bahlawane等[4]利用乙酰丙酮钴和氧气,采用化学气相沉淀法沉积氧化钴薄膜,薄膜为立方尖晶石型多晶Co3O4,晶粒尺寸为30~40 nm。
2.2.2 喷雾热分解法
喷雾热分解法是将可溶性的盐溶解加热,然后高压喷雾进入高温气氛中,经蒸发-热分解-烧结成型等过程形成产物。该方法具有产物粒径可控、粒子分散性好、效率高等特点,是一种较适合制备超细粉体及薄膜等的气溶胶技术,适用于工业化生产。Du等[5]以硝酸钴和尿素混合溶液为原料,在600 ℃空气中经喷雾-热分解-煅烧制备了多孔空心Co3O4微球(图2)。该多孔空心Co3O4微球由纳米颗粒组装而成,其孔隙率随体系中气体量的变化而变化。在热解过程中,尿素不断分解成气态组分,作为模板控制多孔结构。前驱体液滴逸出的气体量直接影响微球的孔隙率,由尿素与硝酸钴的比例控制纳米颗粒的大小。电化学测试结果表明,多孔空心Co3O4微球的性能与纳米颗粒的孔隙率和尺寸有关。
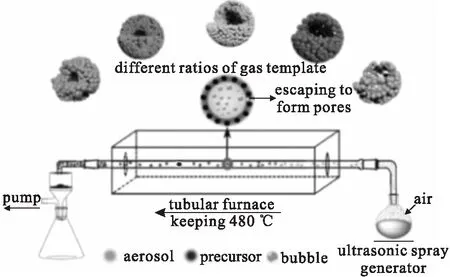
图2 喷雾热分解法制备多孔空心Co3O4微球示意图
2.3 液相法
液相法可以控制晶体的成核和生长过程,进而控制颗粒的形貌及化学组成,是目前实验室以及工业生产制备纳米材料最广泛采用的方法。制备Co3O4的液相法较多,主要包括化学沉淀法、水热法、溶剂热法、溶胶-凝胶法、微乳液法、电沉积法、还原氧化法等。
2.3.1 化学沉淀法
2.3.2 水热法
水热法是以水为反应溶剂,在密闭的高温高压下进行的一种液相化学反应。由于高温高压使体系中的水处于超临界和亚临界状态,水及有水参与的物理过程(如溶解)、化学过程与常温下不同,进而得到不同的产物。Xia等[8]报道了一种简便的自支撑空心Co3O4纳米线阵列大面积生长的水热法。将硝酸钴和硝酸钠溶解于氨水中,反应后将溶液转移到带盖可蒸压的瓶中,随后将沉积了Co3O4种子层的基材固定其中,再注射氧气加热至120 ℃12 h,随后在流动氩气中250 ℃退火,即得到排列整齐的垂直生长到衬底上平均直径为200 nm 的Co3O4纳米线阵列。Rui等[9]以硝酸钴为钴源、尿素为沉淀剂、氟化铵为诱导剂,在120 ℃下水热反应 5 h制得空心海胆前驱体,在空气中通过热处理转化为分层海胆状Co3O4空心球体(直径5~8 μm),其由许多互联的Co3O4纳米颗粒(10~50 nm)组成一维纳米线再组成海胆状。
2.3.3 溶剂热法
与水热法相似,溶剂热法是在纯水中加入有机溶剂或完全釆用有机溶剂,在密闭的高温高压下进行液相化学反应。体系中的有机溶剂不仅可以作为反应介质,有时也可兼作反应物。可通过选择不同的非水溶剂、改变反应条件来控制产物的形貌、尺寸、结构及性能等。Park等[10]以硝酸钴为原料,以十二烷基苯磺酸钠(SDBS)为表面活性剂、甲醇为溶剂,采用表面活性剂辅助溶剂热-煅烧法制备了直径为200~300 nm的Co3O4空心纳米球,其壁厚约为40 nm。Cao等[11]以硝酸钴和尿素为原料,以二甘醇为溶剂,采用一锅溶剂热法制备了具有良好多孔性的Co3O4微立方体,并进行了后续煅烧,热处理后的立方体形貌可以完全保留。Sun等[12]以二碳酸六羟五钴为原料、氨水为溶剂,利用简单的溶剂热法成功制备了具有微球、纳米带和纳米板形貌的Co3O4纳米结构。
2.3.4 溶胶-凝胶法
溶胶-凝胶法是将含有高化学活性成分的化合物混合均匀后,经水解、缩合、老化等一系列反应制备金属氧化物的一种方法。该方法反应温度低,能从分子水平上控制产物的粒径从而获得高纯度、粒径分布均匀的金属氧化物。Lu等[13]以硝酸钴、硝酸铈和柠檬酸为原料,采用柠檬酸溶胶-凝胶-热分解法制备了一系列不同Co/(Co+Ce)原子比的CeO2-Co3O4混合氧化物催化剂。赵清清等[14]采用溶胶-凝胶自蔓延燃烧法制备了纳米Co3O4材料,其中硝酸钴和柠檬酸物质的量比为1∶2、400 ℃空气气氛下热处理制备的Co3O4材料的电化学性能最好。
2.3.5 微乳液法
微乳液法是指利用表面活性剂的作用使两种互不相容的溶剂形成不同形状的胶束,从而在胶束的反应空间制备相对应形貌的产物。其特点是制备产物的形貌和大小可以精准控制,产物粒子间稳定性好、分散性好,但受表面活性剂种类、用量以及溶剂种类、配比等因素影响。璩洁荷[15]使用十六烷基三甲基溴化铵/正丁醇/环己烷/氯化钴和十六烷基三甲基溴化铵/正丁醇/环己烷/草酸双微乳液体系制备了草酸钴前驱体,再通过煅烧前驱体制得棒状Co3O4;并探讨了沉淀剂种类、表面活性剂种类、分散剂聚乙二醇、H2O/表面活性剂比值、油/水比值和表面活性剂/助表面活性剂比值以及煅烧温度对前驱体和Co3O4形貌的影响。Zhang等[16]首次采用快速微波辅助溶剂热过程的微乳液法制备了在可见光下能将纯水分解成化学计量的氢气和氧气的 Co3O4量子点(3~4 nm)。
2.3.6 电沉积法
电沉积法是指金属或金属氧化物从其化合物水溶液、非水溶液或熔盐中电化学沉积出的方法,具有产物粒径和形貌可控的优点。Guo 等[17]在室温和常压下微量添加聚乙烯亚胺,采用一步阴极电泳沉积(C-EPD)法在钛片上制备纳米Co3O4薄膜。Aghazadeh 等[18]以硝酸钴为原料,采用电沉积法先制备出均匀涂覆在不锈钢基体上的氢氧化钴前驱体,再在氧气气氛中高温煅烧制备了Co3O4纳米片(图3)。史咏鑫[19]采用电沉积法结合煅烧法,以硝酸钴溶液为原料,分别在多孔铜和铜箔基底上制备了多孔Co3O4材料和Co3O4材料。
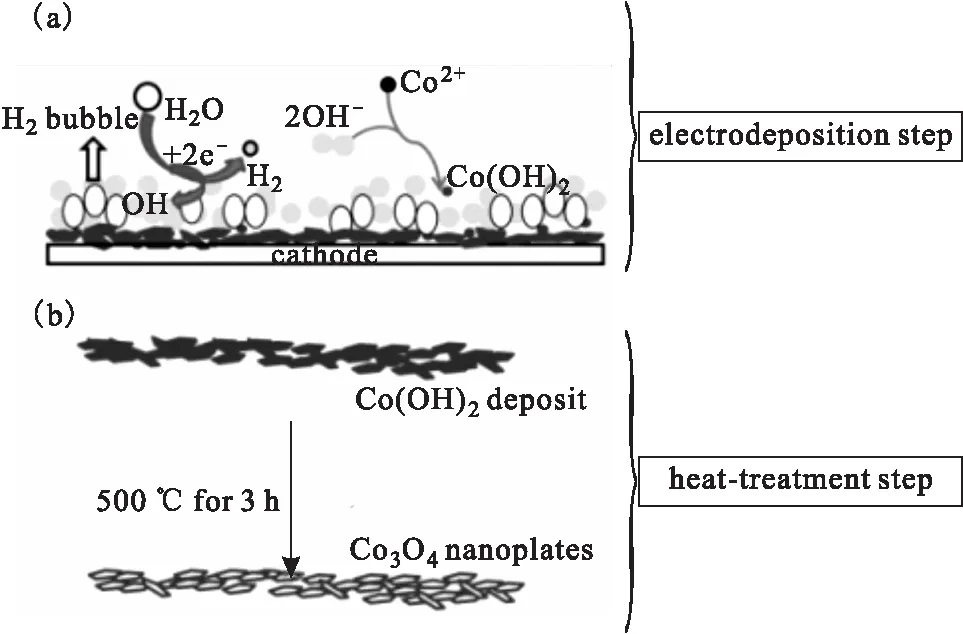
图3 电沉积-热处理法制备Co3O4纳米片原理示意图
2.3.7 还原氧化法
Ke等[20]首次采用还原氧化法制备Co3O4纳米棒。将氯化钴的水溶液和邻二氮杂菲水溶液混合超声形成Co2+配合物,再加入还原剂硼氢化钠水溶液生成由苯基包覆的Co 纳米颗粒,然后离心分离,干燥,与氯化钾和氯化钠混合后高温煅烧,形成直径约150 nm、长度约2 μm的Co3O4纳米棒。加入邻二氮杂菲使钴粉表面包覆有机物而有效降低钴粉的磁吸附团聚,高温煅烧前添加氯化钾和氯化钠可将钴粉粒子分隔而进一步降低了钴粉的团聚。该方法过程比较繁琐,且引入了杂质离子。
2.4 组合法
组合法一般是指将两种及两种以上的方法结合,很多方法都能与热分解法结合来制备目标产物。经热分解后的产物通常能保持中间体的整体外观形貌。如超声沉淀-热分解法、沉淀-溶剂热-热分解法、模板法、接枝/改性-热分解法等。
2.4.1 硬模板法
模板法可以制备许多纳米尺寸的微反应器,使化学反应在微反应器中进行,微反应器的形状决定了产物的尺寸和形貌。模板法采用的模板主要分为两类:硬模板和软模板。硬模板法广泛应用于制备各种空心无机材料,通常至少需要3个步骤:(1) 准备功能化表面硬的模板;(2)在模板上涂覆设计的无机材料;(3) 选择性消除模板得到空心结构产物。许多材料,如高分子、无机非金属和金属颗粒等均可作为硬模板。主要的硬模板包括:胶态聚苯乙烯、碳球、二氧化硅、生物模板、阳极氧化铝等。Ohnishi等[21]采用两步法制备了Co3O4空心球。首先在600 nm 聚苯乙烯表面涂覆碱式碳酸钴制备钴盐/聚苯乙烯杂化粒子,在空气中于400 ℃下煅烧,制备了直径 660 nm的Co3O4空心球。Shen等[22]采用单源化学气相沉淀法,在多孔阳极氧化铝膜的纳米通道内成功制备了具有良好取向的Co3O4纳米管,其平均直径为100~300 nm,与模板的孔径一致。
2.4.2 软模板法
与硬模板法相比,软模板相对容易删除而受到更多的关注,但由于软模板的可变形性,其产物的空心形貌和单分散性较差。常用的软模板包括表面活性剂[SDBS[23]、十二烷基苯磺酸(DBS)[24]等]和聚合物[聚乙烯基吡咯烷酮(PVP)[25]等]。He等[23]在SDBS存在下,采用溶剂热法分解硝酸钴制备了Co3O4空心纳米球。在硝酸钴、氢氧化物转变为Co3O4空心纳米球的过程中,表面活性剂SDBS起到了关键作用。Wang等[25]报道了一种通过无机盐前驱体优先吸附到多壳层的PVP模板来制备多壳Co3O4空心球的方法,认为新结构的形成是由于PVP软模板和羧甲钴的形成。通过控制PVP的浓度,得到不同壳数的PVP多片层胶束,利用PVP多片层囊泡模板制备了多壳Co3O4空心球,因为PVP可以通过-N和/或C-O基团协调匹配金属离子表面。当PVP浓度较低时,单壳Co3O4空心球(S-Co)产生,S-Co是由无数的纳米片指向球体中心;随着PVP浓度的增加,双壳Co3O4空心球(D-Co)形成;PVP浓度继续增加,三壳Co3O4空心球(T-Co)形成。多壳Co3O4空心球可能的形成过程如图4所示。

图4 在PVP模板存在下不同结构钴前驱体的制备示意图
2.4.3 接枝/改性-热分解法
通过高分子化合物或有机溶剂对可溶性钴盐进行接枝或改性,煅烧后可得到不同形貌和粒度的Co3O4产物。杨玉英等[26]通过接枝羧基淀粉(ISC)吸附Co3+获得非晶前驱体,然后进行热分解,制备了粒度均匀、分散性好的球形Co3O4钠米粒子。Zhao等[27]利用氯化钴和各种醇类前驱体,在不同的温度下制备了形貌可控的Co3O4结晶粉体,其中将氯化钴溶解在苄醇中,经烘干、煅烧,制备了具有正方双锥形貌、分散性好、颗粒均匀的Co3O4微粉。有机溶剂不仅吸附Co2+,而且Co3O4与醇形成多面体粒子形状。
3 四氧化三钴的应用
3.1 超级电容器
超级电容器因其比功率密度大、充放电速度快和循环使用寿命长而被认为是最重要的电能存储装置之一。目前,超级电容器已应用于电池、能源动力以及电子产业方面[28]。Co3O4由于其低成本和优异的电化学电容性能,被认为是一种理想的电极材料。Li等[29]采用金属-有机骨架热裂解法制备了多孔Co3O4微花电极,在电流密度为0.625 A·g-1时,比容量达240.2 F·g-1,且经过2 000次循环后,Co3O4的比容量在3.75 F·g-1时仍然大于96.3%。Cui等[30]利用微波辅助水热法制备了Co3O4纳米棒,经过500次循环,其比容量也可达到456 F·g-1,显示了其在电化学电容器中的潜在应用。Wang等[31]利用水热法制备了多种Co3O4纳米结构,其中在50 ℃下合成的介孔网状Co3O4纳米结构具有较好的电化学性能,在1.4 mg·cm-2的质量负载下,其比容量为1 090 F·g-1。
3.2 锂离子电池
锂离子电池是含有锂离子电极材料的一种二次充电电池,具有使用寿命长、安全性好、绿色环保、自放电小等优点,已得到了广泛应用。Co3O4可以提供比目前使用的石墨的理论容量(<372 mA·h·g-1)大3倍的容量。在转换反应Co3O4+8Li++8e-=4Li2O+3Co,Co3O4的理论容量为890 mA·h·g-1。然而,Co3O4材料在实际应用中面临的主要挑战是:由于体积变化引起的多次充放电周期的容量衰减。Wang等[32]采用硬模板法成功制备了产量大、纯度高的均匀多壳Co3O4中空微球,以其作为锂离子电池的阳极材料时,多壳Co3O4中空微球表现出优异的速率容量、良好的循环性能和超高的比容量,在第30次循环后比容量为1 615.8 mA·h·g-1。Co3O4在锂离子电池中的优越性能源于多壳多孔中空微观结构保证了更多的锂储存场所、较短的锂离子扩散长度和足够的空隙缓冲体积膨胀空间。Li等[33]采用喷雾热解CoCl2溶液制备了锂离子电池阳极用纳米微粒组装的Co3O4微球,其具有最小初始粒径和低氯含量的样品,在电流密度为200 mA·g-1时,经过50次循环,初始库仑效率最高为73%,可逆比容量高达1 340 mA·h·g-1。
3.3 催化剂
过渡金属氧化物具有空电子轨道,能接受电子而转移电子,生成较稳定的配合物使反应快速进行,故可作为催化剂,而Co3O4是一种性能良好的过渡金属氧化物催化材料。Co3O4可代替过渡贵金属催化剂催化氧化CO、碳氢化合物和挥发性有机物(VOCs)。Hu 等[34]以Co3O4纳米带和纳米管为模型催化剂,对CO进行了氧化。结果表明,暴露(011)晶面的Co3O4纳米带比暴露(001)晶面的Co3O4纳米管的活性更高,因为在Co3O4纳米带(011)晶面上的Co3+位的翻转频率远高于Co3O4纳米管(001)晶面的翻转频率,揭示了形状和晶面效应的本质。Fei等[35]证明了相比于Co3O4纳米棒,Co3O4纳米管催化氧化甲醇时表现出较好的活性和稳定性。其优异的催化活性主要来自于主要暴露的(112)晶面。一般来说,表面反应性取决于材料表面原子的密度和不饱和化学键的数目(悬空的化学键)。与其它晶面相比,有更多开放结构的(112)晶面的C-H键断裂的电能壁垒更低。Dissanayake等[36]制备的介孔Co3O4对氧化VOCs的模型底物2-丙醇具有较好的活性。活性最高的Co3O4-350材料在160 ℃、单位质量空间速度为60 L·g-1·h-1时,最大翻转频率为25.8 h-1。介孔Co3O4的表观活化能为69.7~115.6 kJ·mol-1。原位漫反射红外光谱显示,该反应在催化剂表面生成羰基和碳酸盐,然后完全氧化为CO2和H2O。
3.4 光电催化剂
Co3O4是一种禁带宽度比较窄的半导体,近年来,在光催化和光电催化领域崭露头角。Co3O4可以光解水制备氧气和氢气[37]、降解有机污染物(如染料[38]、苯酚[39]、1,2,4-三氯苯[40]、异丙醇[41])等。Zhang等[37]利用反向胶束合成法首次快速制备了3~4 nm的Co3O4量子点,其在可见光照射下能够把纯水按化学计量分解为氧气和氢气。由于Co3O4量子点的量子尺寸效应导致Co3O4禁带变宽,而价带无变化,从而导致导带底上移,导带电位低于H+的还原电位,使其在没有任何助催化剂的情况下在可见光照射下光解水同时制备氧气和氢气。这为窄带隙半导体光解水制氢气提供了新的途径。Lou等[38]考察了制备的Co3O4纳米棒在紫外光/可见光照射下对活性染料B-GFF、B-RN和K-NR的光催化降解性能。结果表明,Co3O4纳米棒对3种活性染料均有光催化降解活性。彭亚洲[40]采用溶胶-凝胶法制备了具有可见光响应的Co3O4光催化材料,其对1,2,4-三氯苯的可见光光催化降解效果显著,其反应速率符合一级动力学方程。王强[42]采用光还原法和热分解法制备了三元复合电极Co3O4/Ag/TiO2-NTs,比较了在光催化/电催化/光电催化条件下,其对硝基苯和Cr(Ⅵ)混合废水的处理效果。结果表明,相比于单一的点催化和光催化,光电催化的协同作用使其处理效果大大提高。
3.5 气体传感器
Co3O4可作为检测痕量生物分子或有毒气体的化学传感器。Co3O4纳米结构气体传感的性能在很大程度上取决于其形貌和组合,关于晶体尺寸、形貌、表面结构、晶体取向、可控性孔隙、堆积方式、长径比、晶体密度等形态控制方面的研究很多[43-44]。通常,多孔结构通过增加表面活性位点和促进目标气体的扩散,有利于提高气体传感性能。例如,Choi等[45]以乙酸钴为原料,通过控制溶剂热反应条件,制备了各种形态的含钴前驱体,如纳米片、纳米棒、纳米管等,将其在不发生形态变化的情况下转化为Co3O4纳米薄片、纳米棒和纳米管,在300 ℃下对100×10-6C2H5OH的气体响应分别比凝聚的Co3O4纳米颗粒高10.5倍、4.7倍和4.5倍,主要是由于Co3O4传感材料具有结块较少的纳米结构。近年来,也有许多关于Co3O4基复合材料气体传感的研究报道[46]。由于复合材料中不同组分之间的协同作用,使得复合材料的气敏性能相对于相应的纯体系有所提高,主要包括Co3O4/无机金属氧化物复合材料、Co3O4/碳纳米复合材料、Co3O4/聚合物复合材料、Co3O4/贵金属复合材料等[47]。
3.6 其它应用
处于四面体a位和八面体b位的离子之间发生了尖晶石结构的Co3O4反铁磁交换,因此,Co3O4表现出超强的磁性,可作为磁性纳米颗粒,在微电池、纳米线、特殊合金和催化剂等方面应用广泛。Mohammadi等[48]以尼龙6和Co3O4@SiO2磁性纳米颗粒为原料,首次制备了新型磁性高分子材料,对废水中Pb(Ⅱ)的去除效果显著。Co3O4纳米颗粒的VSM模式表明,Co3O4纳米颗粒在25 ℃时具有顺磁性,因此可以简单地用外部磁铁将其分离出来。
Co3O4可作为制备硬质合金的材料。饶岩岩等[49]采用火花等离子烧结技术,原位制备了WO3、Co3O4和碳的混合粉末,得到了致密的WC-Co硬质合金。
压敏陶瓷是指电阻值随着外加电压变化而敏感非线性变化的半导体陶瓷,Co3O4可以作为制备压敏陶瓷的材料之一。Ghazali等[50]考察了Co3O4掺杂对Zn-Bi-Ti-O压敏陶瓷非线性系数的影响,通过掺杂Co3O4可以改进非线性系数(α)并预防在热处理过程中Bi2O3的蒸发。
Co3O4也可作为玻璃、陶瓷着色剂和颜料。王峰等[51]以纳米级二氧化锆为原料,以Co3O4为着色剂,添加少量烧结助剂,制得了颜色亮丽、性能优良的蓝色氧化锆陶瓷。
吸收材料是指能将照射到其表面的各种能量吸收转化或衰减的一种材料,Co3O4也可作为一种吸收材料。Li等[52]以三聚氰胺泡沫为初始骨架,将Co3O4纳米粒子分散在石墨烯包裹的碳泡沫上,制备了一种简单、经济的新型结构的Co3O4/还原氧化石墨烯/三聚氰胺衍生碳泡沫(Co3O4/RGO/MDCF)混合物。该材料展现出良好的微波吸收性能,在11.54 GHz 的最大的反射损失(RL)值为-31.88 dB。
4 结语
Co3O4由于其结构丰富、性质新颖,潜在应用好,近年来发展迅速。典型的Co3O4制备方法主要有直接高温固相法、室温固相反应-热分解法、化学气相沉淀法、喷雾热分解法、化学沉淀法、水热法、溶剂热法、溶胶-凝胶法、微乳液法、电沉积法、还原氧化法、模板法、接枝/改性-热分解法等。Co3O4在超级电容器、锂离子电池、催化剂、光电催化剂、气体传感器、磁性材料、压敏陶瓷、颜料、吸收材料等领域具有潜在的应用前景。
由于单一Co3O4材料的性能难以满足实际应用需求,因此有必要借助各种措施来提升其性能,如形貌控制、金属/非金属掺杂、表面金属沉积、半导体复合、碳材料复合等。此外,应考虑通过改性来同时满足两个或两个以上功能要求,如超顺磁性、光谱选择性、生物相容性、光催化、机械和/或电特性、荧光、刺激反应等。在应用方面,可以多探究一些新型应用,如光催化、超疏水性等。作为一种重要的多功能材料,Co3O4将会在能源、环境、材料、化学等领域发挥重要作用。

