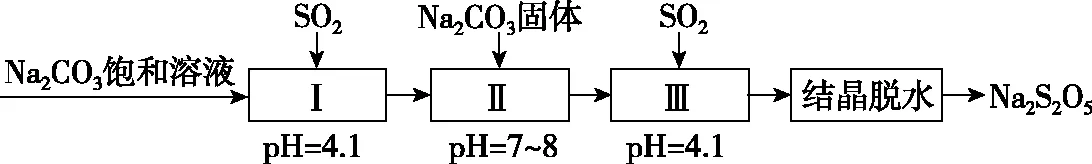
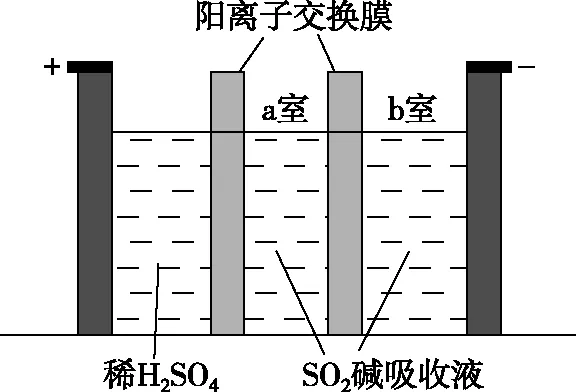
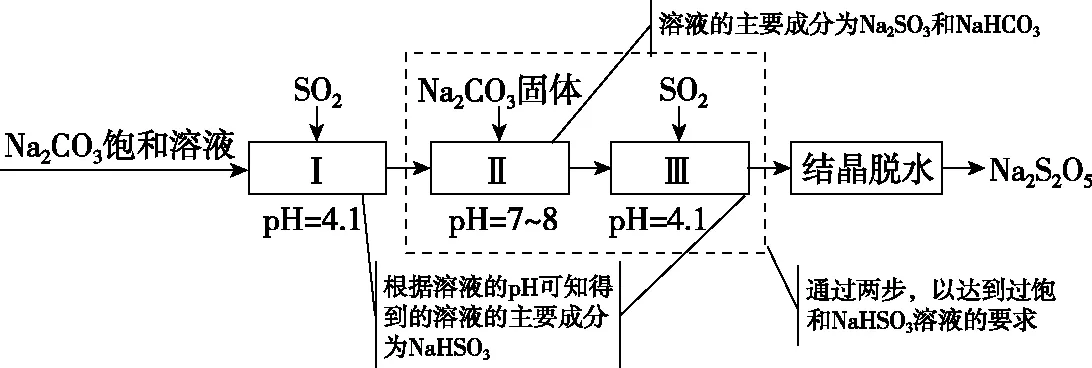
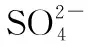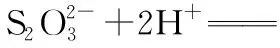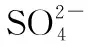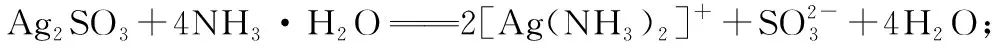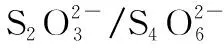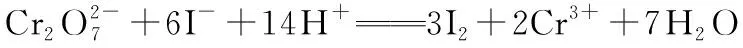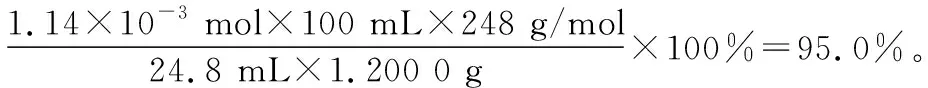构建体系 把握考向 突破考点——氧族元素高考题型例析
江西 张万程
从历年的高考试题分析来看,氧族元素及其化合物是元素化合物知识中的高频考点。作为高考化学命题的重要载体,掌握元素及其化合物知识,有利于宏观把握化学学科的学习,也有利于提高学生的成绩。氧族元素及其化合物种类丰富,需要强制记忆的知识比较多,且在试题中常出现含硫元素的陌生物质,学生在高考有限的时间内难以加工和理解陌生信息,导致得分偏低。本文主要结合学生的认知能力,明确知识脉络,构建知识体系,详细地总结并归纳出近年涉及氧族元素及其化合物的高考试题,供老师和学生在复习时参考,望对高考复习有所帮助。
一、构建知识体系,明晰价-类二维图
1.构建氧族元素知识体系
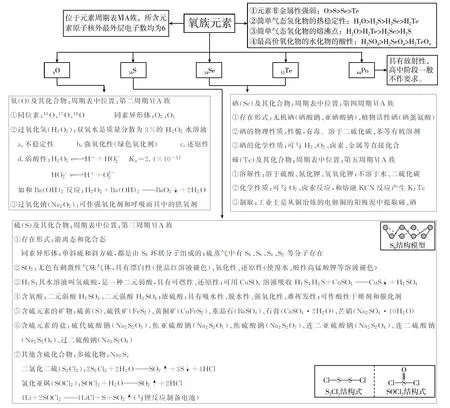
2.氧和硫元素的价态-类别二维图
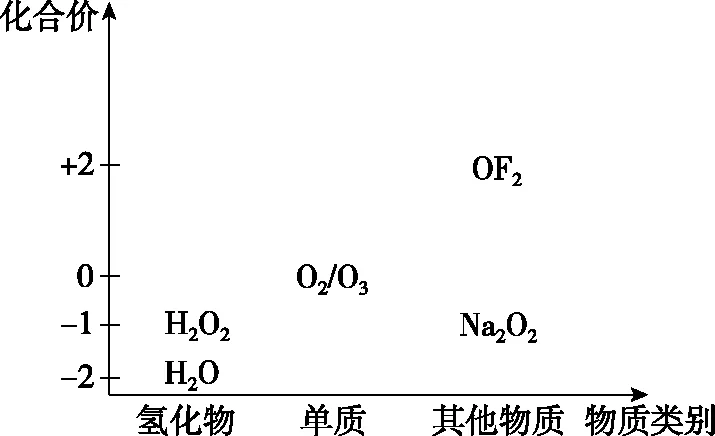
氧的价-类二维图
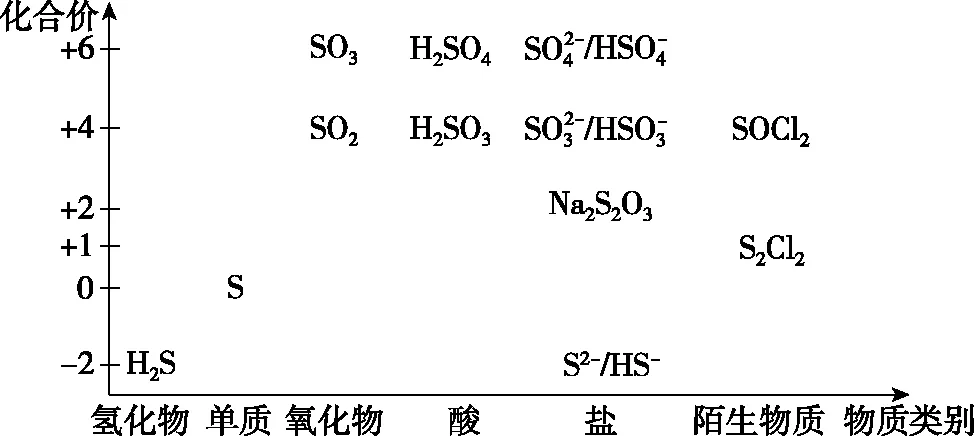
硫的价-类二维图
二、近三年理综化学关于氧族元素的考查点
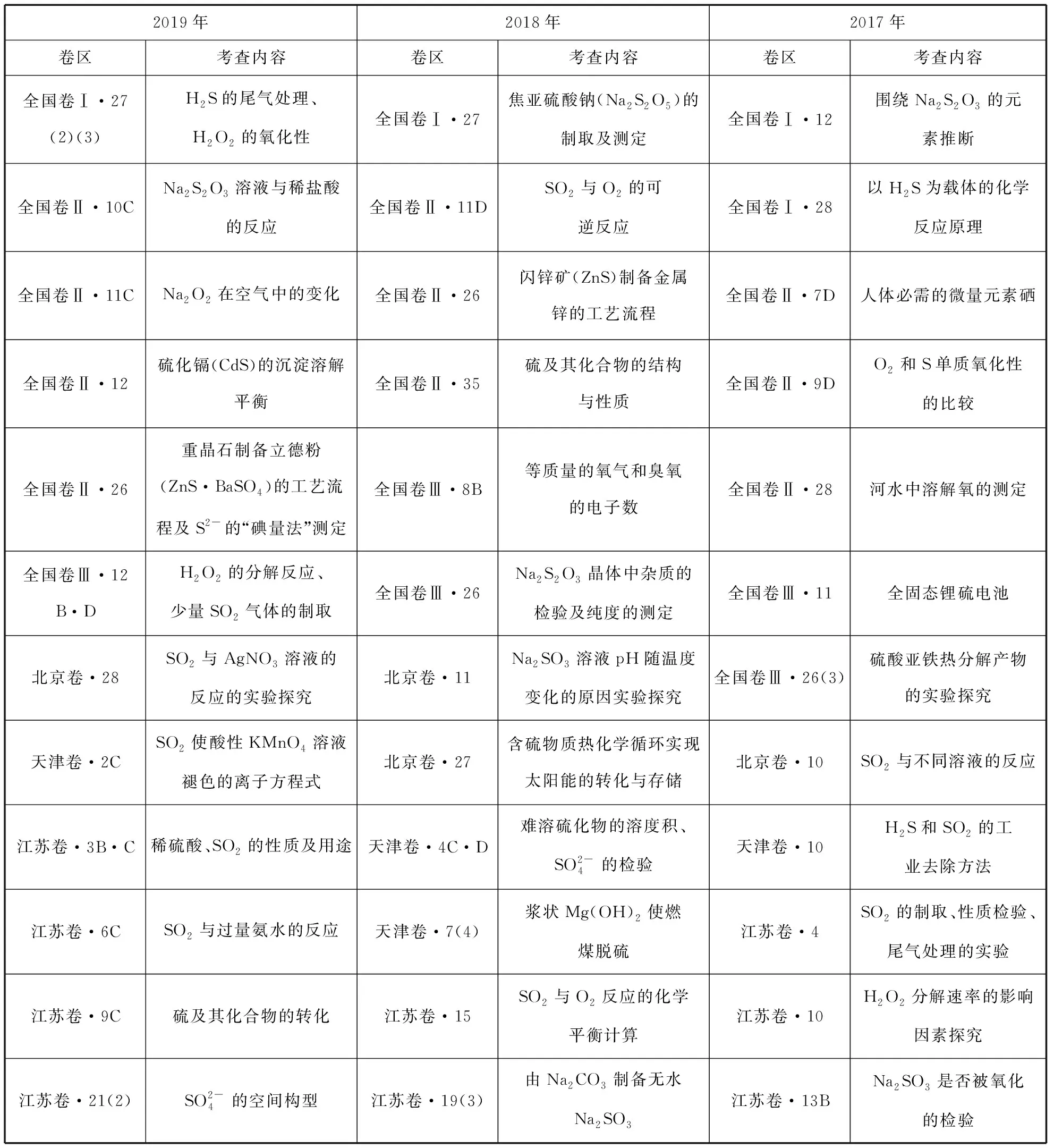
2019年2018年2017年卷区考查内容卷区考查内容卷区考查内容全国卷Ⅰ·27(2)(3)H2S的尾气处理、H2O2的氧化性全国卷Ⅰ·27焦亚硫酸钠(Na2S2O5)的制取及测定全国卷Ⅰ·12围绕Na2S2O3的元素推断全国卷Ⅱ·10CNa2S2O3溶液与稀盐酸的反应全国卷Ⅱ·11DSO2与O2的可逆反应全国卷Ⅰ·28以H2S为载体的化学反应原理全国卷Ⅱ·11CNa2O2在空气中的变化全国卷Ⅱ·26闪锌矿(ZnS)制备金属锌的工艺流程全国卷Ⅱ·7D人体必需的微量元素硒全国卷Ⅱ·12硫化镉(CdS)的沉淀溶解平衡全国卷Ⅱ·35硫及其化合物的结构与性质全国卷Ⅱ·9DO2和S单质氧化性的比较全国卷Ⅱ·26重晶石制备立德粉(ZnS·BaSO4)的工艺流程及S2-的“碘量法”测定全国卷Ⅲ·8B等质量的氧气和臭氧的电子数全国卷Ⅱ·28河水中溶解氧的测定全国卷Ⅲ·12B·DH2O2的分解反应、少量SO2气体的制取全国卷Ⅲ·26Na2S2O3晶体中杂质的检验及纯度的测定全国卷Ⅲ·11全固态锂硫电池北京卷·28SO2与AgNO3溶液的反应的实验探究北京卷·11Na2SO3溶液pH随温度变化的原因实验探究全国卷Ⅲ·26(3)硫酸亚铁热分解产物的实验探究天津卷·2CSO2使酸性KMnO4溶液褪色的离子方程式北京卷·27含硫物质热化学循环实现太阳能的转化与存储北京卷·10SO2与不同溶液的反应江苏卷·3B·C稀硫酸、SO2的性质及用途天津卷·4C·D难溶硫化物的溶度积、SO2-4的检验天津卷·10H2S和SO2的工业去除方法江苏卷·6CSO2与过量氨水的反应天津卷·7(4)浆状Mg(OH)2使燃煤脱硫江苏卷·4SO2的制取、性质检验、尾气处理的实验江苏卷·9C硫及其化合物的转化江苏卷·15SO2与O2反应的化学平衡计算江苏卷·10H2O2分解速率的影响因素探究江苏卷·21(2)SO2-4的空间构型江苏卷·19(3)由Na2CO3制备无水Na2SO3江苏卷·13BNa2SO3是否被氧化的检验
三、典型例题解析
1.氧族元素与阿伏加德罗常数相结合的考查
阿伏加德罗常数题为高考题型的热点,其知识涉及面广,隐含陷阱多,是基本概念、基本理论、定量计算的结合,考查学生分析问题、解决问题的能力。
【例1】设NA为阿伏加德罗常数的值,下列说法正确的是
( )
①(2019·浙江·19)2.3 g Na与O2完全反应,反应中转移的电子数介于0.1NA和0.2NA之间
②(2019·全国卷Ⅱ·11)密闭容器中,2 mol SO2和1 mol O2催化反应后分子总数为2NA
③(2018·浙江·20)32 g硫在足量的氧气中充分燃烧,转移电子数为6NA
④(2015·全国卷Ⅰ·8)2 L 0.5 mol/L亚硫酸溶液中含有的H+个数为2NA
⑤(2015·全国卷Ⅰ·8)过氧化钠与水反应时,生成0.1 mol氧气转移的电子数为0.2NA
⑥(2014·江苏·6)1.6 g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA
⑦(2014·广东·10)56 g铁片投入足量浓H2SO4中生成NA个SO2分子
⑧(2012·海南·7)1.0 L的0.1 mol/L Na2S溶液中含有的S2-离子数为0.1NA
【答案】⑤⑥
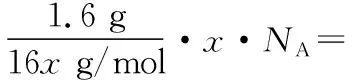
2.氧族元素和化学基本反应原理相结合的考查
物质的制取及物质间的转化、化学方程式、离子方程式、离子的检验等化学基本反应原理是历年考试的重点,氧族元素中主要以含硫化合物为主进行考查。
【例2】下列有关氧族元素及其化合物的说法正确的是
( )
①(2019·全国卷Ⅱ·10)向盛有饱和硫代硫酸钠溶液的试管中滴加稀盐酸,有刺激性气味气体产生且溶液变浑浊

③(2019·全国卷Ⅲ·12)在过氧化氢溶液中加入少量MnO2以加快氧气的生成速率
④(2019·全国卷Ⅲ·12)向饱和亚硫酸钠溶液中滴加浓硫酸制备少量二氧化硫气体

⑥(2019·江苏·3)SO2具有氧化性,可用于纸浆漂白
⑦(2019·江苏·6)SO2与过量氨水反应生成(NH4)2SO3
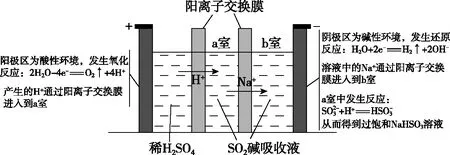
⑨(2018·天津·4)向含有ZnS和Na2S的悬浊液中滴加CuSO4溶液,生成黑色沉淀,则说明Ksp(CuS) 【答案】①③④⑦ 3.氧族元素和电化学相结合的考查 2019年诺贝尔化学奖用于奖励锂离子电池的发展。作为高考试题的“宠儿”,已出现过锂硫电池、锂-空气电池等,这类试题材料陌生度高,图文结合信息量大,综合性强。化学电源的试题定会再次热起来。 ( ) B.电池工作时,外电路中流过0.02 mol电子,负极材料减重0.14 g C.石墨烯的作用主要是提高电极a的导电性 D.电池充电时间越长,电池中的Li2S2量越多 【答案】D 【解题思路】由工作原理图可得:Li+向电极a移动,电极a为正极。列表如下: 电池总反应16Li+xS88Li2Sx(2≤x≤8)电极名称电极材料电极反应电极a:正极掺有石墨烯的S8材料S8+2e-+2Li+Li2S83Li2S8+2e-+2Li+4Li2S62Li2S6+2e-+2Li+3Li2S4Li2S4+2e-+2Li+2Li2S2电极b:负极金属锂Li-e-Li+ 4.氧族元素和化学实验相结合的考查 SO2因其独有的化学性质多样性(氧化性、还原性、漂白性等)而备受青睐,涉及SO2的试题能考查的知识包括:气体的制取与净化、气体性质的检验、尾气处理、实验方案的设计、化学反应实质的探究等。 【例4】(2019·北京·28)化学小组实验探究SO2与AgNO3溶液的反应。 (1)实验一:用如下装置(夹持、加热仪器略)制备SO2,将足量SO2通入AgNO3溶液中,迅速反应,得到无色溶液A和白色沉淀B。 ①浓H2SO4与Cu反应的化学方程式是____________________。 ②试剂a是________。 (2)对体系中有关物质性质分析得出:沉淀B可能为Ag2SO3、Ag2SO4或二者混合物。(资料:Ag2SO4微溶于水;Ag2SO3难溶于水) 实验二:验证B的成分。 ①写出Ag2SO3溶于氨水的离子方程式:____________________。 ②加入盐酸后沉淀D大部分溶解,剩余少量沉淀F。推断D中主要是BaSO3,进而推断B中含有Ag2SO3。向滤液E中加入一种试剂,可进一步证实B中含有Ag2SO3。所用试剂及现象是_________________ 途径1:实验一中,SO2在AgNO3溶液中被氧化生成Ag2SO4,随沉淀B进入D。 ①向溶液A中滴入过量盐酸,产生白色沉淀,证明溶液中含有________;取上层清液继续滴加BaCl2溶液,未出现白色沉淀,可判断B中不含Ag2SO4。做出判断的理由:________________________________________。 ②实验三的结论:_________________ (4)实验一中SO2与AgNO3溶液反应的离子方程式是__________________________。 (6)根据上述实验所得结论:_________________ (3)①Ag+;Ag2SO4的溶解度大于BaSO4,取上层清液加BaCl2溶液,未出现白色沉淀,必定没有Ag2SO4 5.以含硫化合物为载体的化学反应原理大题的考查 非选择题中的陌生物质的出现,会使考生心理更紧张,在复习的过程中,应让学生尽可能多的接触一些高中教材外的物质,掌握归类方法,避免形同“陌”路,则能遇“陌”不难。 【例5】(2018·全国卷Ⅰ·27)焦亚硫酸钠(Na2S2O5)在医药、橡胶、印染、食品等方面应用广泛。回答下列问题: (1)生产Na2S2O5,通常是由NaHSO3过饱和溶液经结晶脱水制得。写出该过程的化学方程式:____________________。 (2)利用烟道气中的SO2生产Na2S2O5的工艺: ①pH=4.1时,Ⅰ中为________溶液。(写化学式) ②工艺中加入Na2CO3固体,并再次充入SO2的目的是_________________ (3)制备Na2S2O5,也可采用三室膜电解技术,装置如图所示,其中SO2碱吸收液中含有NaHSO3和Na2SO3。阳极的电极反应式为________________________。电解后,________室的NaHSO3浓度增加。将该室溶液进行结晶脱水,可得到Na2S2O5。 (4)Na2S2O5可用作食品的抗氧化剂。在测定某葡萄酒中Na2S2O5残留量时,取50.00 mL葡萄酒样品,用0.010 00 mol·L-1的碘标准液滴定至终点,消耗10.00 mL,滴定反应的离子方程式为 , 该样品中Na2S2O5的残留量为________g·L-1(以SO2计)。 (2)①NaHSO3②得到过饱和NaHSO3溶液 ①pH=4.1时,Ⅰ中为NaHSO3溶液;②主要目的是得到过饱和NaHSO3溶液。(3)对电解原理进行分析: 大题中涉及的化学计算题通常被部分考生直接“跳过”,究其原因,是思维不发散、计算能力不过关导致,在复习中,应加强化学计算能力的培养。 【例6】(2018·全国卷Ⅲ·26)利用K2Cr2O7标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下: ①溶液配制:称取1.200 0 g某硫代硫酸钠晶体(M=248 g·mol-1)样品,配成100 mL样品溶液; 【答案】95.0 0.009 5 mol·L-1×20.00×10-3Ly xx 【答案】80ab 在历年的高考题中,涉及考查氧族元素的试题考查内容丰富,基础性强,形式新颖,充分体现了高考试题的基础性和创新性。由于文章篇幅及笔者水平有限,仅从这六个方面列举了近几年的高考试题,各位读者可参考近几年高考真题,认真研读,切实突破高考中涉及氧族元素的考查。