心肌细胞外泌体microRNAs 治疗心血管疾病的作用
陈琮
( 香港大学深圳医院 广东 深圳 510000)
心血管疾病(C V D)仍然是全世界发病率和病死率的主要病理原因[1]。心血管缺血性疾病(CVID)或缺血性心脏病(IHD),例如急性心肌梗塞(MI),心肌缺血/再灌注(MIR)损伤和心力衰竭,在缺血区产生大量的活性氧(R O S)[2],这是心肌细胞坏死/凋亡和死亡的主要因素,并加剧了心脏病。心肌梗死后心脏显示出内源性心肌细胞更新的潜力有限,这导致不可逆转的大量心肌细胞丢失,导致左心室重构和进行性心力衰竭[3]。MI 患者的主要治疗选择是减少梗死面积和心肌损伤,诱导受损心肌的置换或改善其修复,以及减少心肌重塑。在过去的几年中,再生医学已被公认对预防和治疗心脏病有效[4]。具有再生潜力的干/祖细胞移植已被确立为一种有前途的C V D 治疗方法,可替代凋亡或死亡的心肌细胞并增强收缩力[5]。这些细胞包括胚胎干细胞(E S C),诱导多能干细胞(i P S C),间充质干细胞(M S C)和心脏干祖细胞。通过输注和/或心肌内注射将干细胞移植到心脏中已被用于治疗冠状动脉疾病,心肌梗死和心力衰竭,其中它可以促进心脏的修复和再生,并增强患有以下疾病的患者的心脏功能:遵循MIR 的CVD 和动物模型[6]。尽管取得了这些令人鼓舞的结果,但仍存在一些缺点,例如需要稳定地提供具有稳定表型的细胞,由移植的细胞滞留在肺微脉管系统中引起的输注毒性,低存活率和向新功能心肌细胞的分化能力差,免疫排斥和致瘤性,异位组织的形成,这些细胞的产生和处理的高成本和延迟以及道德和安全挑战是临床实践中的主要问题[7]。
1.资料与方法
整合系统生物学和人类工程心脏组织(hECT)技术,对外泌体microRNA 分析数据进行偏最小二乘回归分析,用多种细胞类型的条件培养基处理。描述性统计数据以平均值表示,比较统计方法在相应的图例中进行描述。P<0.05 被认为具有统计学意义。
2.结果
在此分析中,亲代细胞包括hMSCs,人成年心脏成纤维细胞和人包皮成纤维细胞(h F F),这些化合物先前已建立对hECT 收缩力的亲代细胞依赖性旁分泌作用。更具体地说,尽管通过不同的机制介导,来自hMSCs 和人类成年心脏成纤维细胞的条件培养基而非hFFs 显着增加hECT 的收缩功能图1。尽管h M S C 外泌体是通过上述机制增加收缩力的主要贡献者,成年心脏成纤维细胞可溶性因子(例如转化生长因子-β)在很大程度上通过肥大以及钠和钾通道重塑来增加收缩力。最终结果预测microRNA-21-5p(miR-21-5p)水平与hECTs 中的收缩力和钙处理基因表达反应呈正相关。此外,与未处理的对照组相比,在用富含h M S C 分泌蛋白的外泌体部分(hMSC-exo)处理的hECT 中,miR-21-5p 水平显着升高,见图2。这激发了实验测试m i R-21-5p 在h M S C 外源介导的心脏组织收缩性增加中的人类特异性作用。
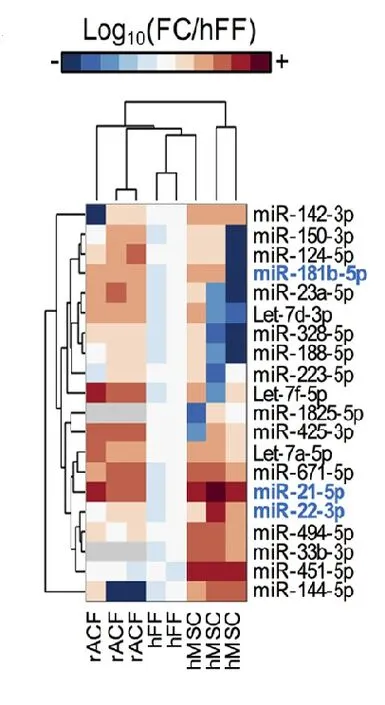
图1 人类成年心脏成纤维细胞表达
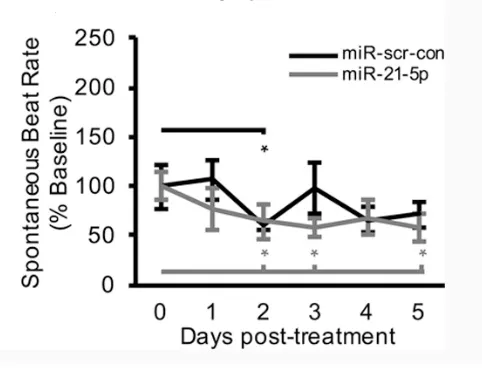
图2 hECTs 的心跳率,*P <0.05
3.讨论
在基于h M S C 的心脏治疗中,心肌收缩性的分子介体仍未解决,从而阻碍了最大化治疗功效的努力[3]。在这项研究中,我们使用集成的系统生物学和组织工程学方法来鉴定关键的心脏活性外泌体m i R s。首先,我们提供生物信息学和实验数据来支持miR-21-5p 在基于hMSC 的旁分泌信号治疗中作为领先的心脏主动外泌体miR[6]。接下来,使用hECT系统,我们提供了人类特异性实验数据,揭示了(1)m i R-21-5p 对h E C T 收缩功能的影响与h M S C-e x o 的作用非常相似,并且除去hMSC 中的miR-21-5p 可减少外泌体的促收缩作用。在mRNA 和蛋白质水平上均支持miR-21-5p 对钙处理和收缩力的作用。最后,我们以机械方式支持m i R-21-5p通过P I3K 信号级联反应增加钙的处理,从而增加收缩力。可庆的是,生物信息学已成功地用于研究干细胞疗法的促血管生成,抗纤维化和免疫调节旁分泌机制[5]。
综上所述,miR-21-5p 可能通过PI3K 信号传导在hMSC外源介导的对心脏收缩力和钙处理的作用中起关键作用。这些发现可能为利用m i R-21-5p 在优化未来基于干细胞的心血管疾病治疗中的作用开辟新的研究途径。

