发生骨折的6 例早产儿代谢性骨病临床分析
刘英丽 周 琳 张永红 谭金童 赵冬莹 许 敏 夏红萍
上海交通大学医学院附属新华医院(上海 200092)
早产儿代谢性骨病(metabolic bone disease of prematurity,MBDP)最早由英国儿科协会营养学组提出[1],其发生与钙、磷等矿物质代谢异常及维生素D3、甲状旁腺素异常分泌有关。MBDP以骨矿含量减少为特征,影像学表现为骨质变薄、骨密度下降,严重时出现长骨和肋骨的脆性骨折[2-4]。在早产儿救治过程中,类固醇、袢利尿剂及甲基黄嘌呤等药物的应用,致钙磷排泄增加,使骨矿化不足加重[4]。国外文献报道,随着人们对营养关注度的不断提高,MBDP的发病率从1987年的50%降至2009年的15%[4]。近年来,随着国内新生儿重症救治技术的发展,极低出生体质量(very low birth weight,VLBW)早产儿的病死率明显下降,MBDP 病例报道亦逐渐增多。本文回顾分析6 例发生骨折的MBDP患儿的临床资料,探讨MBDP的危险因素、临床表现、诊断和治疗方法。
1 临床资料
2016 年1 月至2020 年4 月,上海交通大学医学院附属新华医院新生儿重症监护病房(NICU)的住院早产儿中,通过临床表现、X 线特征及生化指标检测确诊代谢性骨病合并骨折患儿6例。通过电子病历系统查阅患儿的临床资料,包括性别、胎龄、出生体质量、入院日龄、单胎/多胎、出生方式、生后用药情况、使用肠外营养时间、并发疾病、实验室检查、X线表现及代谢性骨病的治疗情况等。
MBDP 诊断标准[4-6]:①早产儿有类似佝偻病样临床表现;②血碱性磷酸酶(ALP)> 900 IU/L和/或血磷< 1.8 mmol/L;③X线表现为肋骨软化、长骨骨折等。X线检查分级:0级,正常骨骼;1级,仅有骨质减少;2级,骨质减少加干骺端模糊呈杯口样改变,骨膜下新骨形成等佝偻病样表现;3 级,具备2 级表现,外加骨折[7-8]。
本组6 例患儿均因早产儿视网膜病(retinopathy of prematurity,ROP)由外院转来。患儿的临床资料见表1。男5 例、女1 例。2 例为单胎,4 例为双胎或三胎。6例患儿中位胎龄为27.1(26.5~29.2)周,出生体质量为900.0(857.5~1 125.0)g。例6 因双胎输血综合 征,出生时为小于胎龄儿;另5 例出生体质量均位于P10~P90,除例2 外,其余4 例在入本院时体质量均<P3,提示发生宫外生长发育迟缓。6例患儿生后即予肠外营养,肠内营养开始时间为生后3~10天。例2因合并坏死性小肠结肠炎(necrotizing enterocolitis,NEC),肠外营养时间相对较长,6 例患儿完全达肠内营养的中位时间为75.5(68.3~100.3)天。6例患儿均合并支气管肺发育不良(bronchopulmonary dysplasia,BPD)。例1 在外院已诊断左股骨骨折,其余5 例在本院诊断骨折,其中左股骨1 例、左肱骨1 例、多发性肋骨骨折1例,股骨合并肱骨骨折2例,右肱骨骨折1例。6例患儿血磷水平为1.55(1.43~1.65)mmol/L,血ALP水平为840.0(664.5~1047.5)IU/L,血钙均在正常范围。
本组6 例患儿均无外伤等诱因下发生骨折,X 线的表现情况见图1。例1,出生61 天外院诊断左股骨骨折,89 天入院X 线检查显示左股骨陈旧性骨折(图1A)。例2,出生后120天X线显示肋骨前端膨大,左肱骨骨痂形成,左股骨皮质不连续伴明显骨膜反应(图1B、1C);例3,生后89天入院X线显示左肱骨陈旧性骨折(图1D);例4,生后136天X线显示左5-8肋陈旧性骨折(图1E);例5,生后97天X线显示右肱骨骨折(图1F)和左股骨骨折(图1G);例6,生后66天入院X线显示右肱骨骨折(图1H)。

表1 6例代谢性骨病患儿临床特征
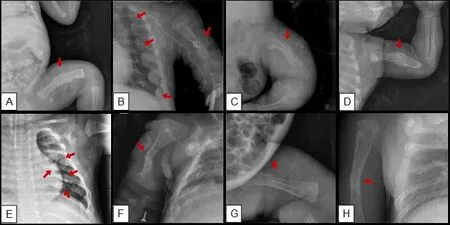
图1 患儿X 片表现
住院过程中积极给予补充钙、磷及维生素D3治疗,骨折患肢制动,动态监测生化指标,患儿未出现新的骨折,临床状况逐渐好转出院。
2 讨论
钙和磷通过胎盘的主动转运在胎儿骨骼矿化过程中起到重要作用,多达80%的矿物质转运发生在妊娠晚期,因此早产儿发生MBD 的风险高[9]。一项对336例胎龄≤31周、出生体质量≤1 500 g的早产儿的研究发现,MBDP 的发生与胎龄、出生体质量呈负相关[10]。早产儿尤其是极低和超低出生体质量儿,由于胃肠道发育不成熟,发生NEC的风险高,需要较长时间的肠外营养,如果肠外营养液的钙磷含量添加不足,则会引起骨代谢异常[11]。肠外静脉营养持续时间越长(持续超过4 周),骨矿物质含量越低,MBDP 的发生风险越高[12]。发生MBDP的另一因素是早产儿骨负荷过低[2]。对骨和关节的机械性牵拉可使骨负荷增加,成骨细胞活动增强,促进骨的形成。早产儿生后由于肌张力低和韧带松弛,自发运动减少,影响骨形 成;生后接受适当的被动运动可增加骨形成和骨矿化[13]。长期机械通气使患儿肢体主动和被动运动受限,致骨负荷过低,影响骨形成,增加骨折风险[14]。骨软化和/或肋骨骨折后,胸壁顺应性增加,进一步影响呼吸运动[4]。超早产儿病情复杂、危重,因病情需要使用类固醇、袢利尿剂、甲基黄嘌呤等药物,致钙磷排泄增加,使骨矿化不足加重,进一步增高MBDP 的发生风险。本组6例患儿中,5例胎龄<29周,1例胎龄>32周,出生体质量均<1 200 g,合并ROP、BPD和NEC等早产儿常见并发症。有利尿剂使用史3 例,同时使用激素和氨茶碱2 例,使用枸橼酸咖啡因2 例,激素1 例,使用呼吸机时间均≥30天,肠外静脉营养时间均>60天。这些发生MBDP的高危因素与文献报道相符。
MBDP的诊断通常将临床表现、实验室检查及影像学检查相结合以明确,但具体的生化指标及诊断阈值尚缺乏共识。MBDP 的临床表现一般于生后6~12周开始出现,通常骨皮质变薄等放射学特征容易被忽视,严重时出现骨折,局部可出现疼痛、肿胀及局部变形[3]。由于血钙、磷和ALP 可经常监测,用于筛查MBDP[15]。美国儿科学会AAP 指南建议,MBDP 的筛查从生后4~6周开始,每1~2周对所有早产儿进行血清钙、磷和ALP 水平监测[15]。然而,因血钙水平较低时,机体可通过骨钙的动员和释放来维持正常的血钙水平,故血钙不能用于代谢性骨病的诊断指标。大部分研究将ALP>900 IU/L和/或血磷<1.8 mmol/ L作为临床诊断MBDP的重要指标[4-6]。相关研究显示,作为严重MBDP的标志物,甲状旁腺激素(PTH)升高比ALP升高更敏感(71%对29%),特异性相似(88% 对93%)[16];当联合低血磷时,PTH升高在识别MBDP时有100%的敏感度和94%的特异性[4]。最近,有研究提出,ALP>500IU/L,磷<1.8mmol/L,可用于初始筛查标准[17]。本研究中,例2、例6ALP>900 IU/L,6例患儿血磷均<1.8 mmol/ L,结合临床病史、X线表现,故诊断为MBDP。
关于MBDP的辅助检查,双能X线吸收法(DEXA)对早产儿微小的骨密度改变敏感,但因有辐射性,且缺少具体标准,临床应用有一定的局限。定量超声法(QUS),通过超声的传播速度(SOS)测量骨密度,无放射性,操作简便且低成本,是有潜力的非侵入性检测方法,可广泛用于早产儿骨密度的评估,但目前尚无明确的早产儿骨密度正常值。
对于早产儿矿物质摄入标准,美国儿科学会(AAP)推荐为:钙150~220 mg/(kg·d)、磷60~140 mg/(kg·d)[18]。2013 中国新生儿营养支持临床应用指南指出,早产儿肠外营养期间每日所需钙为0.6~0.8 mmol/(kg·d),磷为1.0~1.2 mmol/(kg·d)[19]。最近,欧洲儿科胃肠肝病和营养协会(ESPGHAN)指南建议,早产儿钙与磷酸盐比例为1.3:1[20]。早产儿配方奶每100 kcal中含钙元素152 mg、磷90 mg,需要全胃肠道喂养热卡100 kcal/(kg·d)才达到美国生命科学研究组织(LSRO)推荐的钙磷摄入量。维生素D3的需求受出生时机体储备量的影响,而且母亲维生素D3缺乏、早产儿、长期住院致日光照射减少均影响患儿维生素D3的状态。欧洲儿科胃肠和营养指南建议,对于极低出生体质量儿,补充维生素D3200~400 IU/d;当体质量> 1.5 kg,增加到400 IU/d,直到体质量超过3 kg[21]。2014年我国拟定的维生素D3缺乏及维生素D3缺乏性佝偻病防治建议推荐:维生素D3的预防剂量为400~800 IU/d,早产儿、低出生体质量儿、双胎儿建议为800~1 000 IU/d[22]。本资料中6例患儿因病情复杂,喂养受限,口服补充维生素D3时间较晚。一旦诊断患儿发生MBDP 后,应及时给予补充维生素D3和钙、磷。另外,为改善骨矿化,住院期间积极进行床边康复训练,进行抚触及给予适当被动运动等治疗。
综上所述,极低出生体质量儿使用影响体内矿物质的药物、长期使用呼吸机、静脉营养、合并NEC 及BPD 等,易发生MBDP。在临床工作中,对VLBW 儿生后4~6周开始,定期进行血清钙、磷和ALP等监测,及时诊断MBDP。治疗方面尽量减少机械通气时间,尽早全胃肠道喂养,减少静脉营养时间,尽早补充维生素D3和钙、磷制剂,适当进行NICU床旁被动活动,对预防骨质减少、改善MBDP、避免骨折的发生有积极作用。

