少见细胞色素P450 2C9 等位基因对中国汉族心房颤动患者华法林稳态剂量的影响及预测模型的构建
华法林是目前临床应用最广泛的口服抗凝药[1-2],其临床证据坚实充分,适应证广泛,且经济、易于拮抗;然而,其缺点也显而易见,如治疗窗窄、稳态剂量个体差异大且易与多种药物发生相互作用等[1]。不当的给药剂量可能会导致严重出血事件发生[3]。因此应用华法林时需要频繁监测国际标准化比值(INR)来调整剂量,以达到最佳的抗凝效果。许多遗传和临床因素与华法林稳态剂量的变异性相关[4]。大量研究已经证实,基因多态性,主要包括细胞色素P4502C9(CYP2C9)和维生素K 环氧化物还原酶复合体1(VKORC1)相关的突变在华法林稳态剂量变异性中起到重要作用[5-7]。
VKORC1的几种单核苷酸多态性位点(rs7196161,rs9923231,rs9934438,rs8050894和rs2359612)存在高度连锁不平衡[5]。其中,VKORC1-1639G/A(rs9923231)是重要的基因多态性位点。与此同时,迄今已发现62种CYP2C9等位基因,CYP2C9等位基因在不同人群中的分布存在明显差异[7]。CYP2C9*3 为亚洲人群最常见的突变类型,而CYP2C9*2 则极为罕见[8]。近年来在汉族人群发现了多种少见CYP2C9基因突变型,如CYP2C9*13、*16、*36、*39、*43、*45、*60 等,其基因频率与CYP2C9*2 相当,而其功能表达——CYP2C9 酶的活性在体外和体内实验中被证明较野生型明显降低[9-11]。继而可能对临床患者的华法林稳态剂量产生潜在影响。现有的华法林稳态剂量预测模型中CYP2C9基因多仅纳入CYP2C9*2 和CYP2C9*3 突变作为变量[4,12-14]。基因的异质性使得源自其他种族得出的华法林稳态剂量模型无法有效地适用于中国汉族人群。本研究基于汉族人群CYP2C9等位基因分布特点,结合其他遗传和非遗传因素,建立华法林稳态剂量模型,探究除CYP2C9*2 和CYP2C9*3以外的少见CYP2C9等位基因对中国汉族心房颤动(房颤)患者华法林稳态剂量的影响。
1 资料与方法
选取2011 年1 月至2017 年3 月于北京医院就诊的中国汉族房颤患者681 例。入选标准:年龄≥18 岁,满足抗凝治疗适应证,同意接受华法林抗凝治疗≥3 个月。排除标准:血压≥170/110 mmHg(1 mmHg=0.133 kPa),合并活动性出血,凝血功能异常、恶性肿瘤以及合并妊娠。随机将所纳入样本以2:1 的比例分为建模组(n=454)和验证组(n=227),详细记录患者统计学及临床资料,包括:年龄、性别、身高、体重、吸烟情况、血肌酐水平、合并用药情况(他汀类药物、胺碘酮);以及华法林稳态剂量:即在启动口服华法林治疗≥7 d 后,在华法林周给药剂量不变的情况下,患者至少连续2 次(间隔至少7~14 d)血INR 处于目标范围(2.0~3.0)时患者口服华法林的平均日剂量值(mg/d,即周剂量/7 d)[4]。本研究获得北京医院伦理委员会批准。全部患者签署知情同意书。
主要试剂:DNA 聚合酶及扩增缓冲液(TakaRa公司,日本);DNA 相对分子质量梯度标准Marker(TakaRa 公司,日本);PCR 扩增引物(北京天一辉远生物工程公司);E.Z.N.A 凝胶回收试剂盒(Omega Biotek 公司,美国);DTCS QuickStart DNA 测序试剂盒(Beckman Coulter 公司,美国);虾碱性磷酸酶(Promega 公司,美国);核酸外切酶I(NEB 公司,美国);重组凝血酶原试剂(IL 公司,意大利)。
主要仪器:ABI-9700 型PCR 仪(ABI 公司,美国);电泳仪及水平电泳槽(北京市六一仪器公司)、凝胶成像系统(上海复日公司)、CEQTM8000 测序仪(Beckman Coulter 公司,美国)、UV200 紫外分光光度仪(岛津公司,日本)。
DNA 的提取:收集每例患者外周静脉血2 ml,以乙二胺四乙酸(EDTA)抗凝,采用盐析法提取基因组DNA,置于-20 ℃冰箱内保存。根据人CYP2C9和VKORC1已知基因组序列及基因多态性,参照相关文献,采用聚丙烯酰胺凝胶电泳(PAGE)回收纯化方式,由北京天一辉远生物工程公司合成扩增用引物和测序用引物。扩增引物序列见表1。

表1 CYP2C9 和VKORC1 基因扩增引物序列
PCR 扩增:采用50 μl 的反应体系,内含:2×Taqmix(包括缓冲液、DNA 聚合酶、脱氧核糖核苷三磷酸)25 μl,100 ng 的基因组DNA 以及0.2 μmol/L 的上、下游引物,加双蒸水(ddH2O)定容至50 μl。PCR 扩增循环参数如下:95℃预变性5 min,94℃变性30 s,60℃退火30 s,72℃延伸30 s,35个循环后再延伸5 min。PCR 产物用0.8%琼脂糖凝胶电泳进行检测,验证扩增产物。
DNA 产物测序分析:取PCR 扩增产物5 μl,与4.8 U 虾碱性磷酸酶及1.5 U 核酸外切酶Ⅰ混合,于37℃反应30 min,后85℃维持20 min。将纯化后的测序产物放入CEQTM8000DNA 测序仪,输出测序结果经DNAstar6.0 和Chromas 软件进行分析。
统计学方法:所有数据用SPSS 25.0 软件分析。采用直接计数法计算各等位基因和基因型频率,χ2检验确定是否符合Hardy-Weinberg 遗传平衡定律。计量资料用均值±标准差()表示,计数资料用百分比(%)表示。主要参数均进行正态性检验,如不服从正态分布,则进行自然对数转换后再进行正态性检验;如仍不符合正态分布则采用非参数检验。各组间等位因与基因型频率的比较采用χ2检验。组间华法林剂量平均值比较采用独立样本t检验,计量资料与华法林剂量的相关性采用Pearson 相关性分析。采用单因素线性回归分析筛选与华法林稳态剂量相关的遗传和临床变量,进行多元线性回归分析,建立预测方程。P<0.05 为差异有统计学意义。
2 结果
2.1 研究对象基线特征(表2)
681 例患者中男性458 例,女性223 例,平均年龄(68.0±10.2)岁。用药情况方面,单独应用华法林403 例(59.2%),合并使用华法林和他汀类药物120 例(17.6%),合并使用华法林和胺碘酮122例(17.9%),合并使用华法林、他汀类药物和胺碘酮36 例(5.3%)。华法林稳态剂量范围为0.50~9.00 mg/d,平均稳态剂量为(3.34±1.18)mg/d。
2.2 CYP2C9 和VKORC1-1639 基因多态性对华法林稳态剂量的影响
经检验,研究人群CYP2C9和VKORC1-1639等位基因及基因型频率分布符合Hardy-Weinberg 平衡定律,具有群体代表性。
CYP2C9*1/*3 是研究群体中最常见CYP2C9的突变基因型,占9.3%,携带者平均华法林稳态剂量为(2.30±0.88)mg/d,显著低于野生型CYP2C9*1/*1[(3.47±1.13)mg/d,P<0.001]。CYP2C9*1/*2 和CYP2C9*3/*3 基因型携带者各1例,稳态剂量分别为2.50 mg/d 和0.50 mg/d。除CYP2C9*2 和CYP2C9*3 以外,本研究发现了6 种少见CYP2C9等位基因突变,包括CYP2C9*7、*13、*16、*29、*33、*16,均为杂合子,基因型频率为0.92%。其中3 种突变(CYP2C9*13、*16、*60)携带者的临床和药物遗传学信息被完整获取。这三种其他少见基因型CYP2C9*1/*13、CYP2C9*1/*16、CYP2C9*1/*60 平均华法林稳态剂量分别为(1.88±0.53) mg/d、1.39 mg/d、(1.00±0.35)mg/d,均低于CYP2C9*1/*1 及CYP2C9*1/*3 均值(P均<0.05)。将CYP2C9*1/*13、*16、*60 合并为变量CYP2C9(13/16/60),平均华法林稳态剂量为(1.42±0.54)mg/d,显著低于CYP2C9*1/*1(P<0.001)及CYP2C9*1/*3(P<0.05)。
对VKORC1-1639G/A 基因突变位点进行检测,AA 是主要的基因型,占总样本数的78.7%,GA 杂合子占总样本数的19.1%,GG 纯合子占总数的2.2%。AA 组华法林稳态剂量最低,为(3.07±0.87)mg/d,显著低于 GA 组[(4.27±1.37)mg/d]和GG 组[(5.59±1.84)mg/d],差异均有统计学意义(P均<0.001)。
2.3 CYP2C9 和VKORC1-1639 不同基因型组合对华法林稳态剂量的影响(表3)
将样本人群按照CYP2C9与VKORC1-1639G/A不同基因型组合进行分组,可以发现野生型基因型组合CYP2C9*1/*1 +VKORC1-1639AA 最为常见,占69.5%,平均华法林稳态剂量为(3.18±0.82)mg/d。各基因型组合稳态剂量与野生型组合相比较后的P值见表3。对于特定的CYP2C9基因型,华法林稳态剂量均值由VKORC1-1639AA 基因型至GA 型至GG 型逐渐升高。而对于特定的VKORC1-1639AA 基因型,CYP2C9突变型[*1/*3、*3/*3、CYP2C9(13/16/60)]的稳态剂量均值均低于野生型CYP2C9*1/*1(P均<0.01)。
表2 681 例患者的基线特征()
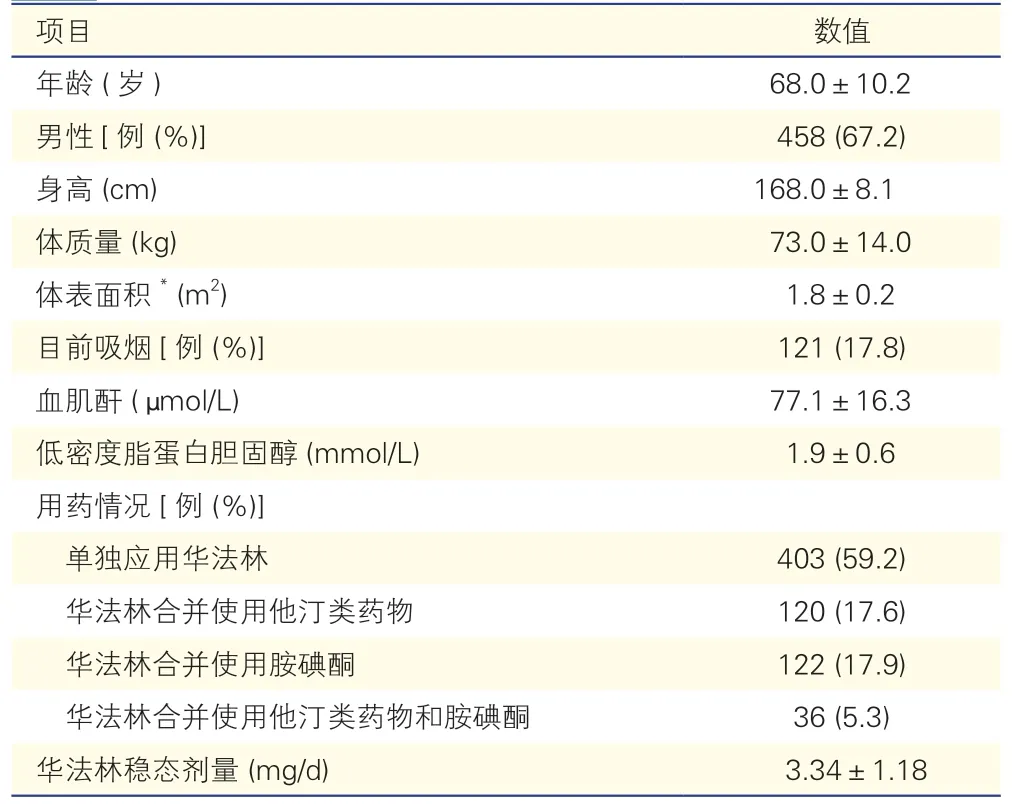
表2 681 例患者的基线特征()
注:*:体表面积计算参照Stevenson's 公式,即:体表面积(m2)=0.0061×身高(cm)+0.0128×体质量(kg)-0.1529
表3 681 例患者不同基因型组合华法林稳态剂量情况()

表3 681 例患者不同基因型组合华法林稳态剂量情况()
注:CYP2C9:细胞色素P450 2C9;VKORC1:维生素K 环氧化物还原酶复合体1。与CYP2C9*1/*1+VKORC1-1639AA 比△P<0.01
2.4 公式建立
对建模组454 例患者的遗传和非遗传变量进行单因素回归分析,其中体表面积、合并使用胺碘酮、CYP2C9*3、CYP2C9(13/16/60)、VKORC1-1639GA、VKORC1-1639GG 均被发现与华法林稳态剂量相关(P均<0.001)。其中,胺碘酮、CYP2C9*3、CYP2C9(13/16/60)与华法林稳态剂量之间呈负相关;体表面积、VKORC1-1639GA,VKORC1-1639GG 这3 个变量则与华法林稳态剂量呈显著性正相关。其余变量经初步分析与华法林稳态剂量之间的相关性均不显著(P均>0.05)。将上述6 个变量进一步纳入多元回归模型,进行分步回归分析,建立华法林稳态剂量预测模型,得到回归方程:华法林日剂量=exp[0.524+0.344×体表面积-0.082×胺碘酮-0.393×CYP2C9*3-0.740×CYP2C9(13/16/60)+0.276×VKORC1-1639GA+0.593×VKORC1-1639GG]R2=44.3%。本模型预测权重达44.3%,遗传因素的总预测权重达39.6%。由表4 可见,CYP2C9*3 是最重要的预测因子,可解释15.8%的剂量差异,而CYP2C9(13/16/60)占总基因频率的0.7%,可以解释6.3%的华法林剂量个体差异,VKORC1-1639G/A 共可解释17.5%的华法林稳态剂量个体差异。

表4 华法林稳态剂量多元线性回归模型
2.5 模型的验证
将验证组的227 例患者的临床及遗传信息代入本研究所建立的华法林稳态剂量预测模型,进行Pearson 相关性分析(图1)。本研究建立模型得到的相关系数r=0.567,其中55.5%的样本预测剂量与实际剂量的偏差小于20%。
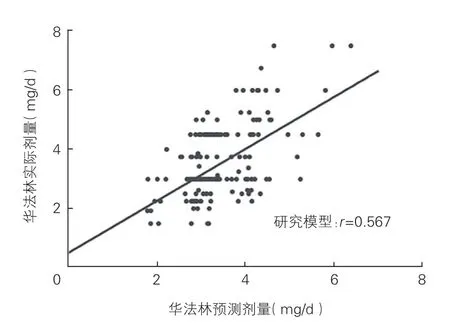
图1 验证组中华法林预测剂量与实际剂量关系
3 讨论
CYP2C9所编码的细胞色素P450 酶是更具药理活性的S-华法林消旋体代谢的关键酶。目前已发现62 种CYP2C9等位基因,CYP2C9等位基因在不同人群中的分布有着明显差异[7]。CYP2C9*3 是亚洲人群中最常见的等位基因突变,基因频率为2%~8%,而CYP2C9*2 则极为罕见[8]。本研究中CYP2C9*3 和CYP2C9*2 的基因频率与既往国内报道的基因频率相当[14-15]。CYP2C9基因多态性在华法林稳态剂量个体差异中发挥着重要的作用,本研究中CYP2C9*3 是最重要的遗传预测变量,其可解释约15.8%华法林稳态剂量变异性。
近年来,除CYP2C9*2 和CYP2C9*3 以外的少见CYP2C9基因型在华法林稳态剂量中的影响越来越受到重视。CYP2C9*5、*6、*8、*11 是其中研究最多的少见CYP2C9突变基因,并与低华法林稳态剂量密切相关[16-17]。它们在非洲人群中最为常见,基因频率可高达约8%~10%,但在东亚人群中却极为罕见[8,18]。在一项研究中,将少见基因突变CYP2C9*5、*6、*8、*11 纳入华法林稳态剂量预测模型,可增加了6%的华法林稳态剂量预测权重[19]。基于上述证据,2017 年临床药物基因组学实施联盟(CPIC)指南推荐,对于CYP2C9*5、*6、*8、*11 基因突变的携带者,应下调其初始华法林剂量15%~30%[1]。
目前国内尚未有将除CYP2C9*2 和CYP2C9*3以外的少见CYP2C9等位基因作为变量纳入华法林稳态剂量预测模型的报道。本研究共发现了CYP2C9*7、*13、*16、*29、*33、*60 共6 种少见CYP2C9等位基因,均为杂合子,上述突变基因频率均与CYP2C9*2 相当。国内2013~2015 年发表的几项研究[8-11],建立了汉族人群中最大的CYP2C9等位基因数据库,发现了除CYP2C9*2 和CYP2C9*3 以外的36 种CYP2C9等位基因,总等位基因频率达2.44%,其中27 种等位基因在体外实验中代谢活性较野生型明显降低,包括本研究中发现的CYP2C9*13、*16 和*60。CYP2C9*13 在2004 年首次于中国汉族人群中发现[20],是中国人群中较为常见的少见CYP2C9等位基因,基因频率达0.16%~0.70%[8,21]。多项体内和体外实验已经证明,CYP2C9*13 与更低的药物代谢活性相关[22-23]。此外临床上也发现带有CYP2C9*13 等位基因的个体有着更低华法林剂量需求[24]。CYP2C9*16 最早于2004 年在东南亚人群中被发现[25]。戴大鹏等[8]2013年的研究报道,CYP2C9*16 在汉族人群基因频率为0.19%。体内和体外实验也已经证明,CYP2C9*16与更低的药物代谢活性相关[9,15,26]。CYP2C9*60 首次于2015 年在对1 例极低华法林稳态剂量患者的研究中被发现,后续的体内和体外实验证明,它与更低的药物代谢活性相关[11]。本研究中6 种其他少见CYP2C9等位基因总基因型频率约为0.92%,低于戴大鹏等的报道。其中3 种少见基因突变(CYP2C9*13、*16、*60)携带者的临床和遗传信息被完整获取,并证实相关突变与低的华法林稳态剂量相关。根据汉族人群中CYP2C9等位基因特点,综合CYP2C9*13、*16、*60 三种少见基因型,我们建立了变量CYP2C9(13/16/60),平均稳态剂量显著低于CYP2C9*1/*1(P<0.001)及CYP2C9*1/*3(P<0.05)。这可能预示携带这些等位基因的患者有着更低的华法林剂量需求,按常规剂量给药可能会导致出血风险增高。CYP2C9(13/16/60)基因型频率共占0.7%,但可以解释6.3%的华法林剂量个体差异。尽管少见CYP2C9等位基因的基因频率较少,但考虑到中国有着约13 亿汉族人口,以及它们对华法林稳态剂量的显著影响,研究少见CYP2C9等位基因对华法林稳态剂量的影响对指导中国汉族房颤患者华法林个体化给药具有重要的意义。
VKORC1所编码的维生素K 环氧化物是维生素K 循环的关键酶和华法林作用的靶点[5]。rs9923231(-1639G>A)是常见的VKORC1基因多态性。VKORC1基因多态性与种族相关,亚洲人群中AA 基因型频率最高达86%,其次是欧洲人达37%,最低是非洲人达10%[5-6];而GG、GA 与更高的华法林稳态剂量相关[5]。这可能是亚洲人华法林稳态剂量较低的部分原因。本研究证实了以上发现,VKORC1-1639G/A 共可解释17.5%的华法林稳态剂量个体差异。本研究所建立模型中遗传因素的总预测权重达39.6%。
临床因素中,体表面积及胺碘酮的使用被纳入模型,其中体表面积与华法林稳态剂量呈正相关,而合并使用胺碘酮与华法林稳态剂量呈负相关。研究表明,胺碘酮及其代谢产物可能通过抑制CYP2C9 酶系统,减少华法林的代谢,从而降低华法林的稳态剂量[27]。
本研究纳入了681 例服用华法林预防血栓事件并达到稳态剂量的患者。基于药物因组学、人口统计学和临床资料,使用逐步回归分析,在汉族人群中首次将除CYP2C9*2 和CYP2C9*3 以外的其他少见CYP2C9基因突变作为变量,建立中国北方汉族房颤患者华法林稳态剂量预测模型,预测权重达44.3%。将得到的模型应用于验证组,结果优于国内外IWPC 模型[4]、Gage 模型[12]、Ohno 模型[13]和Miao 模型[14]。新模型未来如推广到临床,在指导和预测华法林的给药剂量、缩短INR 达标时间以及降低华法林过量风险等方面可能较现有的模型更具优势,当然这还需要进一步前瞻性临床试验的证实。
局限性:(1)发现少见CYP2C9基因例数较少,据此建立的模型方程难免存在偏倚,仍有待于进一步扩大样本量,把更多其他少见CYP2C9基因纳入模型,优化方程,探究对华法林稳态剂量的影响。(2)遗传因素仅纳入了CYP2C9和VKORC1基因,而近年来研究发现,其他遗传因素如CYP4F2、CYP2C19、GGCX、EPHX1、CALU等也与华法林稳态剂量相关[1,28-29]。(3)临床因素中仅有体表面积和胺碘酮的使用被纳入模型,预测权重低于国内外其他研究模型[12-14],以后还可以通过优化样本结构、丰富更多的临床信息,进一步完善模型。(4)本研究属于回顾性研究,其结果还需要前瞻性研究进行验证。
利益冲突:所有作者均声明不存在利益冲突

