贯叶马兜铃叶挥发性成分的地理变化及其潜在价值分析
于玉龙 耿宇鹏 常娜 陈高

摘 要:为探究贯叶马兜铃(Aristolochia delavayi)在不同地理居群挥发性成分含量的变化情况,该文采用固相微萃取-气质联用技术分析了来自五个不同地理区域的贯叶马兜铃叶的挥发性成分,并用气相色谱面积归一化法对各成分进行了定量。结果表明:四个贯叶马兜铃居群植株叶挥发性主成分均为癸烯醛,且占有较高比例。香格里拉三坝乡、丽江大具、楚雄铁锁乡和禄劝则黑乡四个居群植株叶中挥发性成分癸烯醛分别占挥发性成分检出总量的63.5%、79.3%、69.9%、79.6%,其中大具和禄劝两居群含量相对较高并且稳定性较好。分布在鹤庆黄坪的居群,检测出其挥发性主成分为乙酸龙脑酯(30.1%),但癸烯醛含量仅占4.5%,该结果与其他居群有明显差异。通过对该物种不同居群植株叶片挥发性癸烯醛含量的分析,确定了质量更好的种源,同时结合该植物所含马兜铃酸的情况,提出了健康安全的食用方式。该研究结果为合理开发贯叶马兜铃的经济价值及保护该濒危物种提供了技术指导和理论支持。
关键词:贯叶马兜铃,挥发性成分,癸烯醛,固相微萃取,气相色谱-质谱法(GC-MS)
中图分类号:Q946
文献标识码:A
文章编号:1000-3142(2020)09-1251-08
Abstract:In order to study the variation of volatile components from dried leaves of different Aristolochia delavayi populations,solid-phase microextraction followed by gas chromatography coupled with mass spectrometry detection was used to analyze the chemical composition of these plants. The relative amount of each compound was determined by area normalization method. The results showed that the main volatile component of dry leaves was (E)-2-Decenal,which accounted for 63.5%,79.3%,69.9%,79.6% of the total volatile components,detected in the four populations of Shangri-La,Lijiang,Chuxiong,Luquan,respectively. However,the samples belonging to the Huangping population,Heqing County,showed a different volatile component pattern. The main volatile component from this population was bornyl acetate (30.1%) and (E)-2-Decenal only accounted for 4.5%,which was significantly lower than that of in the samples of the other four populations,and the possible reasons for the difference were analyzed and discussed. By analyzing the content of volatiles components in the leaves of A. delavayi,we identified the excellent germplasm of A. delavayi. At the same time,the healthy and safe eating methods were put forward according to the situation of aristolochic acid contained in the plant. The study also provides technical guidance and theoretical support for rational use of this traditional medicinal plant species and protection this endangered species in China.
Key words:Aristolochia delavayi,volatile components,(E)-2-Decenal,solid-phase microextraction (SPME),gas chromatography-mass spectrometry (GC-MS)
貫叶马兜铃(Aristolochia delavayi)是马兜铃科马兜铃属多年生柔弱草本植物,因其叶基部心形而抱茎得名(中国科学院中国植物志编辑委员会,1988)(图1)。又因其植株本身常挥发有类似姜科植物草果的浓郁辛香气味,又名山草果(孙景梅等,2008;陈高等,2018)。该植物产于云南西北部及四川西南部的金沙江干热和干暖河谷中,主要生长在1 640~2 250 m的石灰岩山地、丘陵或河谷稀疏灌丛中,以及土层瘠薄、多砾石的黄壤地带(金振洲等,1994;Yang et al.,2014;和文佳等,2017),是我国马兜铃科马兜铃属的特有植物(Chen et al.,2015),同时也是一种拥有地域特色的野生食用香料资源(和文佳等,2010)。当地居民除了用以去除牛羊肉膻味的香料食用外,还广泛利用其叶作芳香健胃药以增进食欲或用于感冒、疟疾等药用(孙汉董等,1987)。由于当地居民经常用作香料使用,导致该物种的野外分布居群长期遭到采挖,再加上人类活动导致其生境的破碎化以及自然结实率低等自身生物学特性,致使其野生资源逐年减少,濒临灭绝。目前,贯叶马兜铃在《中国高等植物红色名录》和《世界自然保护联盟(international union for conservation of nature,IUCN)红色名录》中均被列为野生濒危物种(EN)(覃海宁等,2017)。
贯叶马兜铃特殊辛香气味来源于其挥发油中的主成分反式-2-十一碳烯醛(孙汉董等,1987;周铁生等,1995)。Li et al.(2013)
对其挥发油化学组分进行了详细的分析,结果在挥发油中共鉴定出95种组分,发现主成分为反式-2-癸烯醛并占总量一半以上;陈高等(2018)通过动态顶空吸附法结合GC-MS技术对贯叶马兜铃叶的挥发性成分进行了分析,结果表明反式-2-癸烯醛占分离出总挥发性成分的79.79%。因此,目前认为癸烯醛可能是贯葉马兜铃精油的主成分。周铁生等(1995)研究表明贯叶马兜铃精油中含有大量以反式-2-癸烯醛为主的2-烯脂肪醛类化合物,是传统辛香料植物相关含量的5倍,因为2-烯脂肪醛类香料是高档香精的增香剂,所以天然含有此化合物的贯叶马兜铃精油具有很高的经济价值。贯叶马兜铃精油不仅在香料香精生产中具有很高的发挥潜力,而且该精油和其主成分癸烯醛对常见的细菌和真菌均还具有一定的抗菌活性,这或许是一种潜在抗菌性产品开发的来源(Li et al.,2013)。
在对其野外居群调查中发现,由于贯叶马兜铃植株本身会在风吹或有其他扰动的情况下散发出浓烈的辛辣气味,这对我们在其生境中寻找为数不多的植株提供了帮助,同时发现不同地理区域植株所释放的挥发性气味略有不同。周铁生和杨庆宽(1995)研究已表明该植物的精油主要存在于叶片中,鉴于挥发性气味是挥发油的外在表现形式,且癸烯醛是贯叶马兜铃挥发油和叶挥发性气味的主成分,从而以贯叶马兜铃叶的挥发性成分中癸烯醛含量来表示精油的“质量”。因此,我们对不同地理区域的贯叶马兜铃叶挥发性气味成分进行分析,来探究贯叶马兜铃挥发性成分在不同居群间的特异性、稳定性和一致性。
本研究按照对材料处理的传统做法(陈佳龄等,2013;李美萍等,2019),采用固相微萃取-气质联用技术,对来自香格里拉三坝乡、丽江大具、鹤庆黄坪、楚雄铁锁乡和禄劝则黑乡五个不同地理居群的贯叶马兜铃植物叶片挥发性成分进行提取与分析,通过对不同居群植株叶挥发性成分稳定性和差异性的比较,筛选出稳定、高质量贯叶马兜铃精油的种源,为以后的合理开发、种植,充分利用其经济价值,以及为改变当地居民的传统食用方式和改善居民的健康状况提供科学依据。
1 材料与方法
1.1 材料
自五个不同地理区域的新鲜贯叶马兜铃叶片,具体采集信息见表1。材料采集后在相同的条件下自然阴干。
1.2 方法
1.2.1 固相微萃取(采集挥发性成分) 分别称取不同地理区域阴干的植物叶片3 g,剪碎后分别置于20 mL顶空萃取瓶里,每个萃取瓶中加入10 μL内标(二氯甲烷溶解的正壬烷720 ng),加磁性铁盖密封后进行萃取。插入65 μm DVB/PDMS萃取头于35 ℃顶空萃取45 min,于200 ℃汽化室解吸5 min。详细实验流程参考Chen et al.(2015)的方法进行GC-MS分析。为确定挥发性成分的稳定性,分别取同一居群的不同植株叶片各进行3次重复实验。
1.2.2 GC-MS分析 采用美国Agilent Technologies公司生产的HP6890GC/5973MS型气相色谱/质谱联用仪。气相色谱条件:HP-5MS石英毛细管柱(30 m × 0.25 mm × 0.25 μm);柱温起始为40 ℃,
保持5 min,程序升温5 ℃·min-1,至280 ℃;柱流量为1.0 mL·min-1;进样温度250 ℃;柱前压100 kPa;进样量1.0 μL;分流比10∶1;载气为高纯氦气。MS条件:电离方式EI,电子能量70 eV;传输线温度250 ℃;离子源温度230 ℃;四级杆温度150 ℃;质量扫描范围35~500 amu。
1.3 数据处理
采用Wiley7n.1谱库检索定性确认贯叶马兜铃叶的挥发性化学成分,按照峰面积归一化法计算出各化学成分的峰面积相对百分含量,并用正壬烷定量植物的自然释放量,同时用在Sigma购买的标准品比对主成分反式-2-癸烯醛的真实性。
2 结果与分析
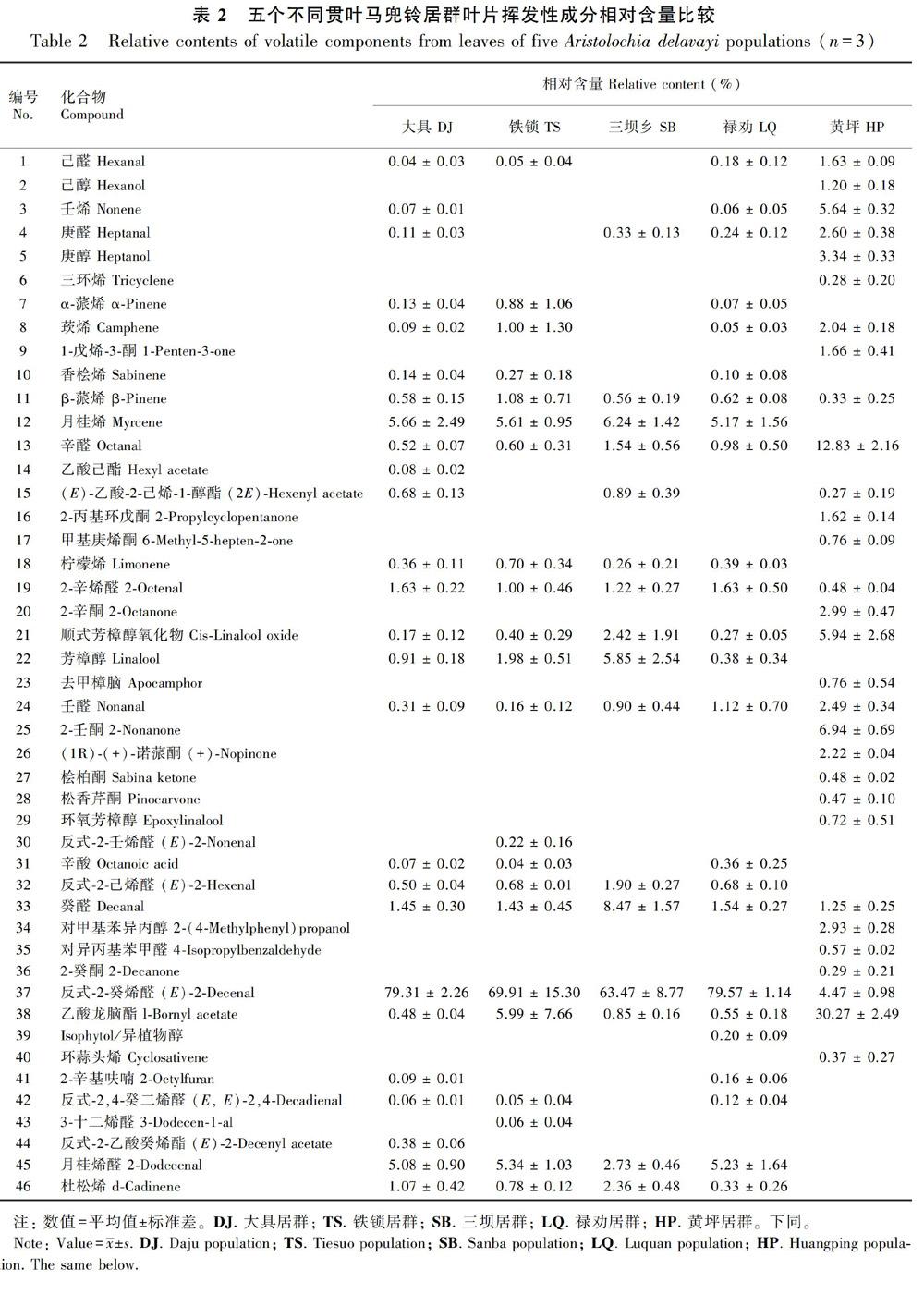
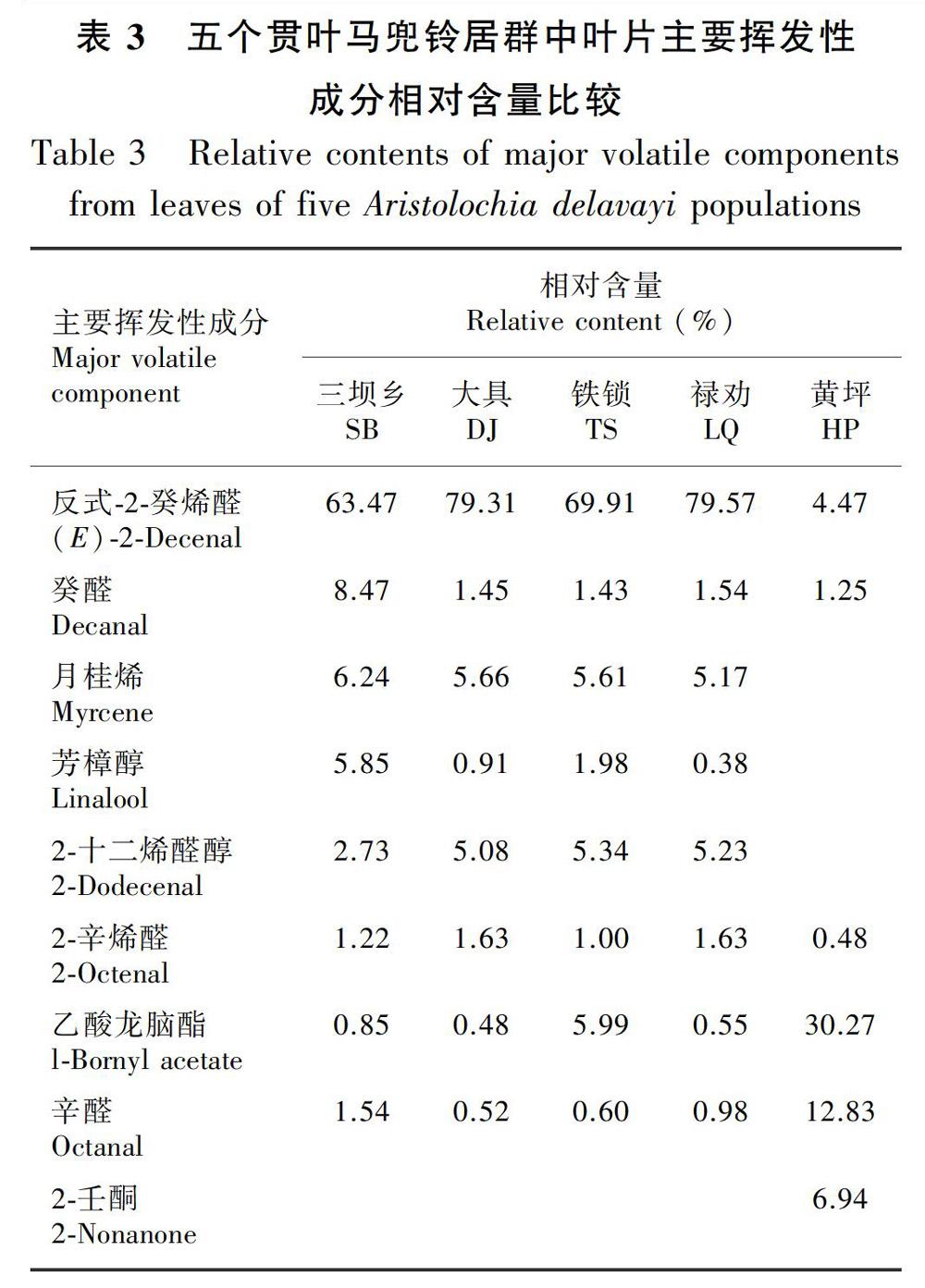
本研究从五个不同地理区域的贯叶马兜铃叶中共检出46个化合物,详情见表2。其中来自香格里拉三坝乡居群植株叶片共鉴定出16个挥发性成分,占总挥发性成分的97.86%。丽江大具乡居群中共鉴定出26个挥发性成分,占总挥发性成分的99.13%。楚雄铁锁乡居群中共鉴定出22个挥发性成分,占总挥发性成分的98.58%。禄劝则黑乡居群中共鉴定出24个挥发性成分,占总挥发性成分的97.93%。在来自鹤庆黄坪居群植株叶片中共分离出30个挥发性成分,占挥发性成分总量的94.56%,然而其主要挥发性成分及其含量与前四个居群差异明显,具体见表3。由此可见,除了来自黄坪地区的居群外,其他四个地区来源的贯叶马兜铃叶主要挥发性成分均为反式-2-癸烯醛,且分别占挥发性成分检出总量的63.47%、79.31%、69.91%、79.57%,这与之前研究的结果相似(Li et al.,2013;陈高等,2018)。另外,通过对萃取过程中加入的内标(正壬烷)换算得出,上述五个居群中每个居群植株干叶片平均每克每小时释放癸烯醛的量分别为17.31、21.63、19.06、21.70、1.22 ng。从以上结果可以看出,来自大具和禄劝两居群的植株叶挥发性成分中癸烯醛占有较高含量以及相对较高的释放量,且在居群内具有较好的稳定性。
3 讨论与讨论
贯叶马兜铃被用作香料食用主要是在金沙江两岸的三坝和大具两地区。这两个地区居群规模较大且分布集中,有着长期被广泛利用的基础,因此也成为当地纳西族人重要的传统香料。然而以贯叶马兜铃干植株或叶片直接用作香料的传统方式存在潜在的健康隐患。当前,关于马兜铃酸类物质(AAs)导致的肾衰竭、尿毒症、肝毒性等问题已进行过大量报道(Vanherweghem et al.,1993;Nortier et al.,2000;Debelle et al.,2008;Ng et al.,2017)。陈高等(2018)为弄清楚当地居民食用的贯叶马兜铃中马兜铃酸Ⅰ和Ⅱ的含量组成情况,分别对贯叶马兜铃干燥叶、果、根中马兜铃酸Ⅰ和Ⅱ的含量进行了分析,结果发现,马兜铃酸Ⅰ在各部分的含量分别为5.5、456.5、1 680.4 μg·g-1,其中果和根中马兜铃酸Ⅰ的含量均远超《中国药典》(2010版)规定的最高上限(10 μg·g-1)。虽然干燥叶中马兜铃酸Ⅰ的含量低于规定的上限值,但鉴于马兜铃酸及其衍生物的致突变性(Grollman,2013;Stiborova et al.,2017),建议尽量不要直接用作香料食用。由于马兜铃酸类物质不具有挥发性(姚东云等,2007),因此贯叶马兜铃的挥发油中不会含此类物质,并且香料成分也主要存在于挥发油中,所以对其挥发油成分的开发应用,可以为当地居民使用传统香料提供一个更安全的食用方式。
关于贯叶马兜铃精油的提取分析早就有过一些研究,结果发现,精油的主成分以及含量情况分别为反式-2-十一碳烯醛(94.23%)、反式-2-十一碳烯醛(53.24%)、反式-2-癸烯醛(52.00%)(孙汉董等,1987;周铁生等,1995;Li et al.,2013)。以上研究均采用水蒸馏法提取,但精油成分的组成却有较大差异,可能是由于蒸馏处理通常会导致植物的组织细胞及代谢相关的酶产生变化,且操作和控制條件的不同,提取的精油成分含量可能会出现较大变化;也可能与不同研究者材料的来源、采集季节,材料的处理方式不同以及挥发性成分鉴定错误有关。本研究没有采取水蒸馏法提取植物叶片挥发性成分,而是依照陈高等(2018)的方法,对其叶片气味成分进行收集分析,因为这样才符合当地人的使用习惯;以及在此研究的基础上,进一步分析了挥发性成分在居群内和居群间的稳定性和差异性。同时,为避免材料采集季节、干燥方法的不同对结果产生影响,我们采取时间上同季,干燥方法相同的策略,以此来最大限度地消除方法上的误差。
贯叶马兜铃精油不仅具有广谱的抗菌活性,而且含有丰富的合成香精香料的重要组分不饱和脂肪醛(张华,2006;江明等,2013;Li et al.,2013)。另外,在我们调查时发现,当地居民储存多年的干燥叶中辛香气味还是非常的浓烈,这可能与特殊香料的抗氧化作用有关(王爱云和李春华,2002),因而我们认为贯叶马兜铃精油具有较强的稳定性。因此,选择合适的种源进行规模化种植,以及优化提取精油工艺,充分开发利用贯叶马兜铃精油,不仅为抗菌类产品的开发提供新的借鉴,也将对香精香料的合成提供原料来源。
此外,我们发现来自黄坪的居群与其他居群在植株叶挥发性气味及成分上存在较大差异。在样品采集前,鉴于该居群植株叶片气味的特异性,依据贯叶马兜铃一般的识别特征,对其植株叶片的形态以及叶的着生方式进行了观察,初步确认是贯叶马兜铃的居群。该居群植株叶片散发出类似塑料的气味,这与本种植物通常所含的辛香气味相去甚远。根据以前的研究,塑料的挥发性成分中主要是羰基类化合物,产生塑料气味的是低分子的己酮和甲基戊烯酮(Villberg et al.,1997;罗忠富等,2010;孔萍和林新花,2011),然而在本研究中没有检测出类似气味的成分,我们推测这种气味的来源可能是挥发性成分混合而引起的“鸡尾酒效应”(Thomsen et al.,2018)。另外,与其他居群典型的干热河谷生境相比,该居群分布在黄坪境内远离金沙江支流的某山体上部区域中,由于相对海拔较高,该分布区小气候呈现湿热的特点,生境中草本的覆盖度较高且立地条件属于石灰岩地质不同于干热河谷的松散沙石土质。挥发性气味成分的较大差异以及特异的生境分布(该居群异于其他四个居群沿江或其支流分布的特点,存在一定程度地理隔离)是否暗示该居群为另一变种或亚种的可能(Francisco et al.,2008),还需对其花部结构等特征进行比较并结合分子生物学方法进一步确定。
参考文献:
CHEN G,GE J,QIN Y,et al.,2018. Research on the volatiles from leaves and roots of Aristolochia delavayi Franch. and their potential safety hazards [J]. Chin Condim,43(8):22-27. [陈高,葛佳,秦燕,等,2018. 辛香料植物贯叶马兜铃的根及叶挥发性成分分析及其食用风险解析 [J]. 中国调味品,43(8):22-27.]
CHEN G,JURGENS A,SHAO LD,et al.,2015. Semen-like floral scents and pollination biology of a sapromyophilous plant Stemona japonica (Stemonaceae) [J]. J Chem Ecol,41(3): 244-252.
CHEN G,LUO SH,MEI NS,et al.,2015. Case study of building of conservation coalitions to conserve ecological interactions [J]. Conserv Biol,29(6):1527-1536.
CHEN JL,GUO W,PENG W,et al.,2013. Volatile components in leaves of six Myrtaceous plants by SPME-GC-MS [J]. J Trop Subtrop Bot,21(2):189-192. [陈佳龄,郭微,彭维,等,2013. SPME-GC-MS分析桃金娘科6种植物的叶片挥发性成分 [J]. 热带亚热带植物学报,21(2):189-192.]
DEBELLE FD,VANHERWEGHEM JL,NORTIER JL,2008.Aristolochic acid nephropathy:A worldwide problem [J]. Kidney Int,74(2):158-169.
FRANCISCO CS,MESSIANO GB,LOPES LMX,et al.,2008. Classification of Aristolochia species based on GC-MS and chemometric analyses of essential oils [J]. Phytochemistry,69(1):168-175.
GROLLMAN AP,2013.Aristolochic acid nephropathy:Harbinger of a global iatrogenic disease [J]. Environ Mol Mutagen,54(1):1-7.
HE WJ,HE JW,LI Y,et al.,2010. Tissue culture and rapid propagation of Aritolochia delavayi Franch [J]. Plant Physiol J,46(12):1273-1274. [和文佳,和加卫,李燕,等,2010. 贯叶马兜铃的组织培养与快速繁殖 [J]. 植物生理学报,46(12):1273-1274.]
HE WJ,LI ZJ,ZHANG HX,et al.,2017. Study on chemical components in the volatile oils obtained from aseptic seeding and callus of Aristolochia delavayi [J]. Flav Frag Cosm,45(1):5-8. [和文佳,李志坚,张红霞,等,2017. 山草果无菌苗和愈伤组织挥发性成分研究 [J]. 香料香精化妆品,45(1):5-8.]
JIANG M,YI QY,WANG M,2013. Rooting test of Aristolochia delavayi tissue culture seedling [J]. J West Chin For Sci,42(4):82-86. [江明,易清元,王梦,2013. 山草果组培苗生根实验 [J]. 西部林業科学,42(4):82-86.]
JIN ZZ,OU XK,QU PD,et al.,1994. Preliminary study on floristic characteristics of seed plants in the dry-hot valley of Jinsha River [J]. Acta Bot Yunnan,19(1):1-16. [金振洲,欧晓昆,区普定,等,1994. 金沙江干热河谷种子植物区系特征的初探 [J]. 云南植物研究,19(1):1-16.]
KONG P,LIN XH,2011. Determination of volatile organic compounds in Soft-Poly (Vinyl Chloride) by GC-MS [J]. Guangdong Chem Ind,38(7):159-160. [孔萍,林新花,2011. 气相色谱-质谱联用法测定软聚氯乙烯塑料的挥发性气体 [J]. 广东化工,38(7):159-160.]
LI MP,LI R,DING PX,et al.,2019. Optimization of HS-SPME condition and analysis of volatile compounds in fresh and different drying coriander by HS-SPME-GC-MS [J]. Sci Technol Food Ind,40(7):228-236. [李美萍,李蓉,丁鹏霞,等,2019. HS-SPME条件优化并结合GC-MS分析新鲜及不同干燥方式的香菜挥发性成分 [J]. 食品工业科技,40(7):228-236.]
LI ZJ,NJATENG GS,HE WJ,et al.,2013. Chemical composition and antimicrobial activity of the essential oil from the edible aromatic plant Aristolochia delavayi [J]. Chem Biodivers,10(11):2032-2041.
LUO ZF,LI YH,YANG Y,et al.,2010. Study on analysis of odour in polypropylene composites for automobile [J]. Eng Plast Appl,38(7):51-53. [罗忠富,李永华,杨燕,等,2010. 车用聚丙烯复合材料气味分析研究 [J]. 工程塑料应用,38(7):51-53.]
NG AWT,POON SL,HUANG MN,et al.,2017. Aristolochic acids and their derivatives are widely implicated in liver cancers in Taiwan and throughout Asia [J]. Sci Transl Med,9(412):eaan6446.
NORTIER JL,MARTINEZ MM,SCHMEISER HH,et al.,2000. Urothelial carcinoma associated with the use of a Chinese herb (Aristolochia fangchi) [J]. New Engl J Med,342(23): 1686-1692.
SUN HD,LIN ZW,DING JK,1987. Chemical constituents of essential oil from Aristolochia delavayi [J]. Acta Bot Yunnan,12(1):108. [孙汉董,林中文,丁靖凯, 1987. 山草果精油的化学成分 [J]. 云南植物研究,12(1):108.]
SUN JM,QIN JL,LI LJ,et al.,2008. Resource status and conservation strategy of Aristolochia delavayi,an endemic and endangered plant in China [J]. New Technol Prod of Chin,13(16):130. [孙景梅,覃家理,李丽娟,等,2008. 中国特有濒危植物山草果的资源现状与保护对策 [J]. 中国新技术新产品,13(16):130.]

