浅析外科植入物磁共振兼容性安全评价
高中 陆离原 王伟明
(上海市医疗器械检测所,上海 201318)
从二十世纪90 年代开始,临床对磁共振成像设备的需求日益增加,因其成像对软组织对比度普遍优于其他放射成像方式,并具有潜在的生理和功能应用价值。磁共振成像设备由于采用超高的磁场,获得软组织内部的成像较传统放射成像更为清晰,使其成为神经系统、肌肉骨骼、脑部、胸部和腹部等部位的首选成像方式[1-3]。且由于未采用X 射线或类似放射性物质,使其适合同一病患多次临床诊断的重复成像,年幼病患以及孕妇的诊断成像。但磁共振成像设备由于其工作原理,在运行期间产生的强大电磁场和成像所必须的射频场会带来一定的潜在风险。随着医学技术的发展以及病患的需求,外科植入物的使用也变得越来越普遍。体内装有外科植入物的患者,需要磁共振成像设备诊断的需求量,也随之日益增多。因此植入物在磁共振环境中的兼容性安全性评价,成为预防磁共振医疗事故极为重要的一环[4,5],现就相关标准和安全性评价的要求进行探讨。
1 外科植入物磁共振兼容性标准的发展历史和现状
1.1 美国标准
1997 年,美国食品药品管理局发布了《医疗器械与磁共振成像系统的交互影响》指南草案[6],由美国材料与试验协会(ASTM)组织研究外科植入物与磁共振兼容性的相关技术细节以及标准制定,并于2000 年发布了5 个标准。美国材料与试验协会后续对这些标准做过几次更新,目前最新版本见表1。

表1 ASTM 系列标准
1.2 国际标准化组织(ISO)标准
ISO 14630 :2012[12]无源外科植入物通用要求(即我国的YY/T 0640-2016[13])引入了磁共振环境的概念,并参考美国ASTM 系列标准来考虑磁共振环境中的安全性。针对有源植入物,特别是带有导线的有源植入物(例如植入式起搏器和植入式除颤器)。2007 年由国际电工委员会和国际标准化组织组成的联合工作组制定了ISO/TS 10974《携带有源植入式医疗器械的患者磁共振成像的安全性评价》,目前最新版是2018 年发布的第2 版[14]。为避免不同组织针对同一研究重复工作,美国材料与试验协会、国际标准化组织和国际电工技术委员会之间进行分工合作。ASTM 主攻无源植入物的兼容性(其中的磁致位移力和磁致扭矩包含有源和无源),国际标准化组织和国际电工技术委员会主攻有源植入物的兼容性(部分测试引用ASTM 系列标准的测试方法),使得整个医疗植入物的磁共振兼容性的标准化历程得到了快速有序的发展。
1.3 我国标准
我国参考ASTM 系列标准重新起草了YY/T 0987 系列标准[15-19],由全国外科植入物和矫形器械标准化技术委员会(SAC/TC110)归口管理。该系列标准于2016 年3 月23 日发布,2017 年1 月1 日开始实施。2017 年,中华医学会放射学分会质量管理与安全管理学组和中华医学会放射学分会磁共振成像学组发布的《磁共振成像安全管理中国专家共识》[20]列出11 种植入物需要进入磁共振环境时的指导意见,与标准的测试方法相比,该共识也可作为是否能安全兼容的经验性依据。
2 外科植入物磁共振兼容性安全评价
2.1 安全标记
对于可能被带入磁共振环境的植入物,应在包装的标签(包括使用说明书和包装插页)和病人信息卡上进行MR 标记。应提供以下信息:根据物体在磁共振环境中的行为属性(特别是磁致位移力、磁致扭矩和射频致热试验),使用指定标记将物体标记为MR 安全、MR 特定条件安全或MR 危险。通过相应的标记和文档支持来区分不同的外科植入物在磁共振环境中的安全性或安全性条件。
磁共振环境的差异主要是磁场强度和射频条件,物体在不同条件下受到的影响可能是不同的。传统定义“MR 安全”和“MR 兼容”容易产生很大的混淆,用户常常错误地认为标记为“MR 安全”和“MR 兼容”的物体在任何磁共振环境中都是安全或兼容的。最新版的定义“MR 安全”、“MR特定条件安全”或“MR 危险”旨在消除这些混淆。

图1 MR 安全标记

图2 MR 安全标记

图3 MR 危险标记

图4 MR 特定条件安全标记
对于MR 特定条件安全的器械,在安装了此器械的病人诊疗信息卡中,应至少包含下述内容:(1)MR特定条件安全标志,或MR特定条件安全的陈述;(2)器械相关型号信息,以及如何获得详细的磁共振安全特定条件信息的方式;(3)对不在上述已确认的兼容环境中进行磁共振扫描可能会产生后果的警告。
2.2 将磁性物体拉进磁共振系统孔腔的磁致位移力
磁共振扫描仪所产生的静态磁场B0,其场强范围在0.2T~3T(极端情况可超过4T,且已有7T的磁共振系统进入临床使用)。这个磁场在扫描仪未做成像扫描动作时也存在,其强度几乎是地球磁场的十万倍。磁场强度随着距离的增大而急剧下降,产生一个非常大的空间梯度,可导致铁磁体的强位移力,甚至造成物品的“飞弹”现象。历年来由于磁致位移力所造成的医疗事故屡见不鲜,甚至直接导致患者或操作人员死亡[21]。
2.3 使磁性物体旋转至与磁场方向一致的磁致扭矩
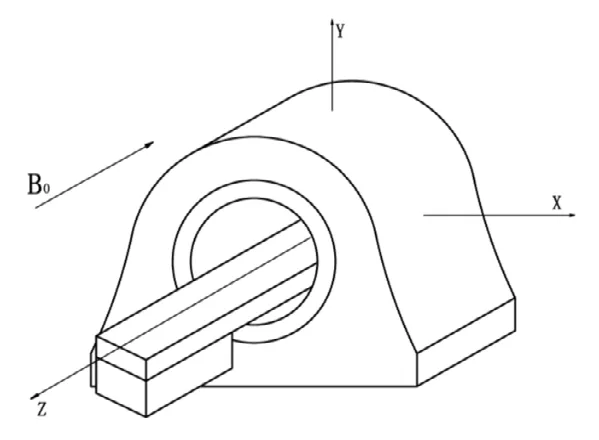
图5 静磁场B0 示意
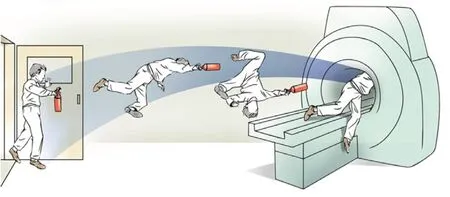
图6 由于磁致位移力造成事故的示意图
磁致扭矩同样由磁共振扫描仪所产生的静态磁场B0造成,其效应类似于地球磁场使指南针的指针与地球磁场方向趋于一致而对指针产生的扭矩。磁致扭矩的比较对象是地球重力场产生的重力矩,通过与重力矩相比来衡量磁致扭矩导致的风险是否高于地球重力场中日常活动的风险。由于不同的磁共振系统产生的场强并不一样,在1.5T 扫描系统中安全的医疗器械在更高或更低场强的系统中(如3T或1T 系统)未必是安全的。此外,开放式和圆柱形磁共振系统也会有显著的差异,这些差异在评价中也需要进行考虑。
2.4 在磁共振孔腔内射频对物体的致热效应
从组织中提取磁共振信号,需由射频线圈产生的射频(脉冲)场B1(其量级为μT,频率在几十到几百MHz)。射频致热效应类似于我们常见的电磁炉,由交变电磁场在金属内产生的电流使金属发热。射频(脉冲)场B1所产生的电磁效应能使人体组织发热[22],特别当存在有外科植入物时。目前普遍采用吸收率[23](简称SAR,单位W/kg)来衡量单位质量的组织所吸收的射频电磁能量。美国食品药品管理局目前针对具有正常热调节功能病患的限值为4.0 W/kg;针对所有病患的限值为1.5 W/kg。为此,对磁共振成像过程中射频(脉冲)信号的占空比需要作出限制以达到控制SAR 的目的。需要特别注意的是那些带有环形状的金属外科植入物以及弯曲的有源外科植入物的导线,他们往往是造成射频致热的主要来源。
2.5 磁共振系统的磁场或射频场导致有源医疗器械基本性能的影响
在磁共振检查过程中,梯度脉冲所造成的开关磁场可在导线电极上产生感应电势。外源性电势可存在于单一的有源外科植入物的电极导线中,也可存在于多电极导线外科植入物的多根电极之间,或者在电极和与组织接触的导电性外壳之间。感生电压所引起的电流可导致非预期的生理刺激或医疗器械故障。与肌肉组织或神经接触的有源外科植入物和部分性植入的有源医疗器械需要注意此问题。有源医疗器械(例如有源外科植入物、有源附件、射频调谐部件、磁化部件)和含有磁铁或磁性控制的或温度控制部件的无源医疗器械暴露于磁共振环境中有可能导致医疗器械的故障。这种故障可能是暴露于磁共振环境中的暂时情况,也可能是永久性的。这可被视作有源医疗器械的电磁兼容/电磁抗扰度的一部分。在磁共振环境中造成的心脏起搏器和除颤器故障所引起的病患死亡的案例也曾有过报道[24]。
ISO/TS 10974[14]提供了评估有源外科植入物在磁共振环境中故障的标准化的测试方法,其主要包括梯度脉冲造成的电极电流泄漏试验、长梯度脉冲序列引起的在与电极接口处接触的组织的整流电流试验、受梯度脉冲影响引起的输出信号变异试验。
2.6 对病患神经系统的剌激和噪音
用于磁共振信号的空间编码的时变快速开关梯度磁场,其频率为kHz 级别,它可引起周围神经刺激和外科植入物的生物效应,包括电刺激神经和产生可能由于施加在视网膜锥上的轻微扭矩。因此,将磁场变化的时间率(dB/dt)限制在不会导致周围神经刺激疼痛的水平是有必要的。同时,这一开关梯度磁场也是磁共振噪音的主要来源,最高可超过100dB[25]。
2.7 图像伪影和图像射频噪声
图像伪影和射频噪声可由磁共振环境中医疗设备的存在和/或操作引起。伪影可由成像视野内或附近的医疗设备(如外科植入物或表面电极)引起。由材料产生的特征静态磁场,可扰动精确图像重建所必需的位置和频率之间的关系。如果物体的磁化率与组织的磁化率明显不同,就会导致变形。此外,外科植入物可能由于进入射频磁场而呈现感应涡流,改变外科植入物附近的射频场,从而导致失真。射频噪声通常在图像上显示为静态噪声,可由位于磁共振室任何位置的医疗设备引起。射频噪声是由于医疗设备的过度电磁辐射干扰了磁共振扫描仪的正常工作。由于磁共振室被屏蔽,不受进入房间的外部射频场的影响,因此房间外电磁噪声设备的操作通常不会影响磁共振扫描仪。与图像伪影和射频噪声有关的主要问题包括在需要解剖信息的地方产生空洞,以及产生可能被误诊为病理学的伪影。
3 总结

图7 心脏起搏器/除颤器引起的磁共振成像伪影例子
外科植入物磁共振兼容性安全评价并不仅限于本文提到的要求,如磁致扭矩,现行行业标准中所指的磁致扭矩是由静磁场和外科植入物磁矩作用产生的静磁扭矩,不包含由于静磁场与涡电流相互作用导致器械旋转而产生的动态扭矩,而动态扭矩也应当考虑作为兼容性的风险来源。相关标准仅仅给出了具体的评价要求指南,实际情况还应结合具体产品作出综合性科学性的评价。此外,参与试验的相关人员应经过充分的培训才可上岗,培训内容应至少不低于医院从事磁共振成像的人员所应接受的培训。完善的标准、合格的设备、规范的流程和操作对于磁共振兼容性安全评价来说缺一不可。

