高效液相色谱法测定人血浆中米卡芬净浓度及其在重症患者中的应用
赵明明,陈亚南,路 童,李国飞,肇丽梅(中国医科大学附属盛京医院药学部,辽宁 沈阳 110004)
米卡芬净是由鞘茎点霉(Coleophoma empetri)酶解产物通过化学修饰合成的一种半合成脂肽类化合物,可非竞争性抑制1,3-β-D-葡聚糖合成酶,从而破坏细胞壁的完整性,是继卡泊芬净后被批准的第2种棘白菌素类抗真菌药[1-2]。棘白菌素类药物对于大多数常见的念珠菌属显示出杀菌活性,对于曲霉菌等易感霉菌显示出抑菌作用[3-4]。由于米卡芬净的作用靶标1,3-β-D-葡聚糖合成酶是真菌的特异性酶,因此,其具有治疗指数高、抗菌谱广、不良反应发生率低及药物相互作用少的特点[5-6]。米卡芬净主要用于治疗食道念珠菌感染、骨髓移植及获得性免疫缺陷综合征患者中性粒细胞减少症的预防[7]。重症感染常伴有侵袭性真菌病,因此,米卡芬净在重症患者中应用广泛[8]。本研究旨在建立高效液相色谱紫外检测法(high performance liquid chromatography-ultraviolet detection,HPLC-UV)用于测定人血浆中米卡芬净的浓度,并将其应用于重症患者体内米卡芬净血药浓度的监测,以期为重症患者合理应用米卡芬净提供一定的参考依据。
1 材料
1.1 仪器
Agilent-1100系列高效液相色谱仪(安捷伦科技有限公司,配有Agilent1100紫外检测器和Agilent 1200自动进样器);TARGIN VX-Ⅱ型多管涡旋振荡器(北京踏锦科技有限公司); TDL-40C型低速台式离心机(上海安亭科学仪器厂); Eppendorf 5424R型高速冷冻离心机(Eppendorf 中国有限公司)。
1.2 药品与试剂
米卡芬净标准品(含量>97.0%,批号为1-LXM-24-1,加拿大TRC);氯唑沙宗(含量>98%,批号为100364-200301,中国药品生物制品检定所),乙酸铵(含量≥99.0%,批号为BCBQ3068V,Fluka试剂);甲醇和乙腈均为色谱纯,空白血浆由中国医科大学附属盛京医院输血科提供。
2 方法与结果
2.1 色谱条件
色谱柱:C18色谱柱(4.6 mm×150 mm,5 μm);流动相:乙腈-5 mmol/L醋酸铵(V∶V=40∶60);流速:1.0 ml/min; 柱温:35 ℃;检测波长:273 nm;进样量:50 μl。
2.2 溶液的配制
对照品溶液的配制:精密称取米卡芬净10.03 mg, 置于10 ml容量瓶中,用甲醇溶液配制成质量浓度为1.0 mg/ml的储备液。取储备液适量用甲醇稀释成质量浓度为0.2、0.5、1、2.5、5、10、20和25 μg/ml的米卡芬净标准系列溶液,置于-20 ℃冰箱保存备用。另外,精密称取氯唑沙宗1.60 mg,置于100 ml容量瓶中,用甲醇溶液溶解并定容,配制成最终质量浓度为16.0 μg/ml的内标溶液。
2.3 血浆样品处理方法
精密吸取血浆样品100 μl于1.5 ml离心管中,加入内标溶液(16.0 μg/ml氯唑沙宗溶液)50 μl,补加甲醇溶液100 μl,然后加入乙腈200 μl,涡旋混合5 min, 12 000 r/min条件下离心5 min,然后取上清液进行HPLC分析。
2.4 方法学考察
在测试临床样本之前,按照《中华人民共和国药典》(2015年版)“生物样品定量分析方法验证指导原则”[9]对临床生物样品测定方法学确证的要求,进行方法学考察,以验证方法。
2.4.1 专属性考察:分别量取空白血浆及给药后血浆样品各100 μl,按“2.3”项下方法操作处理,获得相应色谱图,见图1。在本研究所建立的方法条件下,米卡芬净、内标的保留时间分别为6.421、3.928 min,两者峰形良好,分离度能够达到要求,血浆中内源性杂质不干扰测定。
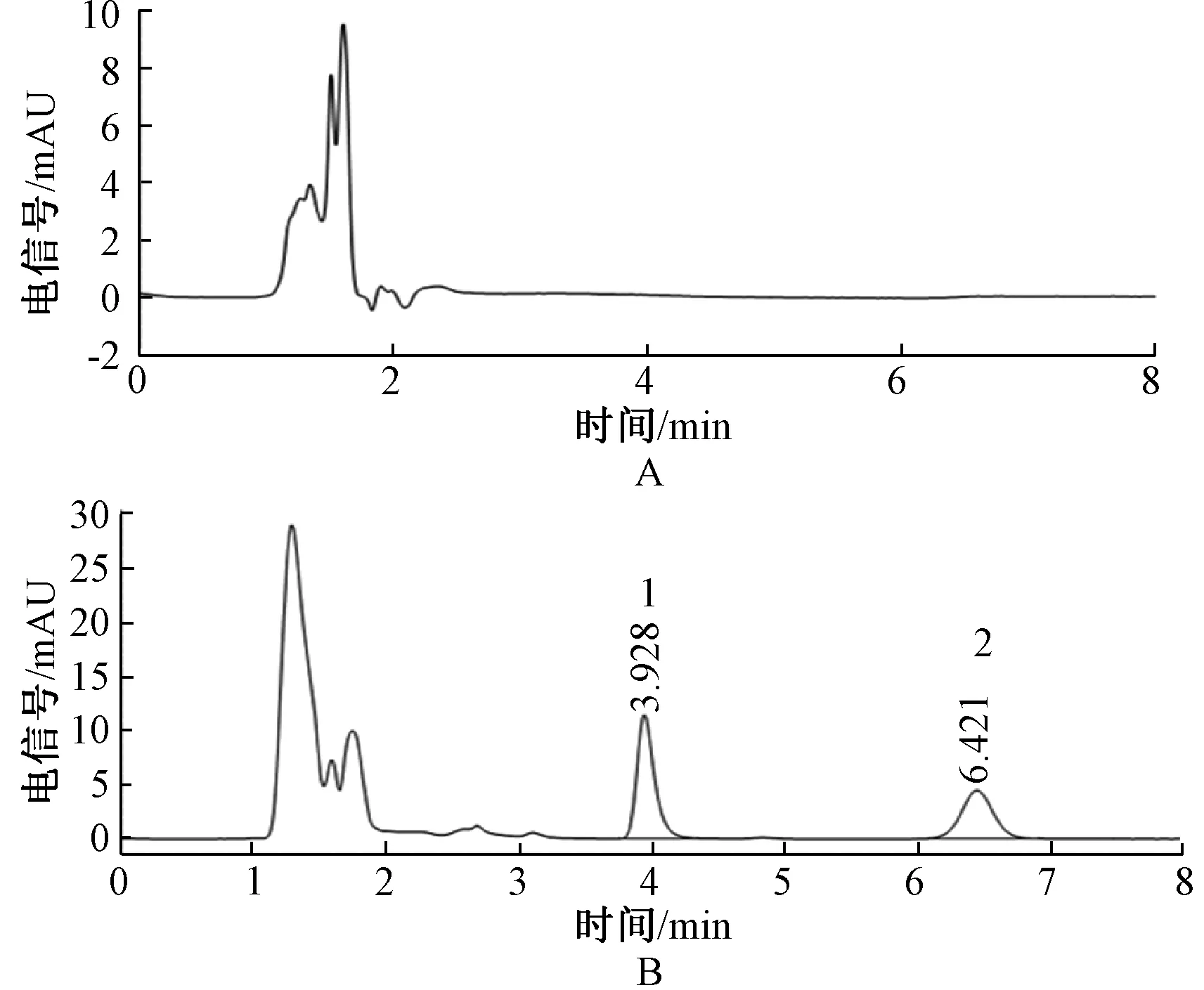
A.空白血浆;B.血浆样品;1.内标氯唑沙宗;2.米卡芬净A. blank plasma; B. plasma sample; 1. chlorzoxazone for internal standard substance; 2. micafungin图1 人血浆中米卡芬净和内标氯唑沙宗的典型色谱图Fig 1 Typical chromatographic column of micafungin and internal standard substance in human plasma
2.4.2 标准曲线制备与定量下限:精密吸取空白血浆100 μl,加入“2.2”项下的米卡芬净标准系列溶液,配制成相当于血浆浓度为0.2、0.5、1、2.5、5、10、20及25 μg/ml的血浆样品,按“2.3”项下方法操作处理,然后进行HPLC分析,记录色谱图,以米卡芬净浓度C(μg/ml)为横坐标,米卡芬净与内标峰面积比值为纵坐标,采用加权(W=1/x2)最小二乘法进行回归计算,求得直线回归方程即为标准曲线,所得回归方程为:As/Ai=0.340 1C-0.000 069(r=0.999 8)。可见米卡芬净在浓度为0.2~25 μg/ml范围内时,线性关系良好,定量下限为0.2 μg/ml。
2.4.3 精密度与回收率:分别制备米卡芬净低、中及高3个浓度(0.5、5和25 μg/ml)的质量控制(QC)样品,每个浓度平行6份,连续测定3 d,根据当日的标准曲线,计算QC样品浓度,根据QC样品测定结果计算方法的准确度和精密度,见表1。同时,另取空白血浆100 μl,除不加内标和标准溶液外,按照“2.3”项下方法操作,向沉淀后的样品中分别加入低、中及高3个浓度的QC样品和内标溶液,涡旋混合后进行HPLC分析,获得相应峰面积,以每个浓度2种处理方法的峰面积比值计算提取回收率,结果见表1。

表1 米卡芬净的精密度与回收率Tab 1 Precision and recovery rate of micafungin
2.4.4 稳定性试验:取米卡芬净低、中及高3个浓度(0.5、5和25 μg/ml)的QC样品,每个浓度平行3份,分别考察4 ℃避光条件下放置8 h后提取、提取后4 ℃避光放置12 h、-70 ℃避光冻融循环3次和-70 ℃避光冰冻放置1个月的稳定性。结果表明,米卡芬净的血浆样品在上述条件下均有很好的稳定性(RE%<±15%)。
2.5 临床应用
选取32例米卡芬净治疗重症患者,在规律用药3 d后,于下次给药前采取静脉血2 ml,以3 500 r/min离心10 min后取上层血浆,用所建立的方法测定米卡芬净的浓度。32例重症患者中,男性21例,女性11例,平均年龄(60.09±15.4)岁,平均体重(70.22±8.62) kg;根据患者病情的不同,给药剂量分别为100、150及200 mg,1日1次;平均米卡芬净血药浓度为(12.09±6.43) μg/ml。
3 讨论
重症患者常常因感染性或非感染性因素引发病理学改变,导致出现全身炎症反应综合征。引发全身炎症反应综合征的一个重要结果,就是体液从损伤内皮细胞和毛细血管漏过度渗透到组织间隙。这种情况在重症脓毒症和脓毒症性休克患者中尤为明显,这种组织间隙容积增大的情况可能导致药物分布容积增加,从而导致血浆药物浓度降低[10]。有研究结果表明,ICU的重症患者体内米卡芬净的药时曲线下面积(AUC0~24 h)显著低于正常人及其他类型患者[11-12]。因此,建立一种有效的血药浓度测定方法,并将其应用于使用米卡芬净进行治疗的临床重症患者,是十分有必要的。
米卡芬净血药浓度的测定方法已有文献报道。金锦等[13]报道了一种液相色谱串联质谱法测定米卡芬净的血药浓度;曹江等[14]将高效液相色谱法荧光检测用于其浓度的测定。但质谱仪和荧光检测器在医疗机构并不常见,因此,开发一种HPLC-UV方法,更有利于监测临床重症患者体内的米卡芬净血药浓度。由于米卡芬净不稳定[15],因此,使用过程中血样的处理都在避光、冰浴情况下操作,以保证样品测定的准确性。
本研究建立了测定人血浆中米卡芬净浓度的HPLC-UV方法,方法简单、灵敏,专属性强,具有普遍适用性,可将其应用于临床重症患者体内米卡芬净血药浓度的测定。

