益生菌在普通型新型冠状病毒肺炎合并腹泻患者中使用的重要性分析
柯娥,张海,鄂东医疗集团黄石市中心医院(湖北理工学院附属医院)消化内科,肾脏疾病发生与干预湖北省重点实验室 湖北省黄石市435000
0 引言
新型冠状病毒(severe acute respiratory syndrome coronavirus 2,SARS-CoV-2)是一种新型病原体,自2019-12,湖北省武汉市首次报道,现已在全世界范围内发生,其感染的肺炎称新型冠状病毒肺炎(coronavirus disease-2019,COVID-19)[1],简称“新冠肺炎”,被纳入《中国传染病防治法》,并规定COVID-19为按甲类传染病管理的乙类传染病.该病毒除引起呼吸系统症状外,部分患者出现了腹泻或以腹泻为首发症状就诊[2].对疫情期间,以腹泻为首发症状而就诊的患者,提醒医务人员及其他参与防控的人员正确识别并及时有效对可能传染源进行分诊及隔离.本文通过观察腹泻患者转归情况,分析腹泻可能机制及评估益生菌的作用.
1 材料和方法
1.1 材料
1.1.1 病例收集:观察2020-01/2020-02黄石市中医医院确诊为普通型COVID-19患者[2],年龄30-70岁,无糖尿病、肠道恶性肿瘤、甲状腺功能亢进、肠易激综合征者,所有COVID-19患者符合《新型冠状病毒肺炎诊疗方案(第七版)》诊断标准.
1.1.2 实验组:入组标准:以临床表现、新型冠状病毒核酸检测、胸部CT检查为依据,根据《新型冠状病毒诊疗方案(试行第六版)》[2]确诊为普通型COVID-19患者,在抗病毒治疗基础上,接受布拉氏酵母菌散的辅助治疗.排除标准:粪便细菌培养见(副)伤寒杆菌、痢疾杆菌、沙门菌属、志贺菌属、大肠杆菌、弯曲菌、金黄色葡萄球菌、副溶血性弧菌或粪便培养出诺如病毒、轮状病毒.入院第一天即开始抗病毒治疗:盐酸阿比多尔片0.2 g,每日3次口服,干扰素α2b 4 mL,每日3次雾化吸入,布拉氏酵母菌散0.5 g,每日2次,口服.
1.1.3 对照组:入组标准及排除标准同实验组,抗病毒治疗方案与实验组相同,且未使用布拉氏酵母菌散.
1.2 方法 记录腹泻病程时间,治疗过程中,原发病加重或合并肠道细菌感染,需使用激素、抗生素或其他治疗,立即终止实验.
统计学处理采用SPSS 13.0统计软件进行统计分析.计量资料以(mean±SD)表示,计数资料用频数表示.
2 结果
2.1 两组受试者一般资料和粪便脓细胞差异比较 两组受试者一般资料.表1:实验组50例,男性32例,女性18例;对照组40例,男性28例,女性12例.两组试验对象的平均年龄分别是51.49岁±12.94岁、50.02岁±10.64岁,无统计学差异(P>0.05).表2:实验组粪便脓细胞阳性12例,对照组粪便脓细胞阳性9例,脓细胞阴性患者中,实验组腹泻病程4.01 d±1.27 d,对照组病程4.12 d±1.17 d脓细胞阳性患者中,实验组腹泻病程5.11 d±1.42 d,对照组腹泻病程5.17 d±1.36 d,两组间两两比较,差异无统计学意义(P>0.05).
2.2 两组受试对象腹泻病程比较 两组受试者相同年龄段比较,相同年龄段,实验组平均腹泻病程较对照组短,差异有统计学意义(P<0.05),表3.
实验组使用益生菌后患者腹胀及恶心、呕吐症状较明显缓解.
3 讨论
SARS-CoV-2感染潜伏期1-14 d,多为3-7 d,临床表现以发热、干咳、乏力为主要临床表现,少数患者伴鼻塞、流涕、咽痛、肌痛、腹泻等[3].部分患者以消化道症状如腹泻、腹痛、纳差等为首发症状.Wang等[4]研究中,纳入138例COVID-19患者,其中14例出现腹泻,该症状发生于发热、咳嗽等呼吸道症状之前.Chen等[5]观察的99例COVID-19患者中,腹泻患者2例.在以上研究病例中,轻症患者腹泻呈自限性,重症患者腹泻需使用药物辅助治疗[2],其中益生菌制剂被提到了重要高度.维持水、电解质及酸碱平衡,避免因肠道菌群失调导致肠道内屏障功能破坏而出现肠道菌群异位加重感染.2020-02-01,深圳市第三人民医院透露,该院肝病研究所研究发现,在某些SARS-CoV-2感染患者的粪便中检测出该病毒核酸阳性,当时不确定是否存在活病毒.2020-02-13,钟南山团队在一例重症SARS-CoV-2感染病例中成功分离出活的新型冠状病毒,李兰娟团队亦有相同的发现.美国首例COVID-19确诊患者亦出现腹部不适,粪便病毒核酸检测阳性[6].根据新型冠状病毒肺炎患者的消化道症状,结合相关研究发现分析病毒直接侵入消化道黏膜可能性大.轻症COVID-19患者腹泻呈自限性,对于不能自行好转的患者肠道菌群调节剂已被列入COVID-19患者诊疗方案,可见早期人们已经意识到腹泻患者肠道内菌群紊乱在病程中的破坏作用.
病毒直接损伤导致腹泻:自2002年非典型性肺炎(severe acute respiratory syndrome,SARS)爆发以来,急性呼吸综合征冠状病毒(severe acute respiratory syndrome coronavirus,SARS-CoV)分子结构已有了广泛的研究,揭示了SARS-CoV Spike蛋白受体结合域(receptor-binding domain,RBD)与宿主细胞(angiotensin-convertingenzyme 2,ACE2)的相互作用,两者之间的作用调节着该病毒的传播,Wan等[7]、Zhang等[8],张明鑫等[9]研究发现 ACE2在消化道中的高表达、为SARS-CoV-2在消化道的潜在感染途径提供了生物学证据.SARS-CoV-2可直接侵入肠上皮细胞导致肠道内屏障功能破坏,增加肠道感染风险,加速肠道内炎症的发生、发展,出现腹泻、腹痛等消化道症状;肠内炎症导致肠道菌群移位加重全身多器官感染,增加脓毒血症发生率.根据本研究,益生菌可提高肠道屏障功能,维持肠道内环境平衡,缩短腹泻病程.抗病毒药物不良反应导致腹泻:自COVID-19爆发至今,针对SARS-CoV-2尚无有效的抗病毒药物,《新型冠状病毒感染的肺炎诊疗方案第五版》[10]将洛匹那韦/利托那韦作为抗病毒的试用药已广泛用于COVID-19患者.洛匹那韦/利托那韦为蛋白酶抑制剂,用于抗HIV治疗.后陆续用于抑制SARS-CoV、中东呼吸综合征冠状病,均取得较理想的效果[11].多研究证明,洛匹那韦/利托那韦的胃肠道反应较常见,主要表现为腹痛、腹泻[12].Kiselev等[13]对阿比多尔进行的临床疗效研究中证明,阿比多尔为广谱抗病毒药,通过特异性抑制病毒与宿主细胞的融合,阻断病毒复制,其不良事件发生率为6.2%,主要表现为恶心、腹泻、头晕和血清转氨酶升高;磷酸氯喹为抗疟药物,其直接对胃肠道的刺激表现为恶心、呕吐,腹痛、腹泻.药物引起的腹泻,在停药或服药数天后可自行缓解.
益生菌缓解腹泻的机制[14]:(1)拮抗致病菌:益生菌与细菌竞争营养和定植位点,产生抗微生物物质,组织病原菌的黏附和定植;(2) 维持肠上皮粘膜屏障功能:益生菌与肠上皮黏蛋白结合,维持肠上皮正常的通透性,刺激粘液产生,促进粘膜再生,增强肠道黏膜屏障功能和定植抗力;(3)增强肠道黏膜和系统的免疫反应:益生菌可刺激过增强IgA的产生、NK细胞的活性、白细胞的吞噬活性、T(B)淋巴细胞的增值活性、细胞因子的产生,从而增强肠道粘膜和系统的免疫反应.故益生菌的使用可有效对抗病原体,调节肠道菌群平衡,维护肠道粘膜屏障功能,有效改善患者腹泻症状.
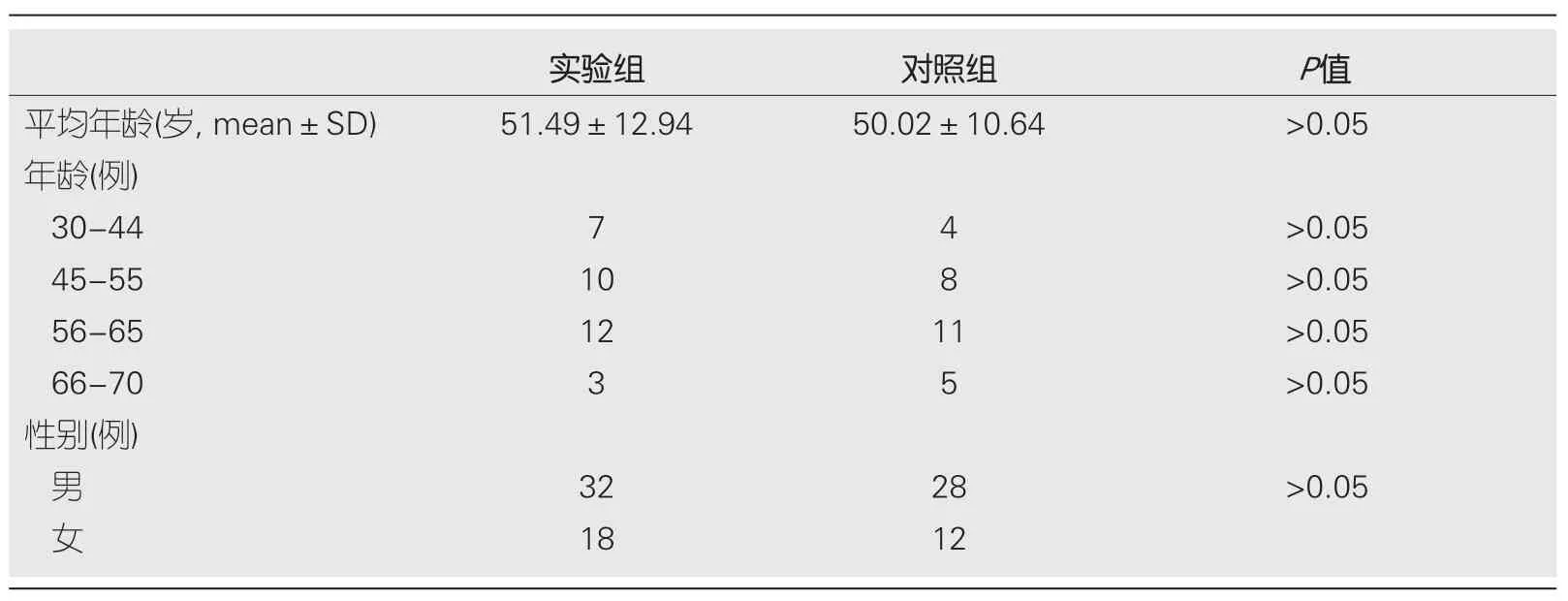
表1 两组受试对象的一般资料

表2 两组受试对象粪便脓细胞差异比较
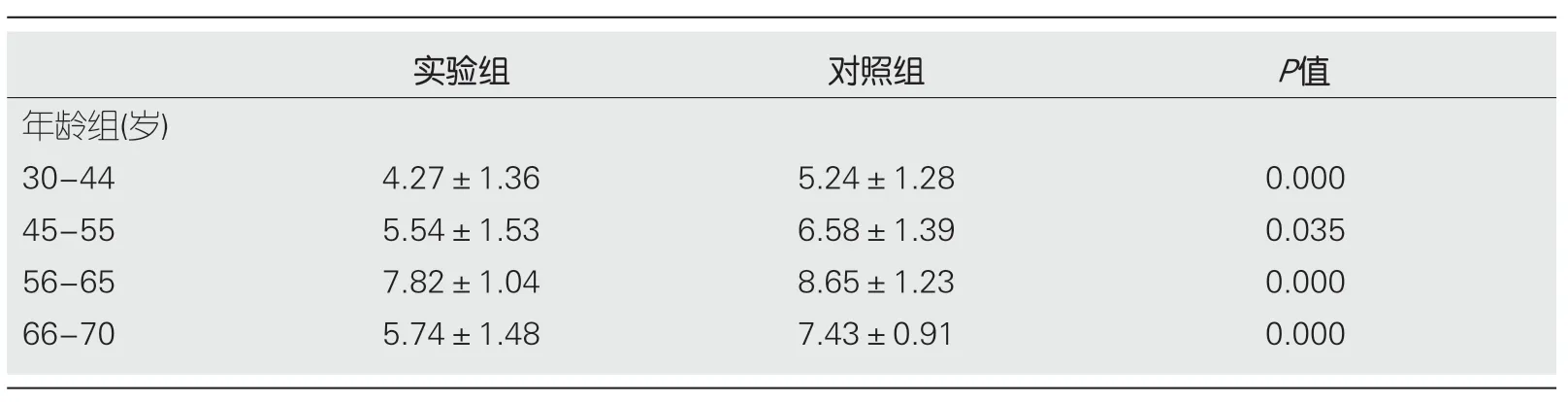
表3 两组受试对象腹泻病程比较
4 结论
本研究仅针对未使用抗生素、粪便细菌培养及排除新型冠状病毒外其他腹泻病毒检测阴性的COVID-19合并腹泻患者,排除抗生素的影响.观察结果显示,COVID-19合并腹泻患者使用益生菌可缩短腹泻病程,缓解腹泻、腹胀、恶心、呕吐等消化道症状.不足之处在于样本量较小,不能排除抗病毒药物不良反应导致的腹泻,此类患者部分症状呈自限性,益生菌使用对该类腹泻患者症状是否有缓解作用仍无法确定,有待大样本研究.
文章亮点
实验背景
目前对于新型冠状病毒肺炎(coronavirus disease-2019,COVID-19)的治疗属于探索式,COVID-19合并腹泻的患者加重胃肠道反应,加重内环境紊乱,治疗过程中患者口服药物种类多,腹泻原因除病毒直接损伤外,亦是部分抗病毒药物的不良反应,益生菌作为经验性用药,其对患者腹泻的临床缓解作用不明确.
实验动机
本研究希望通过对比研究,得出益生菌使用的有效性证据,为益生菌用于COVID-19伴腹泻患者治疗中的必要性进行分析,为该类患者提供有效的治疗用药.
实验目标
保证COVID-19伴腹泻患者在治疗过程中有效的用药.
实验方法
纳入我院年龄30-70岁所有普通型COVID-19伴腹泻患者,将甲亢、糖尿病、肠道恶性肿瘤、肠易激综合征作为排除标准,统计使用和未使用益生菌患者总数,并将其分为实验组和对照组,分析年龄、粪便脓细胞结果的影响,分析两组腹泻病程差别有无统计学意义.
实验结果
(1)两组受试者年龄和粪便脓细胞差异无统计学意义;(2)益生菌使用组中腹泻病程较未使用益生菌组短.
实验结论
(1)益生菌可明显缓解腹泻患者症状;(2)肠道菌群平衡可显著提高患者内环境稳定,益生菌在肠源性感染的控制中起到有利作用;(3)新型冠状病毒肺炎患者中,部分患者腹泻病因为药物不良反应导致,益生菌亦可对其起到积极作用;(4)本研究仅仅使用布拉氏酵母菌散作为菌种,可见酵母菌在维持肠道菌群平衡中发挥着重要作用.
展望前景
作为庞大的细菌库,肠道菌群种类繁多,对于有益菌种,人类了解甚少,在未来的研究中需加大对肠道菌群的探索,尽可能提取出较多有益于人类健康的微生物群,发挥其在胃肠道疾病治疗中不可替代的作用.

