2-[4-[2-[4-[1-(2-乙氧基)苯并咪唑-2-基]哌啶-1-基]乙基]苯基]-2-甲基丙酸的合成
钟雪彬,王 晓,王正泽,林 辉
(南京长澳医药科技有限公司,江苏 南京 210000)
比拉斯汀(Bilastin,1,商品名:Bilaxten),新型第2代组胺H1受体拮抗剂,2010.9.10在西班牙上市。系新型长效组胺拮抗剂,能选择性拮抗周围H1受体而对毒蕈碱受体无明显的亲和性。起效快且可持续作用24 h,避免中枢神经系统和心血管的不良反应及具有良好的药动学性质(即吸收快、生物利用度高、体内半减期长、不被肝脏代谢和主要随粪便排泄)。比拉斯汀安全性良好,无常用抗组胺药物存在的对中枢神经镇静作用及对心血管系统的毒副作用。
1的合成关键中间体片段为苯乙基羟基结构,已有的文献都是围绕该片段的合成进行不同尝试,主要包括:a)通过格氏试剂或者锂盐与环氧乙烷实现增长碳链;b)通过溴苯与有机锡试剂的Still偶联反应或者与有机硼试剂的Suzuki偶联反应实现增长碳链;c)通过溴苯与活泼双键的Heck偶联反应实现增长碳链;d)通过傅克酰基化反应实现增长碳链,再进行羰基还原成亚甲基。
在上述方法中使用了易致癌性物质环氧乙烷,易爆易燃,生产时有一定的安全风险;格氏试剂和丁基锂的使用需要无水无氧条件,操作条件严苛;反应使用了有毒试剂碘甲烷,还有昂贵的金属钯催化剂,有机锡剧毒试剂,这些试剂都不能适用工业化的生产,导致生产成本较高,会对操作人员的健康造成损害和产生环境污染等问题。因此,开发出一条经济安全的合成路线显得尤其重要。
我们在经过文献对比,选取以4-(2-溴乙酰基)-α,α-二甲基苯乙酸乙酯(2)为起始原料,先在酸性还原体系三乙基硅烷和三氟化硼乙醚中,将羰基还原成亚甲基(3),再与2-(哌啶-4-烷基)-1H-苯并咪唑(4)在有机碱N’N-二异丙基乙胺的作用下进行缩合,然后在无水条件下使用氢化钠拔氢,与氯代乙基乙基醚(6)缩合得到(7),最后,在氢氧化钠的乙醇溶液中,将酯基水解得到比拉斯汀(1)。
1的合成路线见图1。

图1 比拉斯汀的合成
1 实验部分
1.1 2-(4-(2-溴乙基)苯基)-2-甲基丙酸乙酯(3)的合成
将2(3.0 kg,9.58 mol,1 equiv)、三乙基硅烷(4.46 kg,38.30 mol,4 equiv)投入二氯甲烷(18 L,6 equiv,v/m)中,搅拌使之溶清。外用冰浴降温,控制内温不超过5℃,滴加入三氟化硼乙醚溶液(11.18 kg,76.64 mol,8 equiv),加料完毕,升温加热至50~55℃,反应3~4 h。反应完毕,冷却到常温,倾入水(90 L)中淬灭,用碳酸氢钠(13.5 kg)调节pH值至6~7,静置分层,上层水相再用二氯甲烷(25 L×2)萃取,合并有机相,用水(20 L)洗涤,向有机相中加入无水硫酸钠(10 kg),搅拌脱水。过滤,滤饼用适量二氯甲烷洗涤,滤液合并减压浓缩,先水浴温度(40±2)℃、压力≤-0.09 MPa浓缩至无液滴滴下,再升温至(70±2)℃、压力≤-0.09 MPa浓缩30min。得淡黄色残液3(2.86 kg),收率为100%。ESI-MS(m/z):300.21[M+H]+;1H-NMR(d6-DMSO,300 MHz,TMS)δ7.32(d,J=8.4 Hz,2H,Ar-H),δ7.20(d,J=8.4 Hz,2H,Ar-H),δ3.67(s,3H,OCH2CH3),δ3.62(s,2H,OCH2CH3),δ3.58(t,J=7.7 Hz,2H,Br-CH2CH2-Ph),δ3.17(t,J=7.7 Hz,2H,Br-CH2CH2-Ph),δ1.60(s,6H,C(CH3)2)。
1.2 2-[4-[2-[4-[1H-苯并咪唑-2-基]哌啶-1-基]-乙基]苯基]-2-甲基丙酸乙酯(5)的合成
将4(2.13 kg,10.57 mol,1.11 equiv)、N, N-二异丙基乙胺(3.42 kg,26.49 mol,2.78 equiv)投入到DMF(17.1 L,6 equiv,v/m)中,搅拌下升温到(60±2)℃,并保持在该温度下滴加入3(2.85 kg,9.53 mol,1 equiv)的DMF溶液(5.7 L,2 equiv,v/m),滴毕,保持内温(60±2)℃反应5~6 h。反应毕,冷却到常温,倾入冰水(75 L)中搅拌30min。离心滤得固体用少量水洗,再次抽干。用正己烷(30 L)(正己烷:3=10:1~15:1,v/m)回流打浆30 min,趁热抽滤,滤饼用少量正己烷洗涤,滤干,滤饼于(50±2)℃鼓风干燥至恒重,得淡黄色至类白色固体5(3.247 kg),收率81.2%。1H-NMR(d6-DMSO,300MHz,TMS),δ7.78~7.19(m,8H,Ar-H),δ3.67(d,3H,OCH2CH3),δ3.62(s,2H,OCH2CH3),δ3.20~3.17(t,4H,N-CH2CH2-Ph),δ3.07(m,1H,CH),δ2.86~2.82(m,2H,CH2N),δ2.23~2.20(m,4H,CH2CHCH2),δ1.60(s,6H,C(CH3)2)。
1.3 2-[4-[2-[4-[1-(2-乙氧乙基)苯并咪唑-2-基]哌啶-1-基]乙基]苯基 ]-2-甲基丙酸乙酯(7)的合成
将5(3.20 kg,7.63 mol,1 equiv)投入到干燥的DMF(25.6 L,8 equiv,v/m)中,搅拌下将NaH(0.46 kg,11.45 mol,1.5 equiv)分批缓慢投入反应液中,保持内温20~25℃,搅拌2~3 h。然后加入6 (2.48 kg,22.88 mol,3 equiv),升温到(80±2)℃,反应2~3 h。反应毕,将反应液倾入冰水(75 L)中,乙酸乙酯(30 L×3)萃取,合并有机相,用水(25 L×2)洗涤。有机相用无水硫酸钠(5 kg)干燥。过滤,在水浴温度(50±2)℃、压力≤-0.09 MPa下减压浓缩除去溶剂,得深褐色至红色油状物7(3.73 kg),收率:99.4%。1H-NMR(d6-DMSO,300 MHz,TMS),δ7.78~7.19(m,8H,Ar-H),δ4.32(t,2H,NCH2),δ3.73(t,2H,OCH2),δ3.66(t,3H,OCH2CH3),δ3.40(s,2H,OCH2CH3),δ3.36(s,2H,OCH2CH3),δ3.20~3.17(t,4H,N-CH2CH2-Ph),δ3.07(m,1H,CH),δ2.86~2.82(m,2H,CH2N),δ2.69~2.66(m,2H,CH2N),δ2.23~2.20(m,4H,CH2CHCH2),δ1.60(s,6H,C(CH3)2),δ1.12(t,3H,OCH2CH3)。
1.4 比拉斯汀(1)的合成
将7(3.70 kg,7.53 mol,1 equiv)、氢氧化钠(2.41 kg,60.2 mol,8 equiv)投入到乙醇(30 L,8 equiv,v/m)中,搅拌加热至回流,反应2~3 h,反应毕,(50±2)℃减压浓干,加入水(40 L)溶解,冰浴下,保持搅拌下用浓盐酸(约3.5 L)缓慢调节pH值至6.0~7.0,并继续搅拌30 min,离心滤得固体用水洗两次。(55±2)℃鼓风干燥至恒重。得红棕色固体比拉斯汀(2.85 kg),收率:81.6%。
ESI-MS(m/z):464.30为[M+H]+,486.30为[M+Na]+。
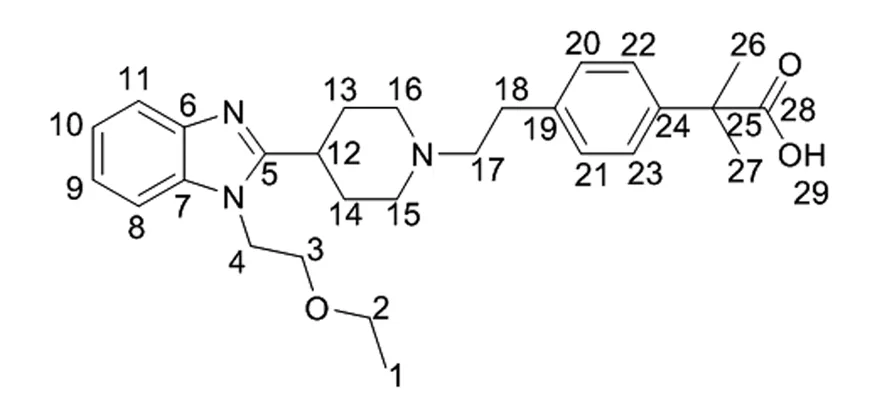
1H-NMR(d6-DMSO,500 MHz,TMS)δ7.547~7.567 (d,J=7.55 Hz,1H),H11。δ7.504~7.526 (d,J=7.35 Hz,1H),H8。δ7.256~7.278 (d,J=8 Hz,2H),H20,21。δ7.191~7.212 (d,J=7.9 Hz,2H),H22,23。δ7.141~7.175 (m,2H),H9,10。δ4.383~4.407 (t,J=6 Hz,2H),H4。δ3.641-3.666 (t,J=6 Hz,2H),H3。δ3.323-3.375 (t,J=8.1 Hz,2H),H2。δ3.021-3.090 (m,3H),H15e,16e。δ2.727~2.766 (t,J=9 Hz,2H),H18。δ2.537~2.576 (t,J=8.5 Hz,2H),H17。δ2.091~2.143 (m,2H),H15a,16a。δ1.864~1.919 (m,4H),H13,14。δ1.462 (s,6H),H26,27。δ0.990-1.024 (t,J=8.5 Hz,3H ),H1。

