类水滑石脱除溶液中Cl-的工艺条件研究
江 晓,杨保俊,赵德先,陈明阳,王百年
(合肥工业大学化学与化工学院,安徽合肥230009)
我国众多行业在生产过程中会产生大量含Cl-废水,如食品、石油化工、制革、造纸等行业。 水体中Cl-含量过高,不仅会对设备造成腐蚀,严重时会污染地下水资源。 因此,高效脱除工业废水中的Cl-具有重要意义。
目前去除废水中Cl-的方法主要有:分离法、沉淀法、氧化还原法、离子交换法等〔1〕。 其中,离子交换法中的类水滑石法是处理含Cl-废水的一种重要方法。 类水滑石(LDHs)是一种层状双金属氢氧化物,其通式为〔M1-x2+Mx3+(OH)2〕x+(An-)x/n·mH2O〔2〕,其中,M2+是二价阳离子(Mg2+、Zn2+等),M3+是三价阳离子(Al3+、Fe3+等 ),An-为 层 间 可 交 换 的 阴 离 子 (CO32-、NO3-等),x 在0.2~0.33 之间。 由于LDHs 层间阴离子的可交换性,以及LDHs 煅烧产物——层状双金属氧化物(LDO)结构的可重建性等,使得LDHs 及其LDO具有较优异的阴离子(如F-,PO43-等)脱除性能,已成为废水脱氯技术研发的热点。
安徽某腈纶生产企业在溶剂循环使用过程中,由于聚合反应工序氯酸钠的添加、纺丝工序用工业水带入Cl-等缘故,近年来循环溶剂中的Cl-一直保持在800~1 000 mg/L,已经造成设备和管道的严重腐蚀。 对此,本研究在不同改性剂作用下,采用共沉淀法制备了不同板层阳离子的CO32-型类水滑石(LDHs),并经焙烧制备了LDO。 以自制的800 mg/L NaCl 溶液为模拟含Cl-废水, 以废水中Cl-的脱除量为评价指标,筛选并确定出较适宜的Cl-脱除剂,并进一步考察了其对Cl-的脱除效果及再生循环使用性能。
1 实验部分
1.1 试剂与仪器
试剂:Mg(NO3)2·6H2O、Cu(NO3)2·3H2O、C2H5OH、Ni (NO3)2·6H2O、Zn (NO3)2·6H2O、Al (NO3)3·9H2O、NaOH、Na2CO3、NaCl、AgNO3、 (CH2OH)2、 (C6H11NO4)n、K2CrO4、HO(CH2CH2O)nH、(C6H10O5)n、C3H8O3,均为分析纯,使用前未经任何处理。
仪器:CP214 电子天平,奥豪斯仪器(常州)有限公司;HH-2 数显恒温水浴锅、CJJ-931 四联加热磁力搅拌器, 常州国宇仪器制造有限公司;DHG-9076A 电热鼓风干燥箱,上海精宏实验设备有限公司;QM-3SP4 行星式球磨机,南京大学仪器厂; PHS-3E型pH 计, 上海仪电科学仪器股份有限公司;KSL-1700X-A2 马弗炉,合肥科晶材料技术有限公司;D/MAX2500 型X 射线衍射仪,日本理学公司;Nicolet 6700 型傅里叶红外光谱仪,美国尼高力仪器公司。
1.2 实验方法
1.2.1 LDHs、LDO 的制备
采用共沉淀法制备CO32-型LDHs。 取0.24 mol的Mg(NO3)2·6H2O、Cu(NO3)2·3H2O、Ni(NO3)2·6H2O、Zn(NO3)2·6H2O 分 别与0.08 mol 的Al(NO3)3·9H2O溶于200 mL 去离子水中,得盐溶液A。 取0.16 mol的Na2CO3与0.68 mol 的NaOH 溶于200 mL 去离子水中,得碱溶液B。 在65 ℃水浴恒温剧烈搅拌下,将盐溶液A 和碱溶液B 混合于水溶液(不加入改性剂或分别加入质量分数6%左右的淀粉、聚乙二醇、壳聚糖或体积分数15 %的乙醇、乙二醇、丙三醇改性剂)中,再用碱溶液B 调节体系pH 至约10,搅拌晶化4 h。 70 ℃下陈化24 h,抽滤、洗涤、烘干、研磨,制得系列LDHs 样品。
将计量的LDHs 样品放入坩埚并置于马弗炉中,在确定的温度下焙烧一定时间,即制得相应的LDO 样品。
1.2.2 Cl-脱除实验
取100 mL 800 mg/L 的Cl-溶液于250 mL 烧杯中,加入计量脱氯剂,在25 ℃下搅拌反应一定时间。过滤、洗涤,将滤液定容至250 mL 容量瓶中,用硝酸银滴定法(GB/T 11896—1989)测定滤液中Cl-浓度。重复3 次取平均值,计算Cl-脱除量、脱除率。
1.2.3 脱氯剂再生和重复使用实验
将脱除Cl-后的LDO 置于0.1 mol/L 解吸液Na2CO3中,常温下搅拌解吸4 h。 过滤、洗涤、干燥,再将所得样品放入坩埚并置于马弗炉中, 于500 ℃下焙烧4 h,即得到再生后的LDO。 按1.2.2 所述步骤进行循环Cl-脱除实验。
2 结果与讨论
2.1 脱氯剂的筛选
在溶液初始pH 为7, 脱氯剂投加量为7.5 g/L,脱除时间为4 h 的条件下, 分别考察不同板层阳离子(Mg2+、Zn2+、Cu2+、Ni2+)、不同改性剂(聚乙二醇、壳聚糖、乙醇、乙二醇、淀粉、丙三醇)下制备的LDHs及LDO(焙烧温度500 ℃、焙烧时间4 h)对Cl-的脱除效果,结果如表1 所示。
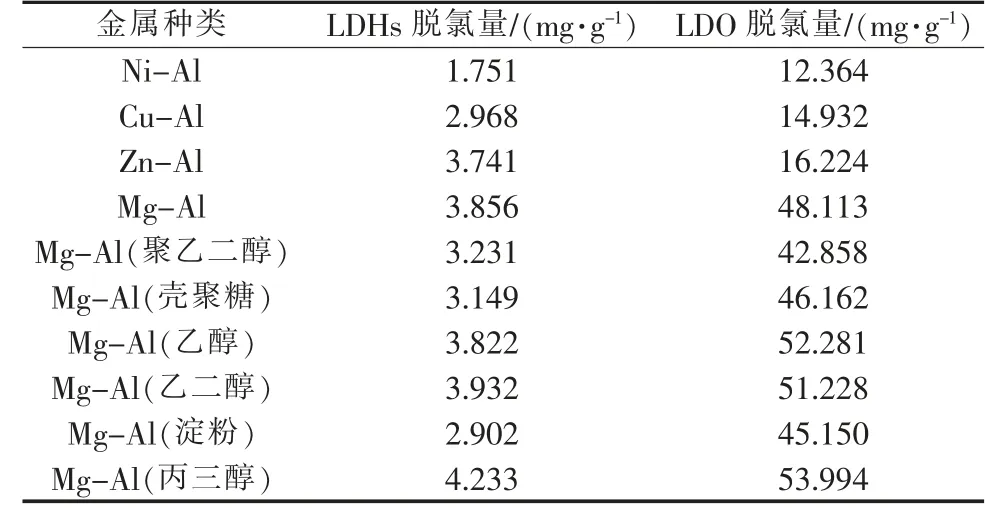
表1 不同改性剂条件下制备的不同板层阳离子LDHs 及LDO 的脱氯性能
由表1 可以看出,不同改性剂条件下制备的不同板层阳离子LDHs 的Cl-脱除量均较小, 而LDO 的Cl-脱除量远大于其相应的LDHs, 其中丙三醇改性Mg-Al-LDO 对Cl-的脱除量最大,可达53.994 mg/g。 后续实验中选择丙三醇改性Mg-Al-LDO 作为脱氯剂。
2.2 丙三醇改性Mg-Al-LDO 脱除Cl-工艺条件
2.2.1 焙烧温度对Cl-脱除量的影响
在焙烧时间为4 h,溶液初始pH 为7,LDO 投加量为7.5 g/L,脱除时间为4 h 的条件下,考察不同焙烧温度下制备的丙三醇改性Mg-Al-LDO 对Cl-的脱除效果,结果如图1 所示。
从图1 可以看出,当焙烧温度<500 ℃时,制备的LDO 的Cl-脱除量随焙烧温度的升高而增加;当焙烧温度为500 ℃时,LDO 的Cl-脱除量达到最大;当焙烧温度>500 ℃时,LDO 的Cl-脱除量随焙烧温度的升高反而下降。这可能是由于焙烧温度过高,会使LDO 转变成尖晶石(MgAl2O4)结构,导致Cl-脱除量降低。 适宜的焙烧温度为500 ℃。
2.2.2 焙烧时间对Cl-脱除量的影响
在焙烧温度为500 ℃, 溶液初始pH 为7,LDO投加量为7.5 g/L,脱除时间为4 h 的条件下,考察不同焙烧时间下制备的丙三醇改性Mg-Al-LDO 对Cl-的脱除效果,结果如图2 所示。
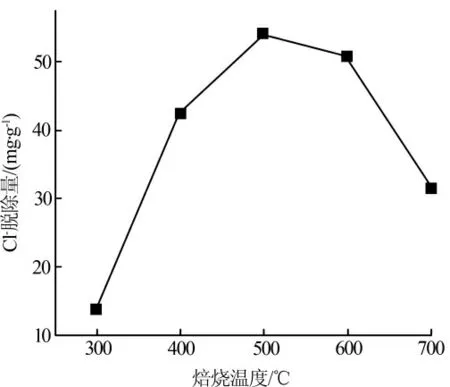
图1 不同焙烧温度下制备的丙三醇改性Mg-Al-LDO 对Cl-的脱除效果
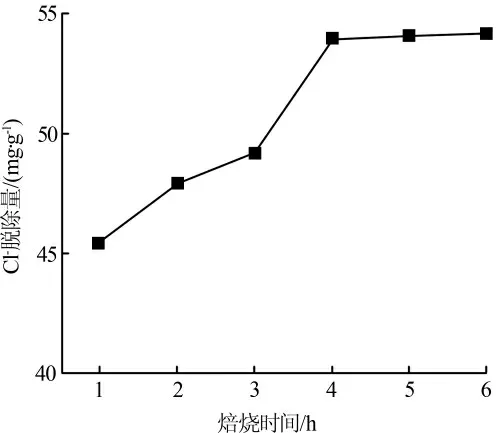
图2 不同焙烧时间下制备的丙三醇改性Mg-Al-LDO 对Cl-的脱除效果
从图2 可以看出,当焙烧时间<4 h 时,制备的LDO 的Cl-脱除量随焙烧时间的增加而快速提高;当焙烧时间为4 h 时,LDO 的Cl-脱除量达53.994 mg/g;当焙烧时间>4 h 时,随焙烧时间的延长,LDO的Cl-脱除量几乎不变。 综合考虑,适宜的焙烧时间为4 h。 后续采用焙烧温度为500 ℃、焙烧时间为4 h条件下制备的丙三醇改性Mg-Al-LDO 进行实验。
2.2.3 脱除时间对Cl-脱除量的影响
在溶液初始pH 为7,LDO 投加量为7.5 g/L 的条件下,考察脱除时间对Cl-脱除量的影响,结果如图3 所示。
由图3 可以看出, 当脱除时间<360 min 时,随着脱除时间的延长,Cl-脱除量不断增加; 当脱除时间为360 min 时,Cl-脱除量达到56.238 mg/g;当脱除时间>360 min 时, 随脱除时间的延长,Cl-脱除量几乎无变化。 较适宜的脱除时间为6 h。
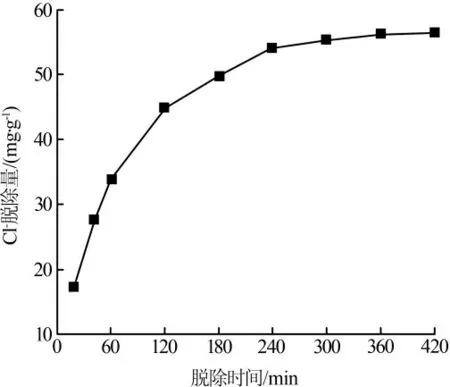
图3 脱除时间对Cl-脱除量的影响
2.2.4 溶液初始pH 对Cl-脱除量的影响
在LDO 投加量为7.5 g/L,脱除时间为6 h 的条件下,考察溶液初始pH 对Cl-脱除量的影响,结果如图4 所示。
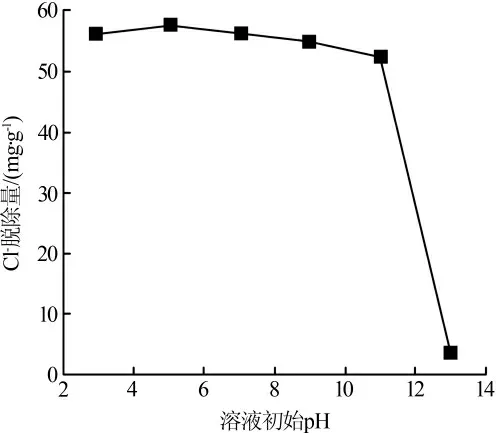
图4 溶液初始pH 对Cl-脱除量的影响
由图4 可以看出,溶液初始pH 在3~11 的范围内时,Cl-脱除量总体变化不大。 当溶液初始pH 为5 时,Cl-脱除量最大,为57.484 mg/g。 酸性条件下,LDO 表面发生质子化带正电荷,可增强LDO 与溶液中Cl-之间的静电吸引作用。 当溶液初始pH 由9 升至11 时,LDO 的表面电荷由正值转变为负值,与溶液中Cl-之间的静电作用由静电吸引转变为静电排斥〔3〕,导致Cl-脱除量缓慢减小。 当溶液初始pH 由11 升至13 时,Cl-脱除量快速下降。 这是由于体系碱性过强,OH-占据LDO 有限的脱Cl-位点, 与溶液中的Cl-形成竞争〔4〕。
2.2.5 LDO 投加量对Cl-脱除量的影响
在脱除时间为6 h, 溶液初始pH 为5 的条件下,考察LDO 投加量对Cl-脱除量的影响,结果如图5 所示。
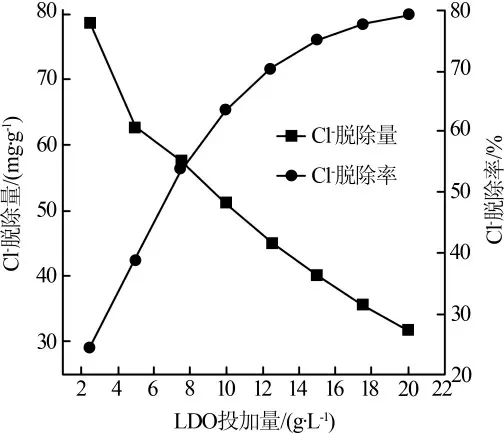
图5 LDO 投加量对Cl-脱除量的影响
由图5 可以看出,随着LDO 投加量的增加,Cl-脱除率不断增加,但增加速率逐渐平缓。 当LDO 投加量增加到20 g/L 时,Cl-脱除率达79.85%。Cl-脱除量则随着LDO 投加量的增加而不断下降。 这是由于随着LDO 加入量的增加,提供的吸附位点增多,有利于Cl-的脱除,所以脱除率增加;但溶液中Cl-的总量一定,随着LDO 投加量的增加,单位质量LDO 所能脱除的Cl-减少,导致Cl-脱除量下降〔5〕。当LDO 投加量增加到15 g/L,Cl-脱除量为40.185 mg/g,脱除率为75.35%;继续增加LDO 投加量,Cl-脱除率变化不大。为避免造成LDO 的浪费,选择适宜的LDO 投加量为15 g/L。
2.2.6 重复实验
通过上述单因素实验确定了较适宜的脱氯工艺条件:焙烧温度500 ℃,焙烧时间4 h,Cl-初始质量浓度800 mg/L,脱除温度25 ℃,脱除时间6 h,溶液初始pH 为5,丙三醇改性Mg-Al-LDO 投加量15 g/L。在此条件下,进行了3 次重复实验,结果见表2。
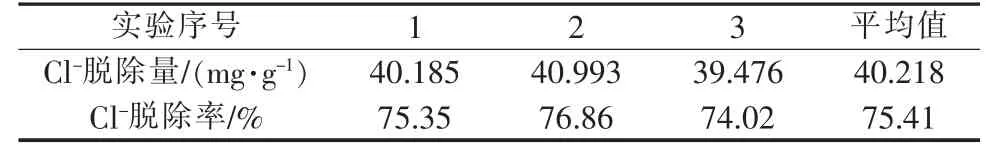
表2 优化工艺条件下的3 次重复实验结果
2.3 脱除特性研究
2.3.1 吸附动力学
采用准一级动力学方程和准二级动力学方程〔6〕分别对2.2.3 实验数据进行线性拟合,结果见表3。

表3 吸附动力学模型拟合参数
由表3 可以看出, 丙三醇改性Mg-Al-LDO 脱除溶液中Cl-的过程能较好地符合准二级动力学方程,说明脱除过程存在吸附活性中心与溶液中Cl-的化学键合。
2.3.2 等温吸附
在初始Cl-质量浓度分别为400、600、800、1 000、1 200、1 400、1 600、1 800 mg/L,溶液初始pH 为7,LDO 投加量为7.5 g/L, 脱除时间为4 h 的条件下进行等温吸附实验,并采用Langmuir 和Freundlich等温吸附模型〔7〕对等温吸附数据进行拟合,结果见表4。

表4 等温吸附模型拟合参数
由表4 可知,2 种模型均能较好地描述丙三醇改性Mg-Al-LDO 对溶液中Cl-的脱除, 其中,Langmuir 模型拟合程度更高,说明脱除过程存在均匀的单层吸附。
2.4 脱氯剂的再生和循环使用
对脱氯后的丙三醇改性Mg-Al-LDO 进行再生和循环使用实验。结果表明,第1 次使用后的再生率为84.56%,第2 次使用后的再生率为69.37%,第3次使用后的再生率为54.95%,第4 次使用后的再生率为41.48%。可见,随着再生次数的增加,LDO 再生率逐渐下降。 这可能是随着多次解吸,LDO 质量发生了损失,同时随着多次焙烧,部分LDO 转变成尖晶石(MgAl2O4)结构。 但经4 次再生循环后,其仍具有40%以上的再生率, 这表明丙三醇改性Mg-Al-LDO 具有良好的再生能力, 可多次再生循环使用,由此降低了脱氯工艺的操作成本。
2.5 脱氯剂表征
2.5.1 XRD 分析
图6 为脱氯前Mg-Al-LDHs、丙三醇改性Mg-Al-LDHs、丙三醇改性Mg-Al-LDO 以及脱氯后丙三醇改性Mg-Al-LDO 样品的XRD 表征结果。
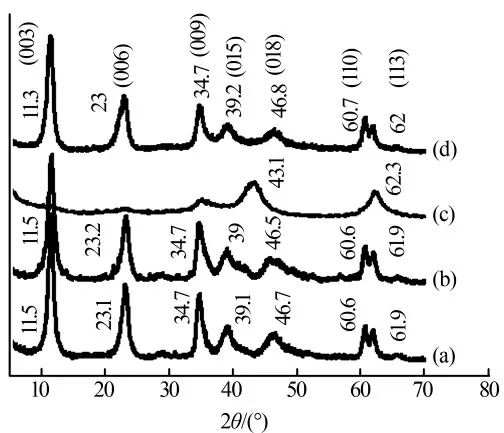
图6 脱氯前Mg-Al-LDHs(a)、丙三醇改性Mg-Al-LDHs(b)、丙三醇改性Mg-Al-LDO(c)以及脱氯后丙三醇改性Mg-Al-LDO(d)样品的XRD 图
由图6 可以看出,脱氯前的Mg-Al-LDHs、丙三醇改性Mg-Al-LDHs 样品在2θ 为11.5°、23.1°、34.7°、39.1°、46.7°、60.6°、61.9°附近出现类水滑石特征衍射峰,分别对应于类水滑石的(003)、(006)、(009)、(015)、(018)、(110)、(113)晶面,说明改性剂丙三醇未改变LDHs 的结构;且基线平稳,各衍射峰峰型尖锐对称,说明所制备的Mg-Al-LDHs、丙三醇改性Mg-Al-LDHs 晶相单一,结晶度较好〔8〕。 经500 ℃焙烧后的丙三醇改性Mg-Al-LDO 对应的(003)、(006)等特征衍射峰消失, 在2θ 为43.1°、62.3°处出现镁铝混合氧化物的特征衍射峰, 说明LDHs 的层状结构被破坏,转变成镁铝氧化物〔9〕。 脱氯后的丙三醇改性Mg-Al-LDO 的(003)、(006)等特征衍射峰重新出现,但相应的衍射峰变宽,结晶度变差。 分析认为:LDO 具有特殊的记忆效应,Cl-进入层间,Cl-成为层间 阴 离 子 ,LDO 又 变 为 原 有LDHs 的 层 状 结 构〔10〕。
2.5.2 FT-IR 分析
图7 为脱氯前丙三醇改性Mg-Al-LDHs、 丙三醇改性Mg-Al-LDO 以及脱氯后丙三醇改性Mg-Al-LDO 样品的FT-IR 图。
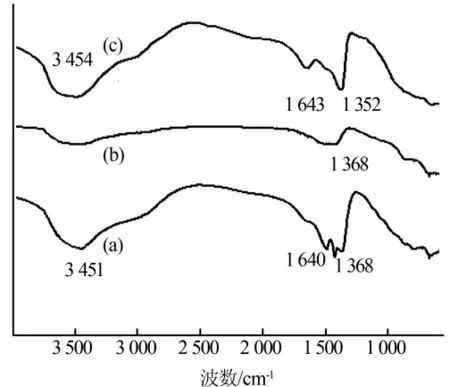
图7 脱氯前丙三醇改性Mg-Al-LDHs(a)、丙三醇改性Mg-Al-LDO(b)以及脱氯后丙三醇改性Mg-Al-LDO(c)样品的FT-IR 图
由图7 可以看出, 脱氯前丙三醇改性Mg-Al-LDHs、脱氯后丙三醇改性Mg-Al-LDO 分别在3 451、3 454 cm-1处出现了羟基的伸缩振动峰。丙三醇改性Mg-Al-LDHs 在1 640 cm-1处对应于水分子的弯曲振动峰, 在1 368 cm-1处为层间CO32-的反对称伸缩振动峰〔11〕;经焙烧后,1 640 cm-1处的水分子的弯曲振动峰消失,3 451 cm-1处的羟基伸缩振动峰以及1 368 cm-1处的CO32-振动峰强度明显减弱, 表明经高温焙烧后丙三醇改性Mg-Al-LDO 样品的层板羟基以及层间结晶水脱水,层间大部分CO32-发生了分解。 脱氯后丙三醇改性Mg-Al-LDO 样品的CO32-振动峰从1 368 cm-1移到1 352 cm-1处, 这可能是Cl-进入层间后与CO32-相互作用引起的〔12〕。
3 结论
(1)在不同改性剂作用下,采用简单的共沉淀法制备出具有不同板层阳离子的CO32-型LDHs 及LDO。 以废水中Cl-脱除量为评价指标,筛选并确定出丙三醇改性Mg-Al-LDO 为较适宜的Cl-脱除剂。
(2)通过单因素实验确定了较适宜的Cl-脱除工艺条件:焙烧温度500 ℃,焙烧时间4 h, Cl-初始质量浓度800 mg/L,脱除温度25 ℃,脱除时间6 h,溶液初始pH 为5,LDO 投加量15 g/L。 此条件下重复实验结果显示,Cl-平均脱除量为40.218 mg/g, 平均脱除率为75.41%。
(3)丙三醇改性Mg-Al-LDO 脱除氯离子过程符合准二级动力学方程、Langmuir 等温吸附模型。
(4)在确定的优化再生工艺条件下,丙三醇改性Mg-Al-LDO 经4 次再生的再生率为41.48%。
(5)XRD、FT-IR 表征结果表明,丙三醇改性Mg-Al-LDO 脱除氯离子的过程存在结构记忆效应,氯离子进入层间,LDO 恢复LDHs 的层状结构。

