小麦纤维素颗粒微生物限度检查方法适用性研究
张威存,黄丽华
1.广州中医药大学第三附属医院,广州 510360;2.广东省药品检验所,广州510663
小麦纤维素颗粒约含80%的纤维素,其中不可溶性纤维素占比≥90%,是一种不能消化的纯天然纤维素制剂,颗粒直径0.8~2.0 mm,并含有大量亲水羟基,增加粪便体积的同时增加其水结合能力,使粪便的体积和质量增大,促进肠蠕动功能,使得粪便排出更加顺畅,是国家食品药品监督管理局批准的治疗便秘的制剂[1-4]。
药品微生物限度检查是目前药物安全的一个重要且有效的手段[5],为了确保小麦纤维素颗粒微生物限度检查法的准确性和可靠性,保证药品的用药安全,参照《中国药典》2015 年版微生物限度检查方法[6],根据小麦纤维素颗粒理化特性和微生物限度标准等因素选择适宜的计数方法和控制菌检查,并对其进行微生物限度方法适用性试验,建立微生物限度检查方法。
1 仪器与试药
1.1 仪器
CL-40M 高压灭菌器(日本ALP 株式会社);GRX-12A 干热消毒箱(上海森信实验仪器有限公司);LRH-250A 生化培养箱(广东省医疗器械厂);MIR-254-PC 恒温培养箱(松下健康医疗器械株式会社);BS323S 电子天平(赛多利斯公司,万分之一)。
1.2 样品
小麦纤维素颗粒,深圳市永科医药有限公司提供(生产企业:Sweden Recipharm Hoganas AB 公司;批号:250301、250302、250303,规格:每包3.5 g)。
1.3 方法适用性菌种
金黄色葡萄球菌[CMCC(B)26003],铜绿假单胞菌[CMCC(B)10104],枯草芽孢杆菌[CMCC(B)63501],大肠埃希菌[CMCC(B)44102],乙型副伤寒沙门菌 [CMCC(B)50094],白色念珠菌[CMCC(F)98001],黑曲霉[CMCC(F)98003],均由中国食品药品检定研究院提供,菌种均为第三代。
1.4 培养基
胰酪大豆胨琼脂培养基(简称TSA,批号:180124);胰酪大豆胨液体培养基(简称TSB,批号:1073065);沙氏葡萄糖琼脂培养基(简称SDA,批号:171207);沙氏葡萄糖液体培养基(简称SDB,批号:1071003);pH 7.0 无菌氯化钠-蛋白胨缓冲液(批号:181029);麦康凯液体培养基(批号:1075425);麦康凯琼脂培养基(简称MAC,批号:1076291);溴化十六烷基三甲铵琼脂培养基(简称NAC,170605);氧化酶试纸(批号:6105168);甘露醇氯化钠琼脂培养基(批号:170509);RV 沙门增菌液体培养基(批号:1086061);木糖赖氨酸脱氧胆酸盐琼脂培养基(批号:180524);三糖铁琼脂培养基(简称TSI,批号:1071771)。以上培养基均购自广东环凯微生物科技有限公司,按使用说明书配制,使用前进行培养基适用性检查,均符合规定。
2 方法与结果
2.1 计数方法适用性试验与结果
2.1.1 菌液的制备分别将金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌的新鲜培养物接种至TSB 中,置32 ℃培养箱中培养24 h;接种白色念珠菌的新鲜培养物至SDB 中,置23 ℃培养箱中培养48 h;将上述菌株培养物用0.9%无菌氯化钠溶液制成每1 mL含菌数为不大于104 cfu 的菌悬液,备用。接种黑曲霉的新鲜培养物至SDA 斜面培养基中,置23 ℃培养箱中培养7 d 后,加入含0.05%聚山梨酯80 的0.9%无菌氯化钠溶液5 mL,将孢子洗脱,收集孢子悬液至无菌试管内,用含0.05%聚山梨酯80 的0.9%无菌氯化钠溶液制成每l mL 含孢子数为不大于104 cfu的孢子悬液,备用。
2.1.2 供试液的制备取本品10 g,加pH 7.0 无菌氯化钠-蛋白胨缓冲液至200 mL,摇匀,静置5 min,取上清液作为1∶20 的供试液。
2.1.3 需氧菌、霉菌和酵母菌检查方法适用性试验试验组:分别取上述菌悬液0.1 mL,加至10.0 mL 供试液中,使各试验菌每1 mL 含菌量不大于100 cfu,混匀。分别取混匀好的溶液1 mL 注入平皿中,立即倾注相应的琼脂培养基(金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌组倾注TSA,白色念珠菌、黑曲霉组分别倾注TSA 和SDA 2 种培养基),每株试验菌平行制备2 个平皿,待凝,TSA 倒置于32 ℃培养箱培养3 d,SDA 倒置于23 ℃培养箱培养5 d,观察培养结果,以平均菌落数作为最终结果。
菌液对照组:取pH 7.0 无菌氯化钠-蛋白胨缓冲液替代供试液,按试验组方法操作加入试验菌液,并进行微生物回收试验。供试品对照组:取制备好的供试液,以稀释液代替菌液同试验组操作。
2.1.4 方法适用性试验结果小麦纤维素颗粒微生物计数结果见表1,从表中可以看出1∶20 供试液微生物检查中,需氧菌,霉菌及酵母菌总数计数的回收比值均在0.5~2.0 范围内,且回收比值均在0.8以上,3 次均能重现试验结果。故该计数方法适用于小麦纤维素颗粒的微生物检查。
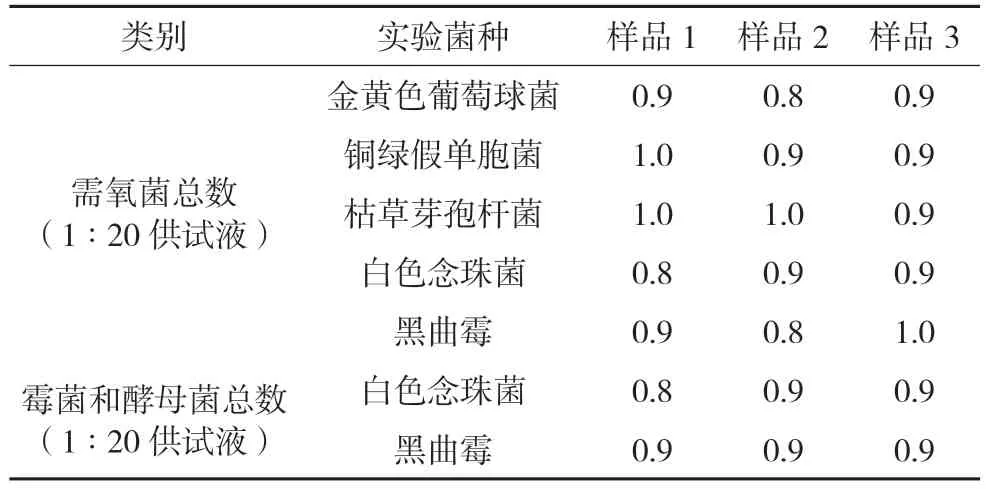
表1 小麦纤维素颗粒微生物计数方法试验回收比值
2.2 控制菌检查方法适用性试验与结果
本品控制菌检查包括有大肠埃希菌、铜绿假单胞菌、金黄色葡萄球菌、沙门菌。
2.2.1 菌液制备分别取大肠埃希菌、铜绿假单胞菌、金黄色葡萄球菌、乙型副伤寒沙门菌的新鲜培养物接种至TSB 培养基中,置32 ℃培养24 h;培养物用0.9%无菌氯化钠溶液制成每mL 含菌数不大于102 cfu 的菌悬液,备用。
2.2.2 供试液的制备取本品10 g,加pH 7.0 无菌氯化钠-蛋白胨缓冲液至200 mL,摇匀,静置5 min,取上清液作为1∶20 的供试液
2.2.3 大肠埃希菌控制菌检查法的适用性试验阳性对照组:取上述1∶20 供试液20 mL 及每mL 含菌数不大于102 cfu 大肠埃希菌的菌液1 mL,加至200 mL TSB 中,32 ℃培养24 h 后,取培养物1 mL 接种至100 mL 麦康凯液体培养基中,43 ℃培养48 h。取麦康凯液体培养物划线接种于MAC 平板上,32 ℃培养72 h。
供试品对照组:取制备好的供试液,以pH 7.0无菌氯化钠-蛋白胨缓冲液代替菌液,同阳性对照组方法操作。阴性对照组:取pH 7.0 无菌氯化钠-蛋白胨缓冲液替代供试液,不加菌液,进行阴性对照组试验。
2.2.4 铜绿假单胞菌控制菌检查法的适用性试验阳性对照组:取上述1∶20 供试液20 mL 及每mL 含菌数不大于102cfu 铜绿假单胞菌的菌悬液1 mL,加至200 mL TSB 中,32 ℃培养24 h 后,取培养物划线接种于NAC 平板上,32 ℃培养72 h 后,取平板上生长的菌落进行氧化酶试验(用玻棒挑起新鲜培养物于氧化酶试纸表面,观察菌落颜色,阳性为红色,阴性不变色)。
供试品对照组:取制备好的供试液,以pH 7.0 无菌氯化钠-蛋白胨缓冲液代替菌液,同试验组方法操作。阴性对照组:取pH 7.0 无菌氯化钠-蛋白胨缓冲液替代供试液,不加菌液,进行阴性对照组试验。
2.2.5 金黄色葡萄球菌控制菌检查法的适用性试验阳性对照组:取上述1∶20 供试液20 mL 及每mL 含菌数不大于102cfu 金黄色葡萄球菌的菌悬液1 mL,加至200 mL TSB 中,32 ℃培养24 h 后,取培养物划线接种于甘露醇氯化钠琼脂培养基平板上,32℃培养72 h。
供试品对照组:取制备好的供试液,以pH 7.0 无菌氯化钠-蛋白胨缓冲液代替菌液,同试验组方法操作。阴性对照组:取pH 7.0 无菌氯化钠-蛋白胨缓冲液替代供试液,不加菌液,进行阴性对照组试验。
2.2.6 乙型副伤寒沙门菌控制菌检查法的适用性试验阳性对照组:取供试品10 g 及每mL 含菌数不大于102cfu 乙型副伤寒沙门菌的菌悬液1 mL,加至200 mL TSB 中,32 ℃培养24 h 后,取培养物0.1 mL接种至10 mL RV 沙门增菌液体培养基中,32 ℃培养24 h。取少量RV 沙门菌增菌液体培养物划线接种于木糖赖氨酸脱氧胆酸盐琼脂培养基平板上,32 ℃培养48 h。若木糖赖氨酸脱氧胆酸盐琼脂培养基平板上菌落生长良好,为淡红色或无色、透明或半透明、中心有或无黑色时用接种针挑选疑似菌落于TSI 高层斜面上进行斜面和高层穿刺接种,培养24 h。
供试品对照组:取制备好的供试液,以pH 7.0无菌氯化钠-蛋白胨缓冲液代替菌液,同试验组方法操作。阴性对照组:取pH 7.0 无菌氯化钠-蛋白胨缓冲液替代供试液,不加菌液,进行阴性对照组试验。
2.2.7 控制菌检查法的适用性试验结果小麦纤维素颗粒的控制菌检查结果见表2。由表可见3 个样品的阳性对照组结果均为阳性,分别检出大肠埃希菌、铜绿假单胞菌、金黄色葡萄球菌、乙型副伤寒沙门菌这4 种控制菌,而供试品对照组及阴性对照组均为阴性,未检出相应的控制菌。因此,小麦纤维素颗粒相应的控制菌可以按照《中国药典》2015 年版四部通则1106 非无菌产品微生物限度检查[6],该方法对小麦纤维素颗粒的控制菌检查适用性试验成立。
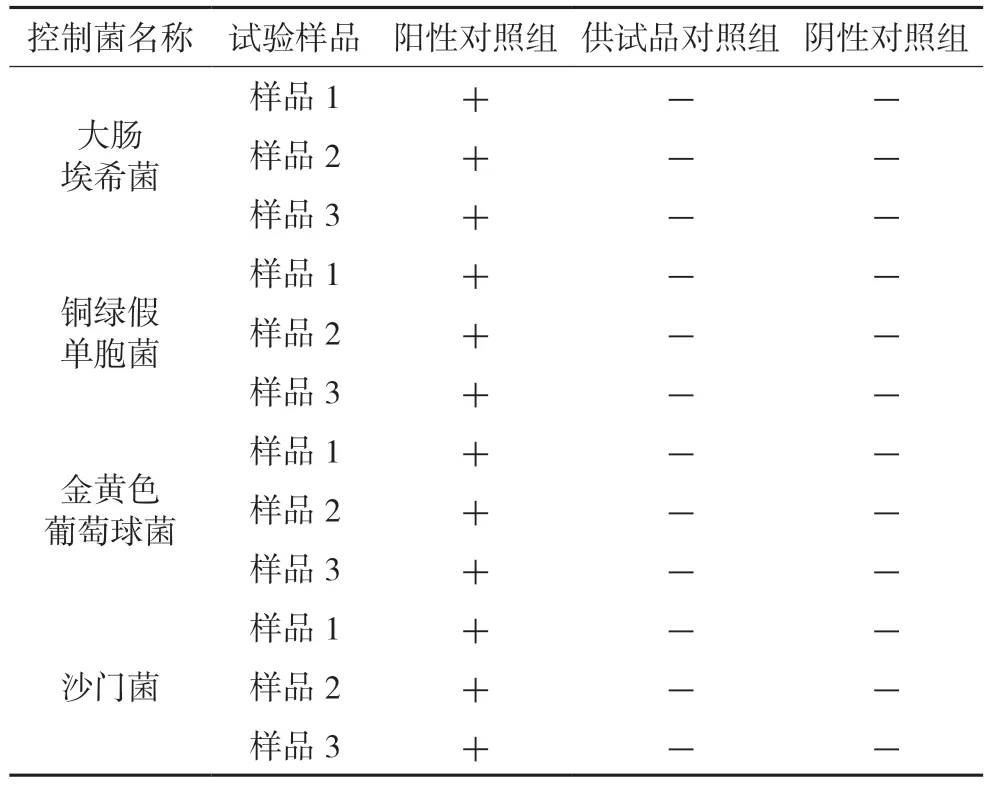
表2 小麦纤维素颗粒控制菌检查法的适用性试验结果
3 讨论
药品微生物限度检查的操作步骤繁杂,结果受多方面的影响[7]。为确保检查方法的准确性和完整性,首先要确认其计数方法适用性试验与控制菌检查方法适用性试验,以保证供试品中被污染的微生物能被检出,结果方属有效。
在小麦纤维素颗粒微生物检查时,采用1∶20的稀释倍数是由于本品吸水性较强,1∶10 的供试液很粘稠,无法吸取,故制成1∶20 的供试液进行计数方法适用性试验与控制菌检查方法适用性试验。值得注意的是,供试品稀释后需静置5 min,使其充分溶解于pH 7.0 无菌氯化钠-蛋白胨缓冲液中,再进行下一步试验。研究结果显示,计数方法试验中各试验菌回收比值均在0.5~2.0 范围内,且回收比值均在0.8 以上,说明该计数方法适用于小麦纤维素颗粒的需氧菌总数,霉菌及酵母菌的检查。
小麦纤维素颗粒是从麦麸中提取的纯天然纤维经过一定的加工而制成口服给药制剂,《中国药典》2015 年版四部通则[6]规定口服制剂控制菌检查中不得检出大肠埃希菌,因其含有纯天然的植物成分,每10 g 供试品中还不得检出沙门菌。另外,原料药小麦麦麸属于药食同源的植物,查阅相关食品质量标准[8]发现金黄色葡萄球菌是常见的食源性致病菌,广泛存在于自然环境中。它在适当的条件下,能够产生肠毒素,可引发食物中毒,化脓性感染及中毒性休克等症状[9]。值得注意的是小麦纤维素颗粒的生产工艺中也涉及到对铜绿假单胞菌的控制,铜绿假单胞菌是一种重要的革兰阴性条件致病菌,可引发人体呼吸道、泌尿道、消化道皮肤软组织及手术创面等多部位的急性或慢性感染[10]。基于金黄色葡萄球菌以及铜绿假单胞杆菌的致病性,为了更加严格控制小麦纤维素颗粒的微生物限度安全,其控制菌检查中还不得检出金黄色葡萄球菌以及铜绿假单胞杆菌。
4 结论
在对3 批样品进行的微生物限度检查方法适用性试验中,需氧菌、霉菌和酵母菌的各试验菌回收比值均在0.5~2.0 范围内,阳性对照组均检出试验菌,阴性对照组及供试品对照组均未检出,该微生物限度检查方法适用性成立。本文建立的方法适用于小麦纤维素颗粒的微生物限度检查。

