芬顿氧化法预处理化学镀镍废水影响因素研究
章龚鸿 ,殷若愚
(1.江西明森环保科技有限公司,江西 南昌 330038;2.江西理工大学江西省矿冶环境污染控制重点实验室,江西 赣州 341000)
基于镍的金属性特别弱这一特性,近年来,镀镍成为电镀工业中占比较大的镀种。由于化学镀生产工艺简单、节约能源而被大范围使用在电子、化工等工业领域当中[1]。化学镀镍废水包括化学镀镍废液以及在对镀件清洗时所产生的清洗水。化学镀镍废水的污染物主要为Ni和P,同时还伴随有大量的难降解有机物和无机物[2],从而导致COD含量也非常高。处理含镍废水的方法有化学沉淀法,氧化还原法,分离、吸附法及电化学法等。黄新[3]等采用浓度为100 g/L的Na2CO3,pH值≥9.3时,沉淀效果最佳。有学者用2-乙基磷酸和2,4,4-三甲基戊基膦酸及煤油作为萃取剂处理预沉淀的化学镀镍废水,取得较好效果[4-6]。Rahman[7]发现胺基膦酸阳离子交换树脂对化学镀镍废水中镍离子的吸附效果好。闫雷等人[8]使用电解法处理化学镀镍废水,镍的去除率高达97.1%以上。
论文以江西某电镀园区化学镀镍废水为研究对象,在分析化学镀镍废水水质基础上,以重金属镍和COD为考察目标,采用芬顿氧化法处理化学镀镍废水,围绕芬顿氧化法通过破络以预处理重金属镍及COD的影响因素进行研究。
1 实验水质与试验方法
1.1 化学镀镍废水水质
本实验用化学镀镍废水来源于江西某电镀园区,即将化学镀镍废液按一定比例加入到前处理样液中,混合均匀,得到化学镀镍废水,该废水水质情况如表1所示。

表1 化学镀镍废水水质情况
1.2 实验方法
分别取3种不同浓度的化学镀镍废水200 mL于3个烧杯中,分别加入适量的芬顿试剂,置于磁力搅拌器中反应一定时间。为了检测氧化效果,在磁力搅拌器中反应一定时间后,经NaOH溶液调节pH值为9,加PAM混凝沉淀后过滤,取上清液测定其中镍离子和COD含量。
采用原子吸收分光光度法测定废水中镍离子浓度。COD采用快速消解分光光度法(HJ/T399-2007)进行测定。
2 实验结果与分析
2.1 初始pH值的影响
为了研究溶液初始pH值对芬顿氧化化学镀镍废水的影响,保持H2O2投加量为0.12 mol/L,H2O2与Fe2+物质的量比为2∶1,反应时间1 h,考察四个不同初始pH值的影响,结果如图1所示。

图1 溶液初始pH值的影响

图2 H2O2投加量的影响
由图1中可知,随着化学镀镍废水初始pH值由3增加到9,镍离子的去除率由99.05%持续降低至44.03%,此时残余镍离子浓度为1.72 mg/L;而COD的去除率总体差异不大,其去除率最大出现在pH值=5时78.92%,而最低出现在pH值=9时70.51%。这可以从芬顿氧化的反应机理进行解释。酸性条件下,利用Fe2+作为H2O2的催化剂,生成具有很强氧化电性且反应活性很高的·OH,·OH在水溶液中与难降解有机物反应,使有机物结构破坏,最终氧化分解。同时Fe2+被氧化成Fe3+,产生混凝沉淀,可去除有机物。后续实验将不调节废水pH值。
2.2 H2O2投加量的影响
为了研究H2O2投加量对芬顿氧化法处理化学镀镍废水的影响,不调节废水pH值,并保持H2O2与Fe2+物质的量比为2∶1,反应时间为1 h,考察四个不同H2O2投加量的影响,结果如图2所示。
由图2可知,H2O2投加量对镍离子和COD去除率的影响趋势一致,均随着H2O2投加量的增加先升高再降低。当H2O2投加量为0.06 mol/L时,产生的·OH数量较少,不足以将废水中以络合物形式出现的镍以及COD完全氧化。当H2O2投加量增加到0.18 mol/L时,镍离子去除率达99.20%,COD去除率达83.51%,此时残余镍离子浓度为1.45 mg/L,残余COD浓度为122.81 mg/L。当H2O2投加量继续增加到0.24 mol/L时,镍离子去除率降低至78.76%,COD去除率降至64.32%,这是由于H2O2过量,溶液中残留的H2O2会与生成的·OH反应,使得镍离子和COD去除率均下降。
2.3 H2O2与Fe2+摩尔比的影响
为了研究H2O2与Fe2+摩尔比对芬顿氧化法处理化学镀镍废水的影响,不调节废水pH值,并保持H2O2的投加量为0.18 mol/L,反应时间1 h,考察四个不同H2O2与Fe2+物质的量比,结果如图3所示。
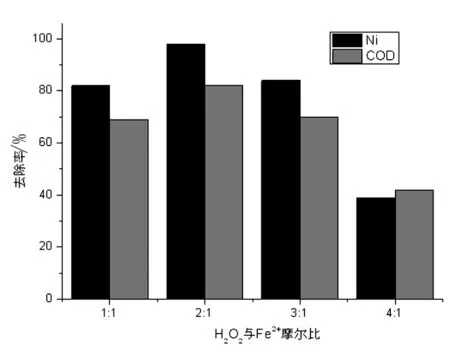
图3 H2O2与Fe2+摩尔比的影响

图4 反应时间的影响
由图3可知,H2O2与Fe2+物质的量比对镍离子和COD去除率的影响趋势一致,即随着H2O2与Fe2+物质的量比的增加,镍离子和COD去除率开始增加,然后再降低。在H2O2与Fe2+物质的量比为1∶1和2∶1时,镍离子和COD去除率有些许增加。在整个反应过程,·OH的数量会随着反应进行不断产生。Fe2+浓度较低时,H2O2很难分解产生·OH,反应速度变慢;而Fe2+过量时,·OH的产生很快,这样部分·OH会和·OH发生反应结合成H2O2,降低H2O2的利用率;同时过高的H2O2与Fe2+物质的量比将使得其中的Fe2+以捕收剂的方式与·OH结合,从而降低H2O2的利用率。
2.4 反应时间的影响
为了研究反应时间对芬顿氧化法处理化学镀镍废水的影响,不调节废水pH值,并保持H2O2的投加量为0.18 mol/L,H2O2与Fe2+物质的量比定为2∶1,反应时间1 h,考察四个反应时间的影响,结果如图4所示。
由图4可以看出,反应时间对镍离子和COD去除率的影响趋势一致,镍离子和COD的去除率随着反应时间的延长先升后降。反应时间到达1 h时,镍离子和COD去除率均达到最大值,继续延长反应时间,镍离子和COD去除率均出现下降,那是由于反应时间过长时,H2O2的挥发导致·OH的减少,从而影响氧化效率。后续实验中芬顿氧化的反应时间定为1 h。
3 结论
采用芬顿氧化法处理化学镀镍废水,考察了溶液初始pH值、H2O2投加量、H2O2/FeSO4物质的量比、反应时间四个影响因素对镍离子和COD处理效率的影响,得到以下结论:
(1)溶液初始pH值影响因素中,化学镀镍废水pH值为3时镍离子和COD处理效率均均达到最高,而该废水初始pH值为2.94,因此不需调节pH值。
(2)H2O2投加量影响因素中,当H2O2的投加量为0.18 mol/L时,镍离子去除率达99.20%,COD去除率达83.51%,此时残余镍离子浓度为1.45 mg/L,残余COD浓度为122.81 mg/L。
(3)H2O2/FeSO4物质的量比影响因素中,H2O2与Fe2+物质的量比确定为2∶1,此时镍离子和COD处理效率均达到最高。
(4)反应时间影响因素中,反应1 h时镍离子和COD处理效率均达到最高。

