Fe2O3/氮掺杂石墨烯复合材料的热分解动力学
马 妍 陈东梁 张东胜 何向向 杨 冉
(北京化工大学 机电工程学院, 北京 100029)
引 言
随着全球能源需求的不断增加,超级电容器以其比功率高、充放电速率快、效率高、循环寿命极长、环境污染少、价格较低等优点被广泛应用于航空、航天、通讯、信息及国防等领域。石墨烯自2004年被发现以来,因其具有良好的电学和力学性能、超高的比表面积,被广泛地应用于超级电容器等领域[1]。过渡金属氧化物(TMOs)高度稳定,其在表面和内部发生的法拉第电容非常大,理论比容量较高(~1 000 mA·h/g),且便宜、环保、易得,在超级电容器应用领域的研究十分深入和广泛[1-3]。石墨烯和TMOs的复合材料应用于超级电容器领域能够发挥各自的独特优势[4],因而得到了广泛关注。其中,将氮原子掺杂到石墨烯中能够显著提高石墨烯的电子结构和化学性质[5],因此氮掺杂石墨烯(NG)与TMOs的复合材料是超级电容器的研究重点之一。Lee等[6]通过水热法将α-Fe2O3与石墨烯进行复合,制备成超级电容器的材料。Sun等[7]通过一步水热法成功制备出Fe2O3/NG材料。陈家元[8]通过水热法制得Fe2O3/NG复合材料,经分析得出Fe2O3的存在促进了NG的热分解。
超级电容器应用于军事和航空航天领域时,要求复合材料具有耐高温性和超高的热稳定性。由于二十世纪五十年代航天技术的兴起,热重法在反应动力学中被用来研究材料的热稳定性和使用寿命[9]。热重(TG)是热解分析的重要研究手段之一[10],它能得到物质的质量损失和化学动力学参数,进而可以有效地分析出物质的热分解特性和反应机理。研究Fe2O3/NG的热分解动力学不仅可以分析其热稳定性,还可以为其以后在高温下的热化学应用提供数据基础。当前,研究者们在氮掺杂石墨烯/TMOs复合材料的制备和改性方面进行了较多研究,而关于其热分解动力学的研究较少。
本文通过水热法制备Fe2O3/NG复合材料并进行热重分析,使用Kissinger Akahira and Sunose(KAS)和Flynn- Wall- Ozawa(FWO)两种“model free”方法以及Coats- Redfern模型拟合法进行热动力学拟合,估算其活化能值与机理函数。
1 动力学分析方法
热分析动力学方法是直接检测体系某一物理性质变化的一种方法,可同时得到反应过程中相应物理性质变化的静态信息和动态动力学信息,通常用于非均相不等温反应。利用热分析动力学方法研究不定温条件下的非均相反应时,首先要对热解动力学进行如下假设[11]:
1)固体材料热解反应类型为
A(s)→B(s)+C(g)
2)炉内的气氛对热解反应没有任何的影响;
3)试样温度与炉内温度相同,不存在温度梯度;
4)Arrhenius方程可用于热分析反应
(1)
通常,非均相固体反应的动力学方程[12]为
(2)
式中,k(T)可由式(1)和(3)确定[12-13]。
(3)
结合公式(1)和(3)可得
(4)
升温速率β是一个常数,β=dT/dt,式(4)可写为
(5)
经过变换
(6)
式中,α为转化率,%;f(α)为反应机理函数;g(α)为转化率作用函数;T为绝对温度,K;T0为起始温度,K;k(T)为反应速数;m0为起始质量,g;mt为任意时刻质量,g;m∞为最终质量,g;Eα为表观活化能,kJ/mol;t为时间,s;A为指前因子;β为升温速率,K/min;R为通用气体常数,8.314 J/(K·mol)。
动力学研究的目的是求出“动力学三因子”,即Eα、A、f(α)。在不引入动力学模型函数的前提下得到比较可靠的动力学参数的方法称为“model free”法,Flynn- Wall- Ozawa(FWO)和Kissinger Akahira and Sunose(KAS)法是其中较常用的方法。
根据式(6),FWO方法表示为[14-16]
(7)
KAS方法表示为[17]
(8)
在进行动力学分析时,一般将实验数据与动力学模型函数相配合,用来判定某个模型函数能否用于描述这个反应,该法称为模型拟合法,Coats- Redfern(CR)是其中最常用的方法。
CR方法表示为[18]
(9)
2 实验部分
2.1 样品的制备
将0.15 g氧化石墨烯(GO,>90%,阿拉丁试剂有限公司)通过超声均匀分散于60 mL去离子水中,1.212 g的Fe(NO3)2·9H2O(>98%,国药集团化学试剂有限公司)加入GO水溶液中。15 mL氨水(28%,阿拉丁试剂有限公司)缓慢加入上述混合液中(氨水既是氮源[19-21],又是金属盐的沉淀剂[22]),随后转移到水热反应釜中,并保持180 ℃反应6 h。反应得到的溶液离心洗涤后80 ℃真空干燥过夜,制得Fe2O3/NG复合材料。氮掺杂石墨烯样品也通过同样的实验步骤制得。样品中Fe2O3的占比为72.36%。
2.2 样品的表征
采用德国Bruker公司的D8tools型X射线衍射仪(XRD)对样品进行物相分析,选取Cu Kα(λ=1.541 8 Å)射线,在5°~90°(2θ)范围内测量。
采用英国赛默飞世尔公司的ESCALAB 250Xi型X射线光电子能谱仪(XPS)表征样品的元素组成及相对含量。以Al靶1 486.6 eV的Kα射线为激光光源,以C1s的结合能(284.8 eV)进行峰位校准。
采用日本日立的S4800扫描电子显微镜(SEM)对样品的微观结构和表面形貌进行分析。
2.3 热重实验
采用德国Netzsch公司的STA449F5型热分析仪器进行TG分析,得到物质的质量损失和化学动力学参数。样品在氮气氛围下以50 mL/min的流率持续通入炉内,然后以5、10、15、20 K/min的升温速率线性升温到1 473.15 K。
3 结果与分析
3.1 表征分析结果
3.1.1XRD分析
图1为GO、NG和Fe2O3/NG的XRD图谱。氧化石墨烯在2θ=11.32°附近的特征衍射峰对应于(001)晶面。水热反应被还原后,氮掺杂石墨烯的衍射峰移动到2θ=25.45°附近,对应于(002)晶面。Fe2O3/NG具有典型斜方六面体结构的Fe2O3的衍射峰(PDF#00- 002- 0919),其位于2θ=24.3°、33.3°、35.8°、41.0°、49.5°、54.3°、57.6°、62.8°和64.2°的衍射峰分别对应于(012)、(104)、(110)、(113)、(024)、(116)、(122)、(214)和(300)晶面。对比3种材料的XRD图谱可以得出,GO的含氧基团在水热反应过程中大部分被还原移除,并成功形成了Fe2O3。
3.1.2XPS分析
X射线光电子能谱是一种表面检测技术,可定性定量地分析材料表面化学元素组成,Fe2O3/NG的元素分析结果如表1所示,其中氮的含量为5.214%。Fe2O3/NG的XPS图谱如图2所示。

表1 各元素的相对物质的量分数Table 1 Relative molar contents of different elements

3.1.3SEM分析
Fe2O3/NG的SEM图片如图3所示。从SEM图中可以看出Fe2O3纳米颗粒呈现出较为规则的球形,锚定在起伏的二维结构的石墨烯表面,且分散均匀。
3.2 Fe2O3/NG的热解过程
图4为Fe2O3/NG在5、10、15、20 K/min升温速率下的热分解过程,可以看出Fe2O3/NG在1 153 K左右发生较为明显的失重。
不同升温速率下,Fe2O3/NG的DTG曲线如图5所示,相关分解参数如表2所示。不同升温速率下失重速率的峰值在1 156~1 194 K的温度范围内出现,出现峰值的温度分别为1 156.85、1 175.75、1 186.85 K和1 194.05 K。随着升温速率的提高,峰值温度增大。这是因为升温速率越高,达到热解终温的时间越短,反应进行的程度越差,导致达到最大热解速率的温度后移。热分解过程从1 100 K左右开始质量急剧损失,直至1 373 K。各个升温速率下的平均残余质量分数为49.92%,升温速率对残余质量的影响不大。总失重的90%在1 173~1 203 K范围内,说明Fe2O3/NG具有很高的热稳定性。
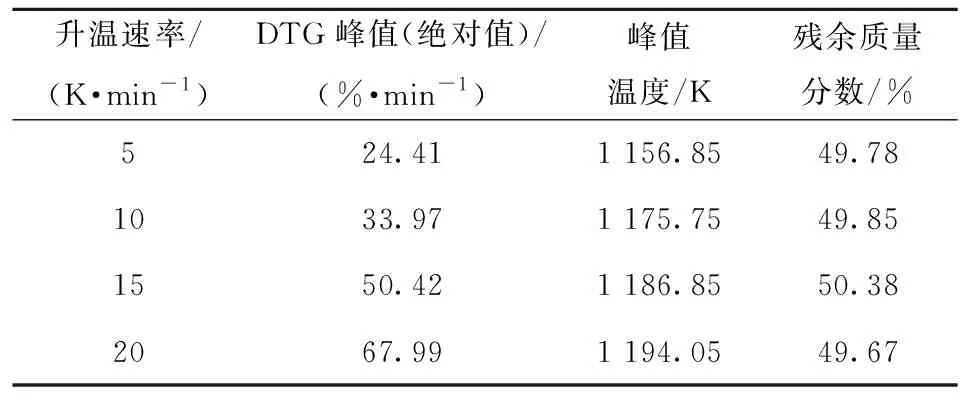
表2 Fe2O3/NG的热分解参数Table 2 Pyrolysis parameters of Fe2O3/NG
3.3 “model free”法估算表观活化能
基于KAS和FWO方法,选取失重峰范围(1 000~1 400 K)内转化率为0.25~0.80,ln(β/T2)与1/T及lnβ与1/T的拟合曲线如图6、7所示。两种方法拟合的曲线是近似平行的,说明在不同转化率下表观活化能近似相同。表观活化能和指前因子可以根据不同转化率的曲线斜率估算得出(KAS法的斜率为Eα/R,FWO法的斜率为1.052Eα/R),具体数值见表3。FWO法和KAS法估算的表观活化能变化范围分别为404.08~424.65 kJ/mol和405.52~427.10 kJ/mol,平均值分别为410.92 kJ/mol和412.74 kJ/mol,相差0.4%。

表3 FWO和KAS方法估算的表观活化能(Eα)和指前因子(A)Table 3 Estimated thermal degradation activation energies(Eα) and pre-exponential factors(A)using the FWO and KAS methods
表观活化能代表反应发生所需要的能量,活化能越大代表反应越不易发生。FWO法和KAS法估算得到的表观活化能与转化率之间的关系如图8所示,表观活化能随着转化率的增大而增加,原因可能是随着分解反应的进行,转化率提高,一些挥发分析出后,反应继续进行下去的难度增加,因而表观活化能增大。表观活化能与转化率之间的关系可表示为
FWO方法Eα=402.782+0.594e4.452α
KAS方法Eα=404.043+0.668e4.374α
3.4 模型拟合方法估算表观活化能
常用的固态热解反应动力学机理函数主要有反应级数模型、扩散机理模型、相界面模型和随机成核模型等[12],具体见表4。
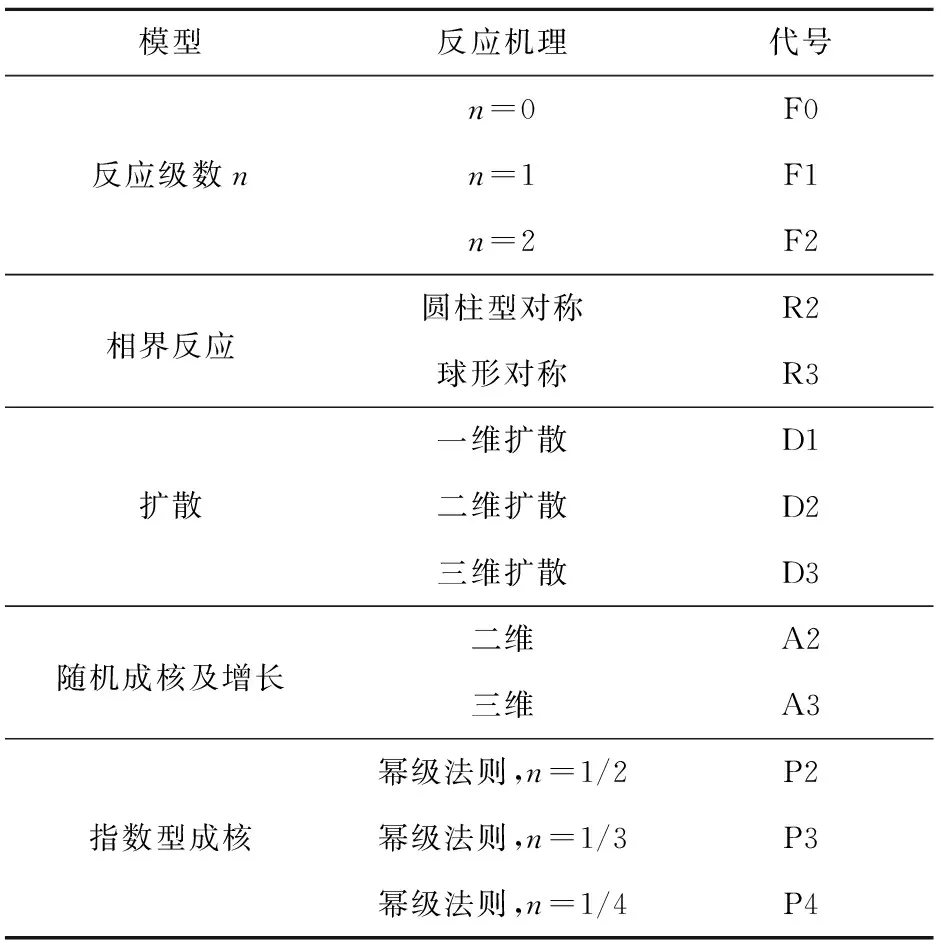
表4 常用的固态热解反应动力学机理函数Table 4 Commonly used solid-state pyrolysis reaction kinetic mechanism functions
表5是用CR方法估算出的表观活化能数据。由于升温速率对模型拟合的方法影响较小,因此本文只对升温速率5 K/min下的热重曲线进行拟合。由表5可以看出,模型不同,估算出的表观活化能值相差较大。Mample Power(P3)估算的表观活化能值与KAS和FWO方法估算得到的表观活化能值最接近,其他模型估算得到的表观活化能值相差较大,不足以很好地描述其动力学行为,因此Mample Power(P3)模型函数是最能反映Fe2O3/NG分解的机理函数,即f(α)=3α2/3,其估算的表观活化能Eα=408.06 kJ/mol,指前因子lnA=33.65。Fe2O3/NG分解反应的反应机理为随机成核和随后生长,且呈指数型成核(n=1/3),反应机理表达式为
dα/dT=(4.11×1014/β)e-4.08×105/RT×3α2/3

表5 CR法估算的活化能值Table 5 Eα values obtained by CR methods
4 结论
(1)FWO法和KAS法估算的表观活化能变化范围分别为404.08~424.65 kJ/mol和405.52~427.10 kJ/mol,且表观活化能随着转化率的增大而增加,平均值分别为410.92 kJ/mol和412.74 kJ/mol,相差0.4%,说明Fe2O3/NG具有高的热稳定性。FWO和KAS法估算得到的表观活化能与转化率之间存在着指数关系,表达式分别为Eα=402.782+0.594e4.452α,Eα=404.043+0.668e4.374α。
(2)与KAS和FWO方法估算得到的表观活化能值相比较,Mample Power(P3)法则是最能反映Fe2O3/NG分解的机理函数,其估算的表观活化能Eα=408.06 kJ/mol,指前因子lnA=33.65。Fe2O3/NG分解反应的反应机理为随机成核和随后生长,且呈指数型成核(n=1/3),反应机理表达式为dα/dT=(4.11×1014/β)e-4.08×105/RT×3α2/3。

