“环丙-林可霉素长效注射液”毒理学试验研究
叶兆伟 , 吴海港 , 李尽哲 , 刘锦妮 *, 姬万民
(1.信阳农林学院生物与制药工程学院,河南信阳 464000;2.信阳市兽药新制剂研究与创制工程技术研究中心,河南信阳 464000;3.瑞普(天津)生物科技股份有限公司,天津空港经济区 300308)
环丙沙星和盐酸林可霉素是兽医临床中使用较为广泛的抗生素之一,其主要用于畜禽相关细菌感染性疾病的预防与治疗(孙建宁,2016;国家药典委员会,2015)。体外联合药敏试验结果显示,环丙沙星与盐酸林可霉素具有协同抗菌作用(吴海港等,2015;刘安述等,2012),但由于二者普通制剂在体内半衰期短,单次使用剂量较大,需要连续多次给药才能在体内保持有效血药浓度,容易引起药物的顺从性差(高艳等,2014;范惠敏等,2012)。因此根据环丙沙星和盐酸林可霉素联合抗菌活性和临床应用需要研制出环丙-林可霉素长效注射液,为了科学、客观地评价“环丙-林可霉素长效注射液”的安全性,依据《新兽药注册管理办法》及相关法律法规的要求(中华人民共和国卫生部药政管理局,1993),本试验对环丙-林可霉素长效注射液进行急性毒性试验、局部刺激性试验和亚慢毒性试验,以期为临床用药提供参考。
1 材料与方法
1.1 试验材料
1.1.1 药物及试剂 环丙沙星、林可霉素原料购于河南自然康生物科技有限公司,环丙-林可霉素长效注射液制备参考吴海港等(2015)的方法,生理盐水与脱毛剂为本实验室自制。
1.1.2 试验动物 小鼠80只、健康成年白色家兔30只,均由郑州大学实验动物中心提供,合格证号 SCXK(豫)2017-0001。
1.1.3 主要仪器 A0820石蜡切片机 (Amershanm optical公司);BHP生物显微镜 (奥林巴斯(中国)有限公司)。
1.2 试验步骤
1.2.1 急性毒性试验 预试验:选用1月龄小鼠20只,雌、雄各半,随机分成5组,每组4只,常规饲养。于试验开始第1天分别按照10、7.5、5、2.5、1 mg/kg肌肉注射给药,记录小鼠的急性毒性反应及死亡情况,包括中毒症状出现的时间、死亡时间、精神、饮食、体重变化及肝脏、肾脏器官的变化。在用药后第6天将所有试验小鼠颈椎脱位处死,剖检观察其对小鼠肝脏、脾脏、肾脏及肺脏等脏器的病理变化。
正式试验:在室温条件下,取禁食12 h的小鼠共50只,雌雄各半,随机将小鼠分为5组,每组10只。各组动物均以肌肉注射给药。根据预试验的结果确定的最高剂量组为7.5 mg/kg,其余组间剂量为1:0.8,观察7 d,常规饲养,记录各组动物用药后所表现的临床症状、体征、死亡数和时间,采用改良寇氏法确定环丙-林可霉素长效注射液的半数致死量(LD50)。
1.2.2 溶血试验 按照环丙-林可霉素长效注射液临床使用浓度(0.2 mg/kg),用生理盐水按 1:5稀释,将稀释后药液按照表1进行试验,将各管置于37℃水浴中保温,开始每15 min观察试验现象1次,试验1 h以后采用每1 h观察试验现象1次,连续观察4 h,参考中国食品药品监督管理局(2005)对试验结果进行判断。
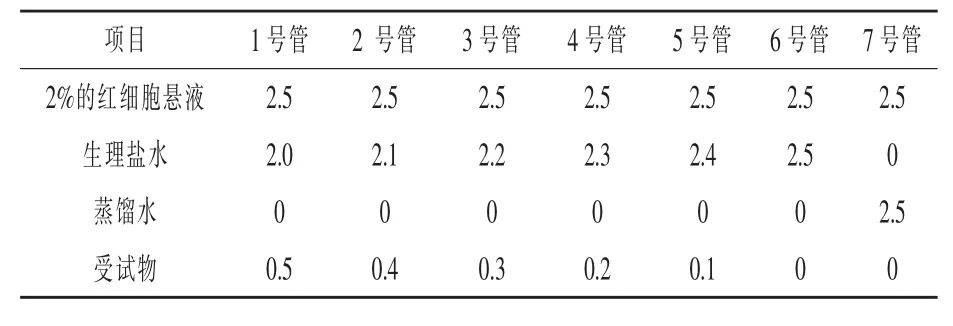
表1 溶血试验加样培育mL
1.2.3 肌肉刺激性试验 参考国家食品药品监督管理局(2005)方法,取健康家兔8只,雌雄各半,将家兔固定于固定箱内,分别于一侧股四头肌内注射环丙-林可霉素长效注射液1 mL。并以生理盐水为对照药物,于另一侧相同部位同法注射给药,观察用药部位肌肉的变化情况(如充血等)。给药48 h后将试验动物处死,纵向切开股四头肌,观察用药部位肌肉的刺激反应。
1.2.4 皮肤刺激试验 参考袁伯俊等 (1997)方法,取健康家兔8只,雌雄各半,体重(2.5士0.5)kg。分笼单独饲养,于给药前24 h沿脊椎两侧相对应部位脱毛,左侧按照0.5 mL/次涂抹环丙-林可霉素长效注射,右侧相对应部位按照相同剂量涂空白基质为对照,采用无刺激纱布固定。涂抹24 h后温水冲洗擦拭,分别于不同时间内观察涂抹部位皮肤变化情况。
1.2.5 亚慢性毒性试验 参考徐叔云等 (2002)方法,选用健康、体重(2.5士0.5)kg的家兔24只,雌雄各半,随机分成4组,分笼常规饲养。根据急性毒性试验结果,环丙-林可霉素长效注射液设高剂量组(1 mg/kg)、中剂量组(0.5 mg/kg)、治疗剂量组(0.2 mg/kg)和对照组(生理盐水)。肌肉注射给药,每天注射1次,连续注射14 d。每天观察家兔健康状况,包括活动、采食、饮水、发病和死亡等;于第15天称重,并对肝脏、肾脏进行组织病理学检查。
2 试验结果
2.1 急性毒性试验 高剂量组(7.5 mg/kg)表现为给药后小鼠出现精神兴奋,呼吸加快,1 min后开始摇晃,伴有共济失调,肌肉抽搐呈划水样,2 min后死亡。剖检可见肝脏颜色呈深褐色,其他器官未有明显的眼观变化。低剂量组(3.0 mg/kg)小鼠6 d后处死,剖检其肝脏、肾脏未有异常。各组小鼠死亡情况见表2,应用改良寇氏法计算LD50=4.81 mg/kg,LD50的95%可信限为4.50~5.53 mg/kg。
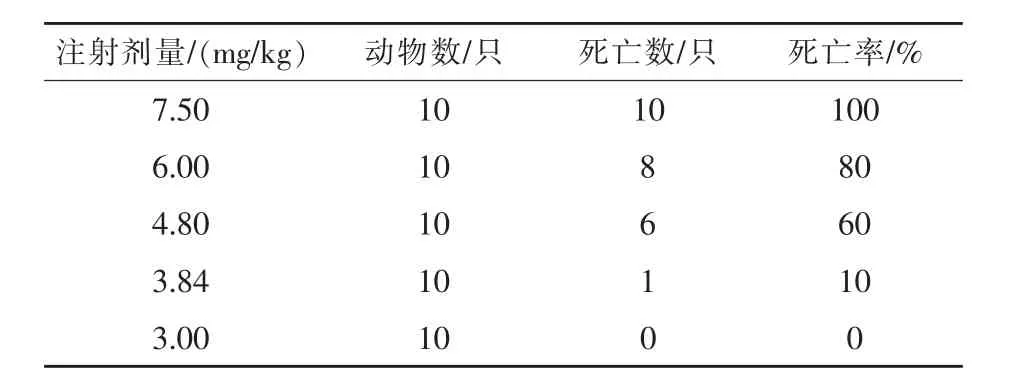
表2 环丙-林可霉素长效注射液对小鼠急性毒性试验结果
2.2 溶血试验 在观察时间内,3~6号管未见溶血和红细胞凝聚现象,第7管溶液呈红色透明,有溶血现象。结果表明环丙-林可霉素长效注射液0.1~0.3 mL在4 h内对红细胞不产生溶血和凝聚作用。
2.3 肌肉刺激性试验 给药后各家兔健康如常,其对肌肉刺激性试验结果见表3。从结果中可以看出环丙-林可霉素长效注射液具有轻度的肌肉刺激反应,其范围在0.5 cm×1.0 cm以下,肌肉刺激性反应级的最高与最低之差等于0,家兔肌肉刺激性反应之和小于10,表明环丙-林可霉素注射液的局部刺激试验符合规定。
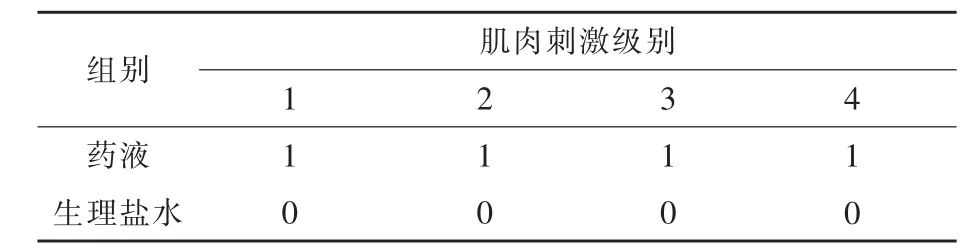
表3 肌肉刺激性反应分级结果
2.4 皮肤刺激试验 由表4可知,环丙-林可霉素长效注射液在涂抹后未对家兔皮肤产生刺激作用,表明环丙-林可霉素注射液的皮肤刺激性试验符合规定。
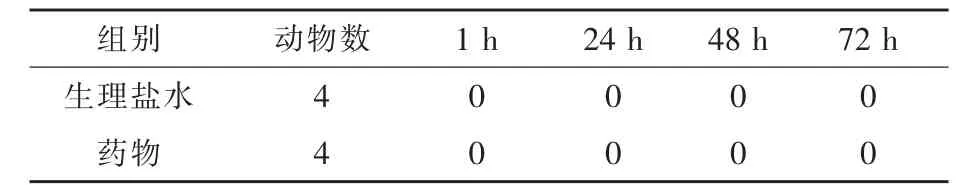
表4 皮肤刺激性的评价
2.5 亚慢性毒性试验
2.5.1 体重变化 正常治疗剂量组与中剂量组家兔的体重基本变化不大,与对照组比较,差异不显著。高剂量组体重增长低于对照组和临床剂量组,并表现出精神不振、呆立或卧地不起、食欲减少等症状,表明高浓度药物对家兔体重有一定的影响。
2.5.2 肝脏、肾脏组织形态学 肉眼观察家兔的肾脏未见明显病理学变化,肝脏稍有肿大,周围颜色较深。通过组织切片观察,治疗剂量组肾小球形态完整,无出血;中剂量组肾小球内有散在的出血,胞浆出现液化,肾小管形态正常;高剂量组肾小球内有大量出血,,肾间质出现坏死,散在血细胞、管上皮正常形态消失。常规剂量组肝索有序,肝血窦未见出血、坏死;中剂量组家兔肝脏主要表现为肝血窦、中央静脉有出血,肝细胞间隙增大;高剂量肝细胞排列紊乱,肝细胞肿胀融合,肝血窦间有大量出血和炎性细胞。
3 讨论
急性毒性试验是药物及制剂安全性评价的重要内容,是评价受试化学物急性毒性大小的主要参数,可以根据半数致死量(LD50)的结果判断该药物的毒性大小及其作用靶器官。为亚急性、慢性毒性试验设计提供资料(楼宜嘉,2011)。通常LD50值越小,化合物的毒性就越大,对靶动物和人产生危害的可能性也就越大 (沈建忠,2011)。研究表明,环丙沙星LD50小鼠口服为>5000 mg/kg,大鼠为>2000 mg/kg;小鼠及大鼠皮下注射均>1000 mg/kg(刘明亮,2012)。 贾海艳等(2010)报道,庆大霉素和林可霉素注射液对小鼠肌肉注射的LD50为4.989 mL/kg。本研究结果显示,环丙-林可霉素长效注射液小鼠静脉注射LD50为 4.81 mg/kg,LD50的95%可信限为4.50~5.53 mg/kg,表明药物的急性毒性与药物制剂、药物辅料以及联合使用药有关,尤其是联合用药,其提高治疗作用同时也增加了药物的毒副作用。
体外红细胞溶血性、局部刺激性及过敏性等是药物安全性评价的重要指标(冯小花,2007)。漆俊等(2012)以乳酸环丙沙星和乳酸甲氧苄定研制出了复方环丙沙星乳剂。该制剂对家兔肌肉注射给药不产生热源反应,无体外溶血性或凝集反应,不产生明显的肌肉刺激性反应,也不产生明显全身过敏性反应;万军梅等(2013)对复方环丙沙星烧伤凝胶毒理学进行研究表明,该制剂无明显急性毒性和致敏作用,未见其对家兔完整皮肤和破损皮肤有明显刺激作用。本试验结果表明,环丙-林可霉素长效注射液无明显刺激性,对试验动物无致敏性,无体外溶血性,提示庆大霉素和林可霉素注射液肌内注射给药符合安全性要求。
脏器是机体发挥生理功能的场所,其形态结构改变将直接影响机体的正常功能,因此病理学检查是评价药物毒性及安全性的直接指标 (邢守叶等,2015)。林晓辉(2015)报道,高剂量使用环丙沙星后大鼠血浆中,异染粒有增加的趋势,在其尿液中出现了黄色针状的结晶。贾海艳(2010)研究表明,高剂量使用复方林可霉素注射液对肾脏存在一定的毒性,对肝脏功能的影响较小。而本试验结果表明,环丙-林可霉素长效注射液治疗剂量和中剂量组肝脏和肾脏组织结构清晰,而高剂量组肾小球内有大量出血,肾间质出现坏死,肝细胞排列紊乱,肝细胞肿胀融合,肝血窦间有大量出血。从细胞形态观察可以说明环丙-林可霉素长效注射液有一定的毒性作用,但作用机制有待进一步研究。

