HPLC 法同时测定鱼腥草中4 种黄酮苷的含量*
廖卫波 王亚敏 戴迪 虞金宝 李晶
(江西省中医药研究院 南昌330046)
鱼腥草为三白草科蕺菜属植物蕺菜(Houttuynia Cordata Thunb)的全草。在我国分布广泛,中部、东南至西南部等地区均较为常见,常生于路旁、沟边、溪边及林下湿地,具有清热解毒、消肿排脓、利尿通淋之功效,应用广泛,并且在我国西南地区人们多有种植并将其嫩根茎作为蔬菜或调味品,是一种重要的收入药食同源全目录名单的植物资源[1]。学者对鱼腥草含量测定及药理方面亦有诸多研究[2~4],现代药理研究表明鱼腥草具有抗肿瘤、增强机体免疫力和抗氧化等作用,有效物质为黄酮类成分[5~7]。国内外对于鱼腥草中挥发油成分的研究较多,但以黄酮类为药效物质基础的相关产品专利较为少见,并且在《中国药典》2015 年版中也未明确相关黄酮类药效成分的含量测定指标。本研究采用高效液相色谱法(HPLC),建立了同时测定鱼腥草中4 种黄酮苷(芸香苷、金丝桃苷、异槲皮苷及槲皮苷)含量的测定方法,以期为鱼腥草药材中黄酮苷类成分的含量测定及质量控制提供一定的参考。现报道如下:
1 仪器与材料
1.1 仪器 岛津LC-20AD 高效液相色谱仪(LC-20AD 泵、SIL-10ADVP 控制器、SPD-20A 紫外检测器、CTO-10ASVP 柱温箱,购于日本岛津公司);ml-T 型万分之一分析天平、XPR 型十万分之一分析天平(METTLER TOLEDO 公司);KQ-250DB型数控超声波清洗器(昆山市超声仪器有限公司)。
1.2 材料 鱼腥草药材购于樟树市中药材市场;芸香苷(批号:100080-201610)、金丝桃苷(批号:111521-201708)、槲皮苷(批号:111538-201606)、异槲皮苷(批号:111809-201403),均购于中国食品药品检定研究院;乙腈(色谱级);甲醇(分析纯);磷酸(分析纯);娃哈哈纯净水。
2 方法与结果
2.1 色谱条件 色谱柱:迪马DiamonsilTMC18(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.1%磷酸(H3PO4)水溶液(B),按表 1 进行梯度洗脱;检测波长:254 nm;柱温:30 ℃;流速:1.0 ml/min;进样量:10 μl。

表1 梯度洗脱条件
2.2 供试品溶液的制备 称取鱼腥草药材粉末(过60 目筛)2 g,精密称定,置于 100 ml 锥形瓶中,加入90%甲醇溶液90 ml,记录所称定重量,浸渍过夜(8 h)后以超声仪超声提取,超声功率为100 w,频率为40 kHz,超声提取时间1 h,冷却后用90%的甲醇溶液补足失重,过滤,续滤液用孔径0.22 μm 的微孔滤膜过滤,备用。
2.3 对照品溶液的制备
2.3.1 对照品母液的制备 分别精密称取芸香苷、金丝桃苷、异槲皮苷及槲皮苷4 种对照品10.52 mg、10.33 mg、8.79 mg 和 9.52 mg,分别置于 10 ml容量瓶中,分别加90%甲醇溶液使溶解并定容至刻度,即配制成浓度为 1.052 mg/ml、1.033 mg/ml、0.879 mg/ml 和0.952 mg/ml 的对照品母液,备用。
2.3.2 混合对照品的制备 分别精密吸取芸香苷、金丝桃苷、异槲皮苷及槲皮苷4 种对照品母液0.2 ml、0.6 ml、0.4 ml 和 1.0 ml 同时置于 10 ml 容量瓶中,加入90%的甲醇溶液定容至刻度,摇匀,即配制成 浓 度 分 别 为 21.04 μg/ml、61.98 μg/ml、35.16 μg/ml 和95.20 μg/ml 的混合对照品溶液,以孔径0.22 μm 微孔滤膜过滤,备用。
2.4 分离度 精密吸取混合对照品、鱼腥草供试品溶液适量,按“2.1”色谱条件下进样测定分析,由图可见,各成分与相邻色谱峰均能达到有效分离,目标峰分离度均>1.5 且各峰理论塔板数均>3 500。见图1。

图1 混合对照品(A)及鱼腥草供试品(B)HPLC 色谱图
2.5 线性关系考察 吸取“2.3.2”所制混合对照品溶液,按“2.1”色谱条件分别进样,进样量分别为2 μl、5 μl、8 μl、10 μl、12 μl、15 μl、20 μl,以样品质量(μg)为横坐标,以峰面积积分值为纵坐标分别计算及绘制芸香苷、金丝桃苷、异槲皮苷及槲皮苷4 种黄酮苷的标准曲线及其相应的线性范围,结果显示,芸香苷、金丝桃苷、异槲皮苷及槲皮苷的相关系数r 分别为 0.999 8、0.999 7、0.999 8 和 0.999 6,表明 4 种黄酮苷在各自相应线性范围内的线性关系良好。见表2。

表2 4 种黄酮苷成分线性范围
2.6 精密度试验 吸取“2.3.2”所制混合对照品溶液,以孔径 0.22 μm 微孔滤膜滤过,按“2.1”色谱条件连续进样6 次,进样量为10 μl,分别记录芸香苷、金丝桃苷、异槲皮苷及槲皮苷相应峰面积并计算相应的 RSD 值,RSD 值依次为 0.34%、0.30%、0.83%及0.52%,均<2.00%,试验表明仪器的精密度良好。
2.7 稳定性试验 取同一供试品溶液,室温条件下放置,并分别于 0、2、4、8、12、16、24 h 按“2.1”色谱条件进样,进样量为10 μl,记录芸香苷、金丝桃苷、异槲皮苷及槲皮苷各色谱峰的峰面积,并计算4 种黄酮苷24 h 内各自相应峰面积的RSD 值,RSD 值依次为0.73%、0.42%、0.75%和0.68%(均<2.00%),表明鱼腥草供试品溶液在24 h 内稳定性良好。
2.8 重复性试验 取同一批次的鱼腥草粉末6 份,按“2.2”方法制备鱼腥草供试品溶液,并按“2.1”色谱条件方法对其进行测定分析,进样量为10 μl,记录芸香苷、金丝桃苷、异槲皮苷及槲皮苷各色谱峰的峰面积,并计算4 种黄酮苷各自相应含量的RSD 值,RSD 值依次为0.96%、1.05%、0.87%和 1.12%(均<2.00%),表明该方法重复性良好。
2.9 回收率试验 取同一批次鱼腥草粉末9 份(约1 g),精密称定,加入低、中、高三个不同质量浓度的混合对照品溶液,每个浓度三份,按“2.2”方法制备成供试品溶液,并按“2.1”色谱条件方法对其进行测定分析,进样量为10 μl,记录各色谱峰峰面积,计算回收率。结果显示,芸香苷、金丝桃苷、异槲皮苷及槲皮苷加样回收率在95.16%~102.14%范围内,RSD值均<2.00%,表明该方法良好,准确度符合要求。见表3。
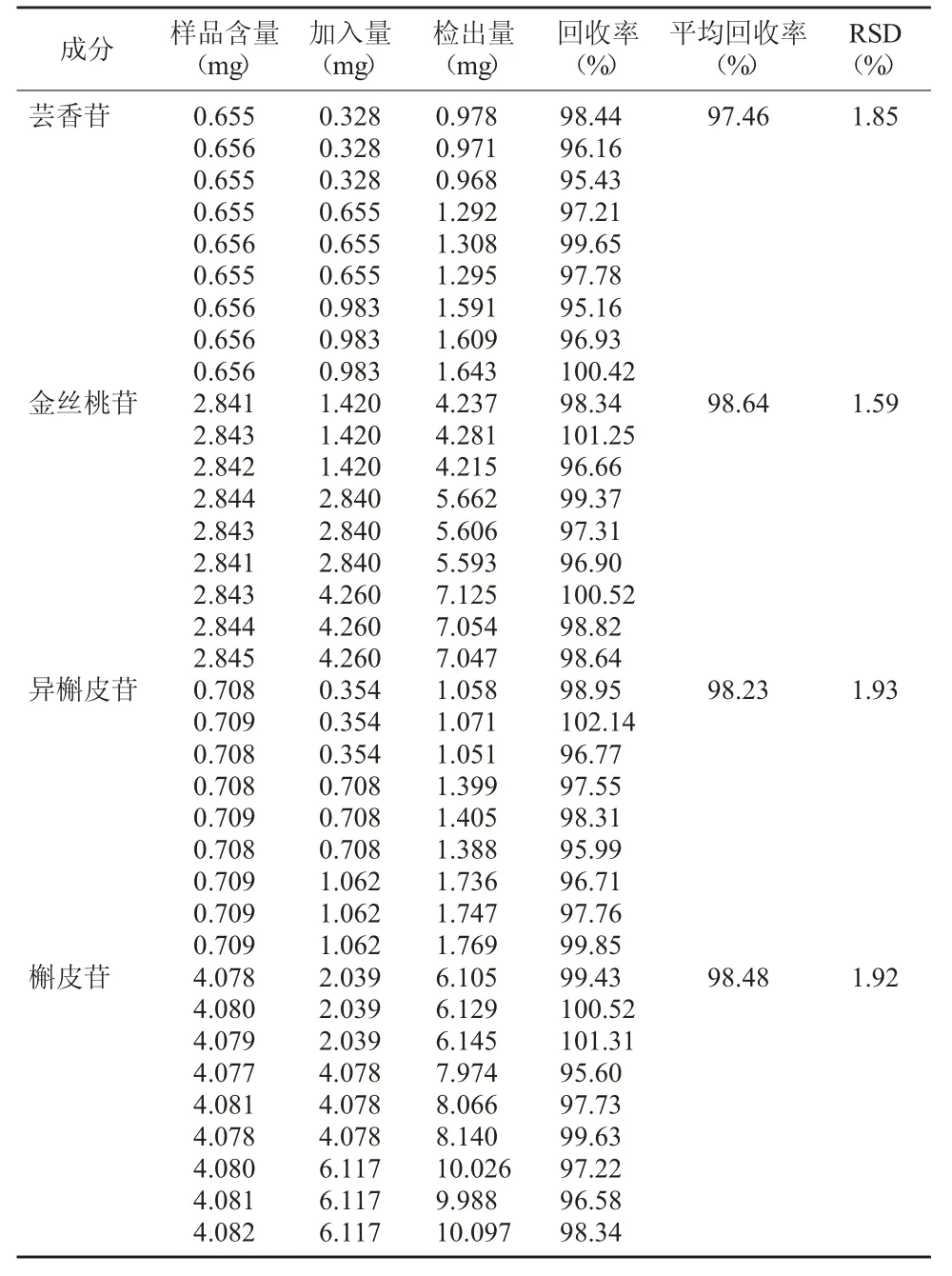
表3 回收率试验结果
2.10 样品含量测定 取不同批次鱼腥草粉末各2 g,精密称定,按“2.2”项下方法制备成供试品溶液,并按“2.1”项下色谱条件方法测定分析,进样量为10 μl,记录芸香苷、金丝桃苷、异槲皮苷及槲皮苷的色谱峰面积,计算4 种黄酮苷各自相应的含量。结果显示,三批样品中4 种黄酮苷芸香苷、金丝桃苷、异槲皮苷及槲皮苷的含量存在一定的差异,芸香苷、金丝桃苷、异槲皮苷及槲皮苷的平均含量分别为0.70 mg/g、2.97 mg/g、0.68 mg/g 和 4.44 mg/g,总含量约占8.80 mg/g。金丝桃苷和槲皮苷的含量较高,仅二者即占总含量的7.41 mg/g。见表4。
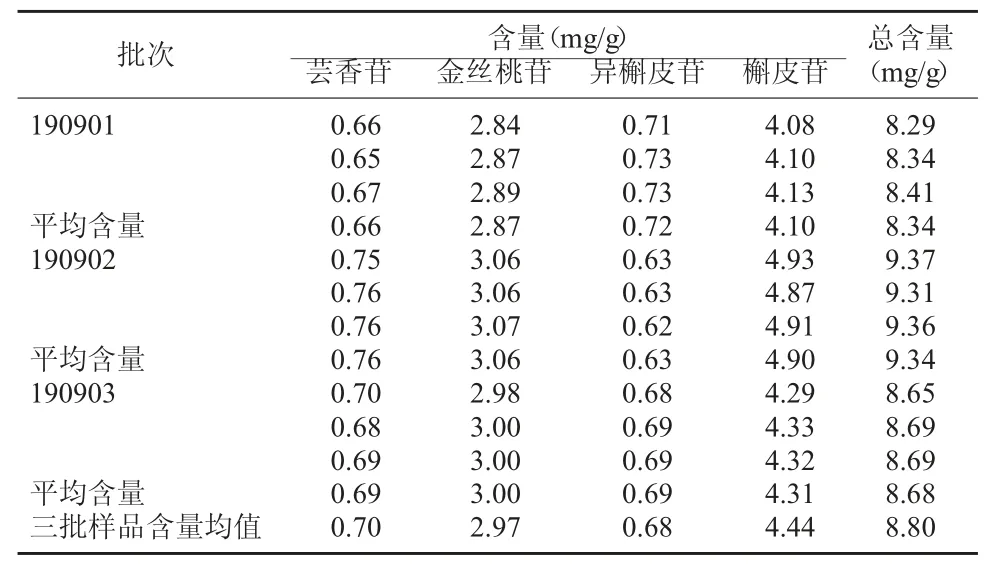
表4 样品含量测定
3 讨论
鱼腥草作为重要的药食同源植物,其药用价值应用广泛,单一指标的质量评价对其质量控制存在一定的不足,不能很好反映药材质量的优劣。黄酮类成分作为鱼腥草有效物质,其含量测定尤为重要[8~9],本研究以HPLC 法建立了同时测定4 种黄酮苷含量的方法,为其质量评价提供了一定参考。
鱼腥草中芸香苷、金丝桃苷、异槲皮苷、槲皮苷4 种成分均属于黄酮苷类化合物,易溶于水及甲醇等较强极性的溶剂中,本研究前期分别选择(50%、75%、90%)甲醇、纯甲醇、(50%、75%、90%)乙醇及水等多种不同溶剂作为提取溶剂,探究优选最佳提取溶剂,结果表明,以90%的甲醇作为提取溶剂时4种目标产物均能达到较完全的提取效果,且杂质干扰较少。本研究中针对金丝桃苷与异槲皮苷分离度不佳及峰拖尾等问题,采用梯度洗脱,以乙腈-0.1%H3PO4为流动相,并适当延迟出峰时间的方式,最终获得了较好的分离效果。
此外,本研究的方法学考察结果显示,该方法操作简便,具有较高的准确度,灵敏度及稳定性。通过测定鱼腥草中芸香苷、金丝桃苷、异槲皮苷、槲皮苷4 种黄酮苷成分的含量,能提高鱼腥草药材在质量控制方面的准确性及可控性,对其应用及开发有重要的意义。

