选择性5-羟色胺再摄取抑制剂治疗癫痫合并抑郁症效果的meta分析
邢航,路承彪,韩雄
(1.河南省人民医院/郑州大学人民医院 神经内科,河南 郑州 450000;2.新乡医学院 生理学与神经生物学教研室,河南 新乡 453003)
癫痫是神经系统疾病的常见病之一,其发病机制尚不清楚,目前比较一致的观点是中枢神经系统兴奋与抑制性不平衡所致。癫痫的临床特点以反复发作为主,严重影响患者的身心健康。抑郁症是癫痫最常见的共患病,流行病学调查显示癫痫患者共患抑郁症的发生率为8%~48%,比普通人群高5~20倍[1-2]。癫痫合并抑郁症的抑郁、焦虑、认知功能障碍和睡眠障碍症状与单纯的癫痫发作相比,前者对患者生活质量的影响更明显[3]。自杀行为及自杀观念可增加患者癫痫发作的风险[4],同时抑郁可导致抗癫痫药物的不良反应和耐药性增加[5]。一方面,癫痫频繁发作往往容易掩盖患者的情绪反应,导致临床治疗多侧重于控制癫痫发作而忽略合并的抑郁症的识别与治疗;另一方面,临床医生担心抗抑郁药物可能增加癫痫发作恶化的风险。因此,早期识别癫痫患者合并抑郁,选择恰当的抗抑郁药物十分重要。选择性5-羟色胺再摄取抑制剂(selective serotonin reuptake inhibitors,SSRIs)是治疗抑郁症的一线常用药物,通过抑制突触再摄取泵对神经递质5-羟色胺的再摄取以提高突触间隙中5-羟色胺水平,从而达到抗抑郁的治疗效果。一些临床随机对照试验表明,SSRIs对癫痫合并抑郁具有显著疗效,同时不增加癫痫发作,但这些研究使用的SSRIs结构不同,并且存在单中心、小样本等局限性[6]。为客观评价SSRIs治疗癫痫合并抑郁症的效果,本研究采用Cochrane系统评价方法对所纳入的随机对照试验进行全面评价,将多个独立的临床研究综合起来进行定量统计分析,通过真实、可靠的结论为临床治疗癫痫合并抑郁症提供依据。
1 资料与方法
1.1 研究类型研究已发表的SSRIs,包括氟西汀、帕罗西汀、舍曲林、西酞普兰等治疗癫痫合并抑郁症的随机对照试验,文献语种限定为英文和中文。
1.2 选取标准纳入标准:(1)年龄小于18岁;(2)男女不限,根据临床症状、神经系统检查、脑电图和头部CT检查确诊为癫痫,包括任何类型的癫痫发作;(3)符合DSM-5、ICD-10或CCMD-3对抑郁症的诊断。排除标准:(1)先天性神经功能发育不全;(2)重要器官如心、肝、肾功能和血液系统等异常。
1.3 干预措施与结局指标抗癫痫药物(antiepileptic drugs,AEDs)组接受抗癫痫药物单药或联合治疗,SSRIs+AEDs组在原抗癫痫药基础上加用SSRIs。各组均为口服给药,且经过剂量调整期,直到最佳有效剂量。(1)主要结局指标:对抑郁症的疗效,采用汉密尔顿抑郁量表(Hamilton depression scale,HAMD)及达到HAMD评分有效减分率的比例评估治疗抑郁症的效果,有效减分率为>25%,若减分率≤25%评定为无效。(2)次要结局指标:对伴发焦虑症的疗效,采用汉密尔顿焦虑量表(Hamilton anxiety scale,HAMA)评估治疗焦虑症的效果。(3)以控制癫痫发作频率及达到有效控制癫痫发作频率的比例评估治疗癫痫的效果:有效为控制癫痫发作频率降低50%以上;若发作频率降低在50%以下评定为无效。(4)不良反应发生率。
1.4 文献检索
1.4.1数据库 PubMed、EMbase、Cochrane图书馆、维普中文期刊数据库(VIP)、 万方数据库、中国生物医学文献数据库(CBM)和中国期刊全文数据库(CNKI),收集SSRIs治疗癫痫合并抑郁症的随机对照试验,检索时限均为从建库至2020年2月。
1.4.2检索策略 采用主题词、关键词检索,并结合文献追溯、手工检索等。英文检索词:epilepsy、depression、fluoxetine、paroxetine、sertraline、escitalopram、citalopram、fluvoxamine、volazodone、vortioxetine和clinical trails。中文检索词:癫痫、抑郁、氟西汀、帕罗西汀、舍曲林、西酞普兰、依他普仑、氟伏沙明、维拉唑酮、伏替西汀和临床研究。
1.5 文献的筛选由两位研究者独立阅读所获文献题目和摘要,按照纳入标准排除不符合的试验,并交叉核对,如有分歧,讨论决定是否纳入。
1.6 数据提取与文献质量评价采用Cochrane手册5版RCT偏倚风险评估工具[7],由两位研究者对纳入文献的方法学进行独立质量评价,并交叉核对。若有分歧,由第3位研究者协商解决。评价内容包括:随机(序列产生和分配隐藏)、实施(包括对研究者和受试者施盲)、测量(研究结局盲法评价)、随访(结局数据的完整性)、报告(选择性报告研究结果)及其他(其他偏倚来源)。以上评价标准在Cochrane手册中有详细描述,根据评价标准可以评价为 “低风险偏移(low risk of bias)”或“高风险偏移(high risk of bias)”或“不清楚(unclear risk of bias)”。
1.7 统计学分析采用RevMan 5.3统计软件进行分析。如果监测指标为计数资料,采用比值比(odds ratio,OR)及其95%置信区间(95% CI)作为效应量。如果监测指标为计量资料,采用均数差(mean difference,MD)及其95% CI统计效应量。通过分析纳入研究的临床异质性,检验各个独立研究的结果是否具有一致性。按照临床异质性和方法学进行亚组分析,采用χ2检验分析各研究结果间的统计学异质性,如果各独立研究的结果是同质的(P≥0.01),采用固定效应模式分析,计算合并后的综合效应,如果各研究结果不同质(P<0.01),采用随机效应模型分析,计算合并后的统计量。
2 结果
2.1 文献检索结果初检到相关文献1 416篇文献。根据纳入标准,阅读文题和摘要排除非随机对照试验、重复发表、非临床研究文献,初筛得到41篇文献。进一步阅读全文排除不符合纳入标准的文献后,最终纳入10个研究[8-17],总共包括721例患者。见表1。
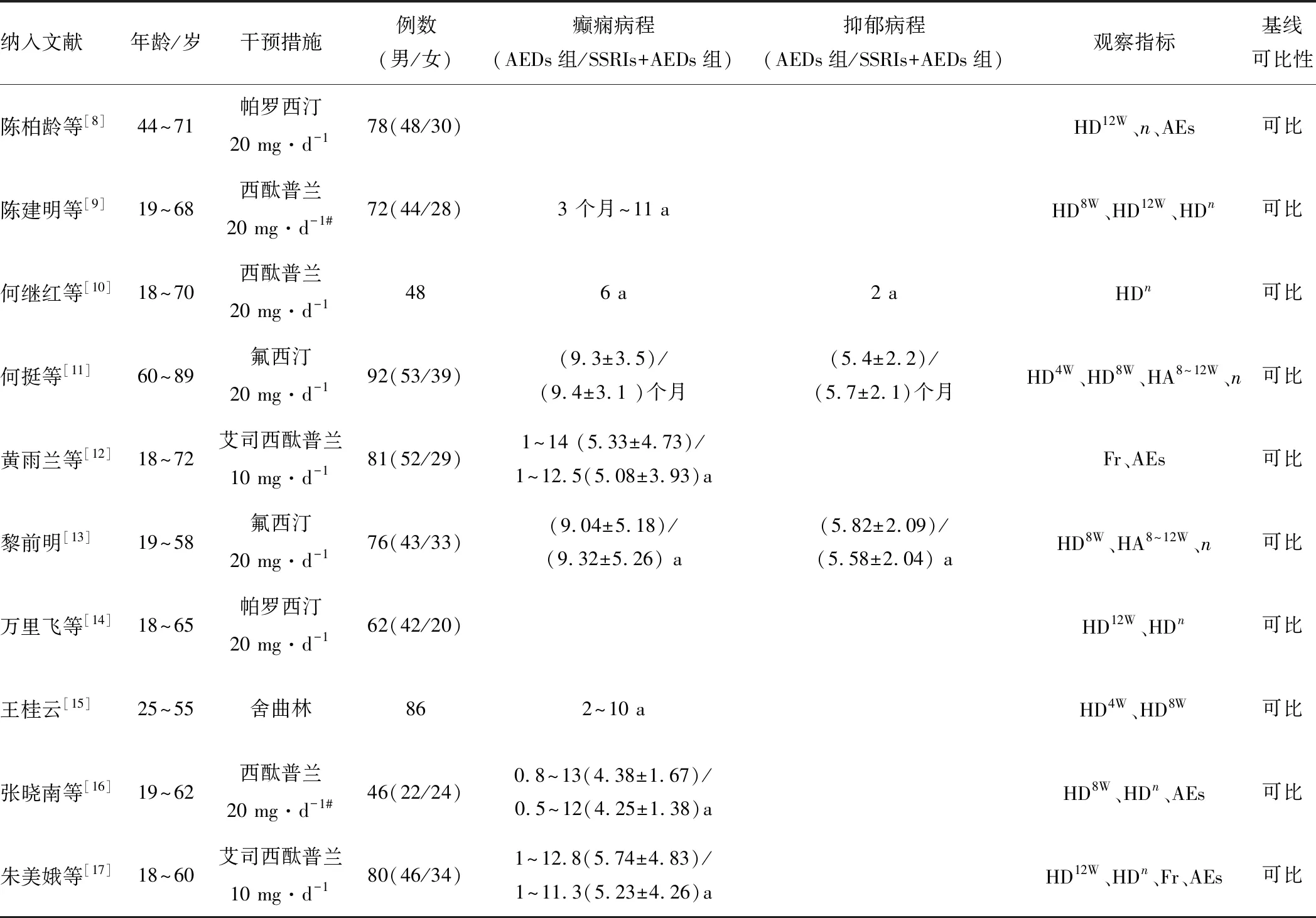
表1 纳入文献的基本特征
2.2 纳入研究的一般情况和质量评价纳入研究均提到采用随机分组,其中9个研究提到采用随机分配,1个研究详细记录失访退出情况,其他纳入研究均未描述盲法的实施、随机分配方案的隐藏和记录失访退出情况,根据Cochrane系统评价偏倚风险维度对文献进行质量评估。

图1 偏倚风险总结图
2.3 meta分析结果
2.3.1抑郁症状改善 纳入研究的9篇文献报道了SSRIs+AEDs组与AEDs组治疗癫痫合并抑郁症患者4、8和12周HAMD评分。亚组分析显示,各结果有统计学异质性(P=0.97,I2=0;P<0.01,I2=96%;P=0.30,I2=16%),其异质性可能与各研究中患者的抑郁程度构成比差异有关,故采用随机模型进行分析。meta分析结果显示,SSRIs+AEDs组在治疗4、8和12周的HAMD评分均低于AEDs组:4周的合并效应量为MD=-4.99(95% CI:-5.84~-4.15,P<0.01);8周的合并效应量为MD=-9.84(95% CI:-13.86~-5.83,P<0.01);12周的合并效应量为MD=-5.70(95% CI:-7.24~-4.16,P<0.01)。见图2。4篇文献报道了SSRIs+AEDs组与AEDs组治疗癫痫合并抑郁症患者8、12周达到HAMD评分有效减分率的比例,亚组分析显示,各结果无统计学异质性(P=0.86,I2=0;P=0.97,I2=0),故采用固定模型进行分析。meta分析结果显示,SSRIs+AEDs组达到HAMD评分有效减分率的比例高于AEDs组:8周的合并效应量为OR=35.50(95% CI:12.20~103.28,P<0.01);12周的合并效应量为OR=6.42(95% CI:2.43~16.92,P<0.01)。见图3。
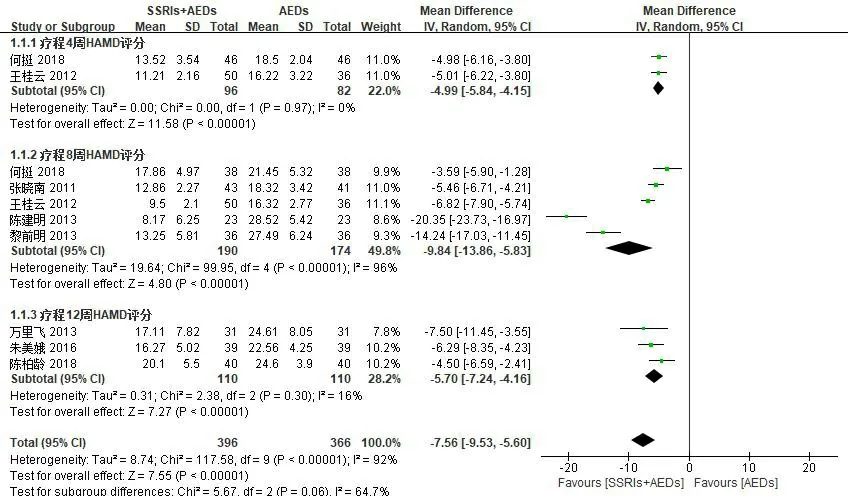
图2 HAMD评分meta分析
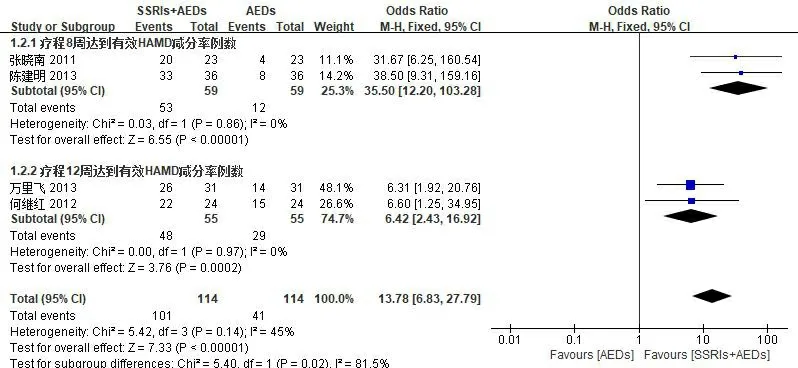
图3 达到有效HAMD减分率例数meta分析
2.3.2焦虑症状改善 纳入研究的2篇文献关注了SSRIs+AEDs组与AEDs组治疗癫痫合并抑郁症患者焦虑症状的HAMA评分。分析显示,结果有统计学异质性(P<0.01,I2=99%),故采用随机模型进行分析。meta分析结果显示:两组治疗癫痫合并抑郁症患者HAMA评分比较,差异无统计学意义:合并效应量为MD=-12.44(95% CI:-28.05~3.18,P=0.12)。见图4。
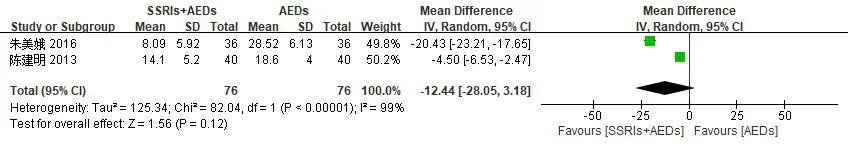
图4 HAMA评分meta分析
2.3.3控制癫痫发作 2篇文献报道了SSRIs+AEDs组与AEDs组治疗癫痫合并抑郁症患者的癫痫发作频率。分析显示,结果无统计学异质性(P=0.70,I2=0),故采用固定模型进行分析。meta分析结果显示,SSRIs+AEDs组癫痫发作频率低于AEDs组,合并效应量为MD=-0.58(95% CI:-0.71~0.45,P<0.01)。见图5A。提示SSRIs可能协同AEDs发挥抗癫痫作用。3篇文献研究了SSRIs+AEDs组与AEDs组有效控制癫痫发作的比例,各结果无统计学异质性(P=0.74,I2=0),故采用固定模型进行分析。meta分析结果显示SSRIs治疗癫痫合并抑郁症患者有效控制癫痫发作频率的比例高于对照组,合并效应量为OR=4.95(95% CI:2.27~10.79,P<0.01)。见图5B。

B
2.3.4不良反应 6篇文献研究了SSRIs组与AEDs组治疗癫痫合并抑郁症患者的不良反应发生情况。分析显示,结果无统计学异质性(P=0.73,I2=0),故采用固定模型进行分析。meta分析结果显示,两组治疗癫痫合并抑郁症患者的不良反应发生率比较,差异无统计学意义,合并效应量为OR=1.13(95% CI:0.68~1.88,P=0.62)。见图6。

A
3 讨论
本研究评价纳入10项研究,共有721例患者(SSRIs+AEDs组368例,AEDs组353例),这些文献提供了详细的治疗效果。癫痫合并抑郁症患者的HAMD评分分为4、8和12周疗程亚组,达到有效HAMD评分减分率的比例分为8、12周疗程亚组,以上两类结局指标无论亚组分析或总体分析,合并效应量均表明SSRIs能够有效改善癫痫合并抑郁症患者的抑郁症状。SSRIs影响癫痫发作控制程度的两个结局指标为有效控制癫痫发作例数和控制癫痫发作频率,这两组结局指标的合并效应量表明SSRIs可能增强AEDs的抗癫痫作用,这与以往临床研究相符[18]。不良反应结局指标分析发现SSRIs+AEDs组与AEDs组的效应量无统计学差异,提示SSRIs治疗癫痫合并抑郁症患者不良反应较少。
本研究纳入的文献均明确指出采用随机分配方法将患者分为SSRIs+AEDs组和AEDs组,保证了结局数据的完整性,但未表明是否对研究者和受试者施盲以及盲法评价测量指标、选择性报告研究结果及其他偏倚来源。本研究纳入的文献质量一般,造成结论的可靠性局限。分析以上合并结果的异质性,8周HAMD评分的5篇文献存在异质性,可能是患者的病情严重程度、评定者对量表评定的熟练程度影响了结果;HAMA评分的4篇文献存在异质性,可能由于两篇文献的疗程分别是8周和12周,评估时间点的不同造成了HAMA评分的异质性。
综上所述,在现有证据资料基础上,本研究结果表明,SSRIs能够改善癫痫合并抑郁症患者的抑郁症状,减少癫痫发作频率,且不良反应较少。为临床应用SSRIs治疗癫痫合并抑郁症患者提供了新的依据,可为早期识别和恰当治疗癫痫合并抑郁症提供用药参考。由于所纳入研究存在潜在发表偏倚,为全面客观地评估SSRIs治疗癫痫合并抑郁症,需要大样本、 多中心的高质量对照试验加以证实。

