柱前衍生-超高效液相色谱-电化学检测法测定牙膏中氨甲环酸
冯梅艳,罗 敏,何 婷,徐时杰,汪辉娟,陈荣祥,3∗
(1.遵义医科大学 基础医学院,遵义 563000; 2.遵义医科大学 药学院,遵义56300;3.遵义市理化分析测试工程技术研究中心,遵义 563000)
氨甲环酸又称凝血酸或止血环酸,具有止血、美白等作用,广泛运用于医疗卫生和美容行业,临床上可用于全髋关节、全膝关节置换以及黄褐斑的诊疗[1-2]。氨甲环酸在临床上有明确的用量规定,但如果过量服用,就会造成非常严重的后果。因此,氨甲环酸的添加量须控制在一个安全的范围内。调查发现,市场上有部分治疗牙龈出血功效的牙膏使用了氨甲环酸,且牙膏的专利也将氨甲环酸的添加作为技术的创新点[3]。但是,目前国内还没有关于日用品中氨甲环酸限量的相关规定。因此,建立一种高效便捷的测定日用品中氨甲环酸含量的方法,对日用品中氨甲环酸添加量的监测及相关规定的制定都是极有意义的。
氨甲环酸的测定方法主要有分光光度法[4]、气相色谱-质谱法(GC-MS)[5]、高效液相色谱法(HPLC)[6-8]、超高效液相色谱-串联质谱法(UPLCMS/MS)[9]等。相对于其他方法,HPLC 和UPLCMS/MS具有出色的分离性能、快速的分析时间和较高的灵敏度等特点,应用非常广泛。但是,HPLC常用的紫外检测器(UVD)的检测灵敏度较低,在氨甲环酸的检测波长(220 nm)附近,干扰较为严重。氨甲环酸属于氨基酸,因此可采用衍生化的方式提高UVD 对其的检测灵敏度,而适用于氨基酸的衍生试剂有很多,文献[10-11]采用丹磺酰氯衍生试剂进行柱前衍生,用UVD 对牙膏和化妆品等样品中的氨甲环酸含量进行了测定,检出限可达0.3~2.0 mg·kg-1,极大提高了HPLC 的检测灵敏度;邻苯二甲醛(OPA)常联合巯基乙醇、巯基丙酸、N-乙酰-L-半胱氨酸、亚硫酸钠等巯基化合物(用作还原剂)来对氨基酸进行衍生[12-13],前3种巯基化合物的衍生物常用UVD 或荧光检测器(FLD)检测,而亚硫酸钠会影响目标物衍生物的吸光度,因此常用电化学检测器(ECD)检测[13-14]。和光学检测器相比,ECD 具有较高的灵敏度和选择性,近年来在生命科学、药物、食品分析中的应用较多[15-17]。ECD的检测池一般分为安培检测池和库仑检测池,安培检测池可通过调节工作电极与对电极之间的距离来调节检测灵敏度,但长时使用时,电极表面容易受污染,电极响应下降,因此在分析基质复杂的样品时,其日间精密度较差,需要定期进行电极维护;库仑检测池以多孔石墨电极作为工作电极,和安培检测池相比,多孔石墨电极的表面积更大,抗污染能力更强,且可实现目标物在电极表面接近完全氧化,响应更高[14]。
本工作采用OPA-亚硫酸钠对氨甲环酸进行柱前衍生,采用UPLC 分离,采用ECD 检测,建立了一种快速、灵敏地测定牙膏中氨甲环酸含量的方法,以期为牙膏等日化产品中氨甲环酸的监测提供技术参考。
1 试验部分
1.1 仪器与试剂
Thermo Ultimate 3000 Bio-RS 型超高效液相色谱仪,配ECD-3000RS 型电化学检测器,检测池为6011型库仑检测池;5B-5200DT 型超声波清洗机;ME104/2型电子天平;FE 28型p H 计;PURELAB Chorus 2型纯水及超纯水系统。
氨甲环酸储备溶液:称取氨甲环酸标准品10 mg,用水溶解并定容,配制成0.99 g·L-1的溶液,其他所需质量浓度均由此溶液稀释制得。
衍生试剂溶液:称取OPA 15 mg,用0.5 mL甲醇溶解;同时称取亚硫酸钠0.13 g,用0.5 mL 水溶解;将上述两种溶液混合,加入0.1 mol·L-1硼砂缓冲溶液(pH 10.0)9 mL,混合均匀,作为储备溶液备用,于4 ℃避光保存,使用有效期为3 d。使用时用0.1 mol·L-1硼砂缓冲溶液(pH 10.0)将储备溶液稀释定容至100.0 mL(其中OPA 和亚硫酸钠的质量浓度分别为150 mg·L-1和1.3 g·L-1),该溶液即为衍生试剂溶液,现用现配。
氨甲环酸标准品的纯度不小于99%;OPA 的纯度不小于99%;甲醇、乙腈、乙酸铵均为色谱纯,亚硫酸钠、氢氧化钠、硼砂均为分析纯;试验用水为超纯水;牙膏购自本地超市,共6种,其中一种标注有氨甲环酸的添加。
1.2 仪器工作条件
Waters ACQUITY UPLC BEH C18色谱柱(100 mm×2.1 mm,1.7μm),柱温为40 ℃;检测电压为500 mV;流量为0.4 mL·min-1;流动相为体积比为2∶8的乙腈-30 mmol·L-1乙酸铵缓冲溶液(pH 3.6),等度洗脱;进样体积为1μL。
1.3 试验方法
称取牙膏样品约1 g,加入水50 mL,超声萃取30 min,以12 000 r·min-1转速离心10 min,在上清液中加入和上清液等体积的衍生试剂溶液,在室温、标准大气压条件下反应5 min,按照仪器工作条件进样测定。
2 结果与讨论
2.1 色谱行为
按照仪器工作条件对衍生后的氨甲环酸标准溶液进行测定,色谱图见图1。
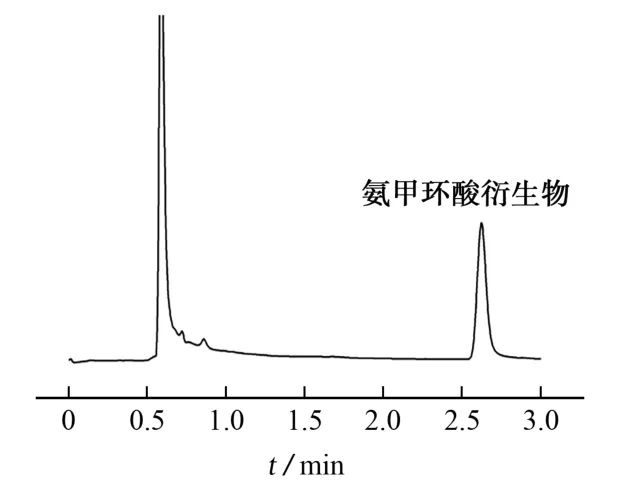
图1 氨甲环酸衍生物色谱图Fig.1 Chromatogram of the derivative of aminocyclic acid
2.2 流动相条件的优化
2.2.1 乙酸铵缓冲溶液酸度
当用色谱分离氨甲环酸的衍生物时,流动相的酸度对氨甲环酸衍生物的保留时间影响很大。试验考察了乙酸铵缓冲溶液的酸度对衍生物保留时间的影响。结果发现:pH 7.0时,衍生物以离子化形式存在,在C18色谱柱中几乎无保留;酸度继续增加,衍生物的保留时间增加;当pH 为3.6时,氨甲环酸衍生物的分离度好,峰形对称,且容量因子适中。因此,试验选择乙酸铵缓冲溶液的pH 为3.6。
2.2.2 乙酸铵缓冲溶液浓度
为了消除衍生反应中较高浓度碱性缓冲溶液[0.1 mol·L-1硼砂缓冲溶液(pH 10.0)]对流动相酸度的干扰,试验考察了乙酸铵缓冲溶液浓度分别为15,30 mmol·L-1时对氨甲环酸衍生物峰形的影响。结果发现:当采用15 mmol·L-1乙酸铵缓冲溶液时,氨甲环酸衍生物峰形不对称,色谱峰拖尾;继续增加乙酸铵缓冲溶液的浓度,当乙酸铵缓冲溶液浓度为30 mmol·L-1时,峰形得到明显的改善,满足试验要求。因此,试验选择乙酸铵缓冲溶液的浓度为30 mmol·L-1。
2.3 检测电压的优化
试验考察了检测电压在600 mV 以内时对目标衍生物峰面积的影响,结果见图2。
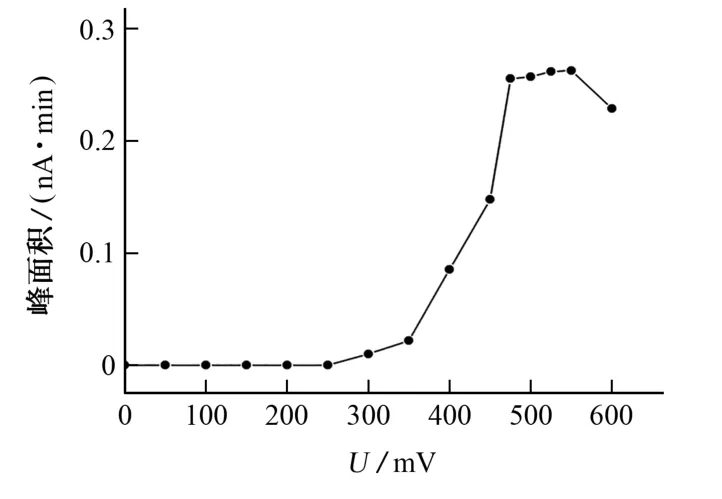
图2 检测电压对峰面积的影响Fig.2 Effect of detect potential on peak area
由图2可以看出:当检测电压在250 mV 以内时,衍生物的信号几乎为0;当检测电压大于300 mV 时,衍生物的峰面积值随着检测电压的升高而增大;当检测电压为475 mV 时,峰面积接近最大值;当检测电压为475~550 mV 时,峰面积基本保持稳定;当检测电压大于550 mV 时,峰面积降低。综合考虑,试验选择检测电压为500 mV。
2.4 OPA质量浓度的优化
试验考察了衍生试剂溶液中OPA 的质量浓度分别为0,15,30,75,150,300 mg·L-1时对目标衍生物峰面积的影响,结果见图3。
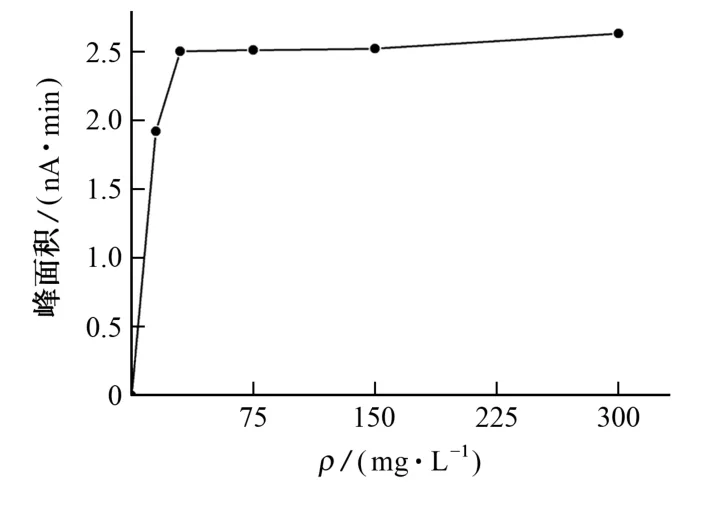
图3 OPA 质量浓度对峰面积的影响Fig.3 Effect of the mass concentration of OPA on the peak area
由图3可以看出:当OPA 质量浓度为30 mg·L-1时,衍生物峰面积接近最大值;继续增加OPA的质量浓度,峰面积保持稳定。由于实际样品中氨甲环酸的添加量不确定,为保证高添加量样品的检测准确度,试验采用OPA的质量浓度为150 mg·L-1。
2.5 标准曲线和检出限
按照仪器工作条件对衍生化后的0.495,0.990,1.980,4.950,9.900,19.800 mg·L-1氨甲环酸标准溶液系列进行测定。以氨甲环酸的质量浓度为横坐标,其对应的峰面积为纵坐标绘制标准曲线。结果表明:氨甲环酸标准曲线的线性范围为0.495~19.800 mg·L-1,相关系数为0.999 7,线性回归方程为y=4.615x+1.230。
以3倍信噪比(S/N)计算检出限(3S/N),得到氨甲环酸的检出限为0.003 6 mg·L-1,换算到实际样品,得到的检出限为0.18μg·g-1。
2.6 精密度和回收试验
按照试验方法对添加了氨甲环酸的牙膏样品进行加标回收试验,加标水平为0.297 mg·g-1,平行制备6份进行测定,计算测定值的相对标准偏差(RSD)和回收率,得到回收率为98.6%,RSD 为2.4%。表明该方法的精密度较好,准确度较高。
2.7 重复性试验
按照试验方法平行制备6份样品溶液,按优化后的色谱条件进样测定,计算得衍生产物峰面积RSD 为3.3%。表明该方法的重复性良好。
2.8 衍生产物稳定性试验
采用OPA 和硫醇对氨基酸衍生化得到的衍生产物通常不稳定,采用亚硫酸钠代替硫醇类试剂可以提高衍生产物的稳定性[14]。为了考察氨甲环酸衍生产物的稳定性,将衍生化后的样品溶液在4 ℃条件下储存,每隔2 h进样测定,结果显示:12 h内,衍生产物保持稳定,峰面积下降了不到5%。
2.9 专属性试验
OPA 衍生试剂常用来衍生伯胺,为了确认其他氨基酸是否对氨甲环酸的测定存在干扰,分别对空白牙膏样品(不含氨基环酸)、加标牙膏样品、氨甲环酸标准溶液按照试验方法进行测定,结果显示,杂质峰对氨甲环酸峰均无干扰。因为牙膏中常见的氨基酸类添加剂为精氨酸和茶氨酸,二者的衍生物均在氨甲环酸衍生物之前出峰,不会干扰氨甲环酸的测定。
2.10 样品分析
按照试验方法分析了6份牙膏样品,只在添加了氨甲环酸的牙膏样品中检出了氨甲环酸,添加量为0.23 mg·g-1。实际样品的色谱图见图4。

图4 牙膏样品色谱图Fig.4 Chromatogram of the toothpaste sample
2.11 方法比对
将本方法与文献中氨甲环酸的测定方法进行了比对,结果见表1。

表1 本方法同文献中方法结果的比较Tab.1 Comparison of results between this method and other methods in the literature
由表1可知:与其他方法相比,本方法的灵敏度更高,有助于更低添加水平的氨甲环酸含量的测定;另外,牙膏中含有的大量表面活性剂,会造成色谱柱的较大损伤,而本方法可对样品进行大比例稀释,进而减少表面活性剂的进样量,延长色谱柱的寿命。
本工作建立了柱前衍生-UPLC-ECD 测定牙膏中氨甲环酸含量的方法,该方法准确度、精密度、重复性、稳定性、专属性均较好,适用于牙膏中氨甲环酸含量的测定。

