富马酸喹硫平脂质立方液晶制备工艺研究*
田 勇,李见春,李婷婷,侯方燕
(1. 蚌埠医学院第一附属医院,安徽 蚌埠 233000; 2. 蚌埠医学院药学院,安徽 蚌埠 233000)
富马酸喹硫平(QF)是经典的第2 代抗精神病药物,主要通过拮抗中枢D2受体和5-HT2受体发挥作用,用于治疗精神病疗效佳,且药物安全系数较高,对精神分裂症的疗效肯定,同时对狂躁症也有一定疗效。目前,市场多为片剂,口服易产生心悸、嗜睡、头晕、食欲不振和便秘等不良反应[1-2]。脂质立方液晶(LCNP)是两亲性聚合物,分散于水溶液时可自发组装形成一种新的分散体系,能包封不同极性的药物[3]。立方液晶的稳定性优于脂质体,进入人体后受到免疫系统的干扰较少[4-5]。对于溶解性较差的药物,立方液晶内部独特的立方相结构可包载各种不同极性的药物,显著增加难溶性药物的生物利用度,减少毒副作用[6-7]。本研究中将富马酸喹硫平制备成立方液晶纳米粒,以降低喹硫平的不良反应,同时提高生物利用度。为确保富马酸喹硫平立方液晶(QF-LCNP)具有较高的包封率,对QF-LCNP 的制备工艺进行了优化。现报道如下。
1 仪器与试药
1.1 仪器
Nano-ZS90 型粒度检测仪(英国Marlven 公司);JN-04HCF 型高压均质机(聚能生物科技公司);Milli-A10 型纯水机(英国Milibol 公司);TGR16-WJ 型高速离心机(长沙湘仪离心机仪器有限公司);TB5210FB 型超声波清洗器(昆山超声仪器有限责任公司,功率为180 W,频率为40 kHz)。
1.2 试药
甘油单油酸酯(上海Boilmen 公司,批号为1921036);泊 洛 沙 姆407(上 海Sigma 公 司,批 号 为163223);甲醇、乙腈(色谱纯,国药集团,批号为176331);富马酸喹硫平(成都贝斯特股份有限公司,批号为131227FM,含量为99.4%);透析袋(截留相对分子质量为8 000~14 000,美国Viskase 公司,批号为201810112111)。
2 方法与结果
2.1 处方筛选与验证

图1 偏光显微镜观察到的液晶形态
采用注入法制备QF-LCNP,将脂质材料甘油单油酸酯(GMO)与稳定剂泊洛沙姆407(F127)按一定比例混合,融化后搅拌成均一的澄明液体,向脂质溶液内逐滴加入同温足量的蒸馏水,边滴加边搅拌,经高压均质机后,形成立方液晶纳米粒。参考文献[8-9],根据GMO 形成立方液晶的三元相图,对形成立方液晶所需的原料比例进行初步筛选。取不同比例的GMO 和F127适量,精密称定,60 ℃水浴融化,形成均一脂质液,向脂质液内缓慢加入不同质量分数(wt%)的蒸馏水,磁力搅拌10 min,通过高压均质机均质一定次数,即得白色乳状液。偏光显微镜观察并记录样品形态。详见图1 和表1。
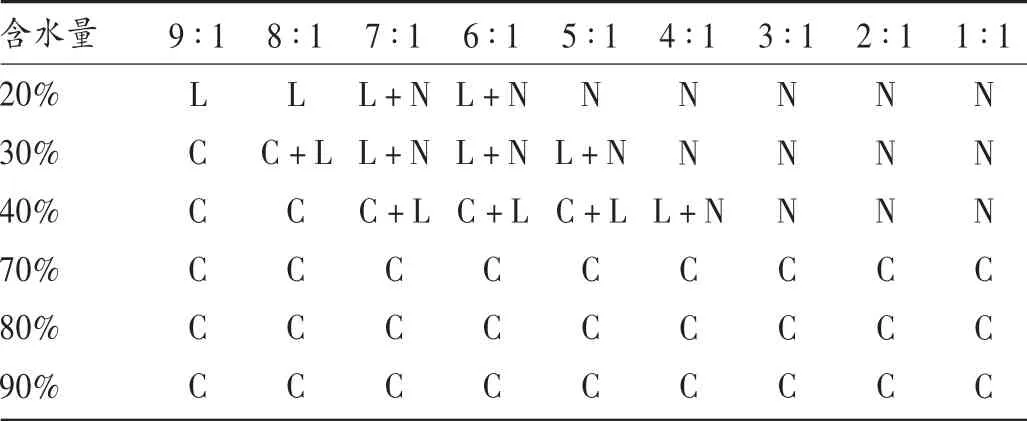
表1 GMO 与F127 的处方比例对液晶形态的影响
由图1 可见,各液晶形态差异,层状液晶为片状雪花样结构,非液晶在偏光下呈现无序样结构,立方液晶的光学特性为各同向性,在偏光显微镜下无偏光,故呈现暗视野。由表1 可见,当含水量在较低区间(20%~40%)范围内时,大多为层状液晶和非液晶形态,当含水量在较高区间(70%以上)范围内时,基本形成立方液晶,表明立方液晶的形成与含水量有关,同时GMO 与F127的比例也有一定影响,GMO 质量比重越高,越易形成立方液晶,基本符合GMO 的三元相图[10]。
2.2 处方工艺优化
根据处方工艺的筛选与验证,选择影响药物包封率较大的4 个因素:蒸馏水用量(mL,因素A),药物占GMO 质量比(因素B),甘油单油酸酯与F127 的质量比(两者总质量为1 g,因素C),搅拌时间(min,因素D),将以上4 个因素设计成L9(34)的正交试验,以QF-LCNP的包封率为考察指标,因素水平见表2,正交试验结果见表3,方差分析见表4。由表2 可见,各因素对包封率的影响程度为C >A >B >D,因素A 及因素C 对包封率有显著影响。故富马酸喹硫平立方液晶的最佳处方工艺为A3B2C1D3,即富马酸喹硫平投药量为54 mg,蒸馏水为40 mL,甘油单油酸酯投药量为900 mg,泊洛沙姆407 投药量为100 mg,搅拌时间为18 min。

表2 富马酸喹硫平立方液晶处方筛选的影响因素水平
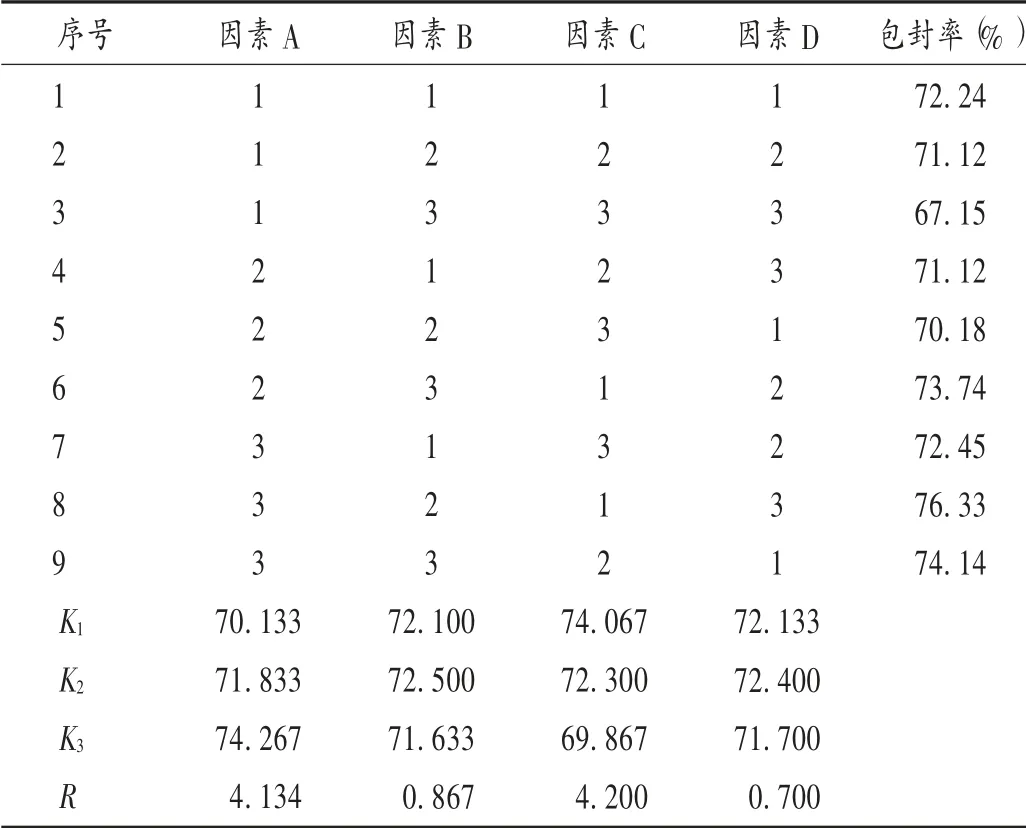
表3 正交试验结果
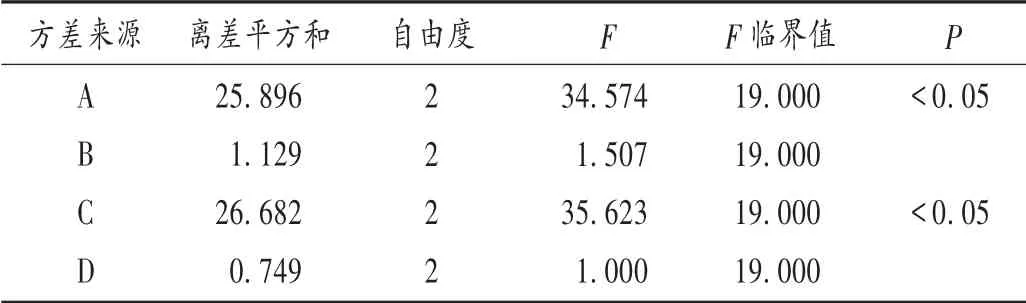
表4 包封率方差分析结果
2.3 制备工艺优化
2.3.1 均质压力考察
高压均质机预热10 min,用蒸馏水冲洗均质机内部,将恒温水接通入均质槽内,均质机内槽保持恒温,温度设置为25 ℃,将QF-LCNP 放入高压均质机内,固定均质次数为5 次,调整均质压力,分别设为1 000,1 500,2 000,2 500 bar(1 bar=0.1 MPa),收集均质后QF-LCNP,测定药物的包封率及粒径。结果见表5。可见,当均质次数设为定值时,均质压力对富马酸喹硫平包封率和平均粒径影响较大,随着均质压力的增高,QF-LCNP 的包封率和粒径逐渐降低,当均质压力超过2 000 bar 时,粒径下降不明显。当均质压力过高时有可能会破坏一部分立方液晶的结构,故选择2 000 bar 作为制备富马酸喹硫平立方液晶纳米粒的最优制备工艺。
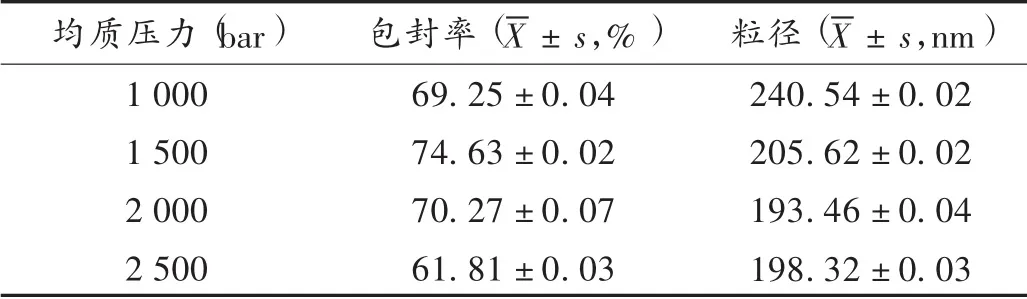
表5 不同均质压力对包封率及粒径的影响(n=3)
2.3.2 均质次数考察
高压均质机预热10 min,用蒸馏水冲洗均质机内部,将恒温水接通入均质槽内,均质机内槽保持恒温,温度设为25 ℃,将QF-LCNP 放入高压均质机内,设置均质压力为最优1 500 bar,均质次数分别为2,4,6,8 次,收集均质后QF-LCNP,测定包封率及粒径,结果见表6。可见,均质次数对富马酸喹硫平的包封率和平均粒径均有影响,随着均质次数的增加,立方液晶纳米粒的粒径逐渐下降,当均质次数超过6 次时,包封率有所降低,粒径下降不明显。故最终选择循环次数为6 次作为最优制备工艺条件。

表6 不同均质次数对包封率及粒径的影响(n=3)
2.4 制剂含量测定方法建立
2.4.1 色谱条件
色谱柱:Thermo C18柱(250 mm×4.6 mm,5 μm);流动相:甲醇-水(含0.5%三乙胺,冰醋酸调节pH 至6~8,78 ∶22,V/ V);流速:1 mL/min;检测波长:289 nm;柱温:45 ℃;进样量:20 μL。
2.4.2 溶液制备
取富马酸喹硫平对照品0.5 mg,精密称定,置10 mL容量瓶,用甲醇稀释并定容,4 ℃冰箱保存,备用。临用前用甲醇稀释。取富马酸喹硫平立方液晶纳米粒5 mg,精密称定,置100 mL 容量瓶中,用甲醇溶解并稀释至刻度,0.22 μm 滤膜过滤,即得。
2.4.3 方法学考察
标准曲线绘制:精密量取富马酸喹硫平对照品贮备液,用甲醇稀释成质量浓度分别为1,2,4,8,16,32,64,128 μg / mL 的系列标准溶液。按拟订色谱条件进样20 μL,记录峰面积。以质量浓度(X)为横坐标、峰面积(Y)为纵坐标进行线性回归,得回归方程Y=28 612 X +29 549,R2=0.999 7(n=8)。结果表明,富马酸喹硫平质量浓度在1~128 μg/mL 范围内与峰面积线性关系良好。
精密度试验:精密量取富马酸喹硫平对照品贮备液,配置低、中、高质量浓度(分别为4,16,64 μg/mL)的对照品溶液,按拟订色谱条件进样6 次,记录峰面积。结果的RSD 为1.32%(n=6),表明仪器精密度良好。
稳定性试验:制备同批QF-LCNP 样品,分别于0,2,4,6,8,12,24 h 时按拟订色谱条件进样测定。结果的RSD 为1.14%(n=7),表明供试品溶液在24 h 内稳定。
加样回收试验:精密量取同一已知含量的QF-LCNP供试品溶液9 份,每3 份1 组,置10 mL 容量瓶中,分别加入相当于标示量80%,100%,120%的对照品溶液适量,用甲醇稀释至刻度,按拟订色谱条件进样测定,记录峰面积,并计算加样回收率。结果见表7。
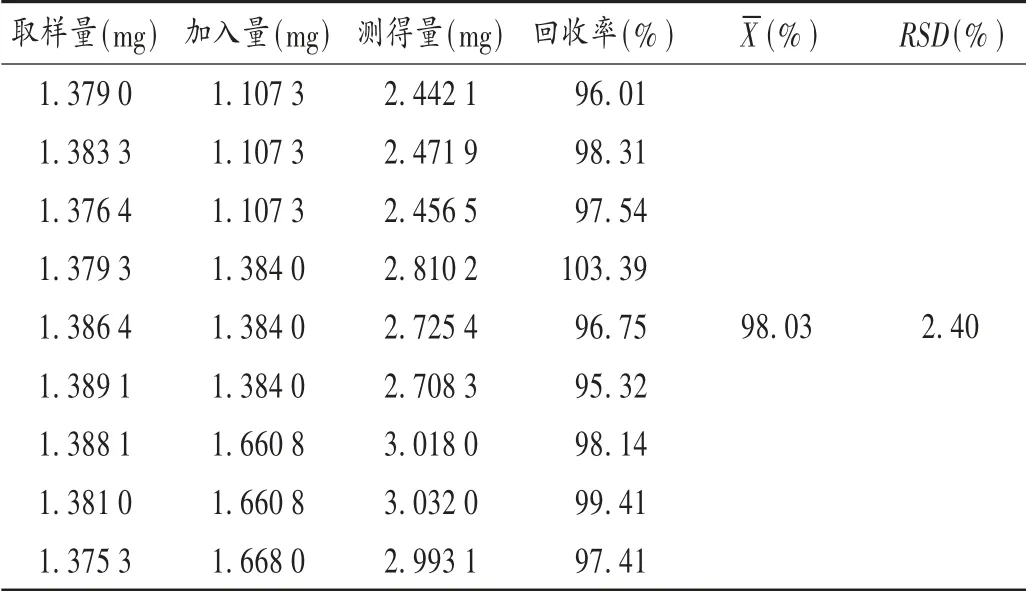
表7 加样回收试验结果( n=9)
2.5 体外药物释放
采用透析法[11],释放介质选取pH 7.4 磷酸盐(PBS)缓冲液,以富马酸喹硫平对照品为对照,进行体外释药试验。分别精密量取QF 对照品溶液和QF-LCNP各0.5 mL,将样品放入已处理好的透析袋内,两端扎紧,浸入100 mL pH 7.4 PBS 缓冲液中,密封,维持温度在37 ℃,磁力搅拌,于设定时间点取样,同时补充相同体积的释药介质,以保证透析环境不变。取1 mL 透析介质,0.22 μm 微孔滤膜滤过,测定每个取样点时的药物含量,计算累积释放度。结果见图2。

图2 QF-LCNP 和喹硫平溶液释放曲线(n=3)
可见,QF 溶液在前10 h 内的累积释放度约达到100.00%,而富马酸喹硫平脂质立方液晶在前10 h 内的累积释放度约为58.00%,体外48 h 的累积释放度约为84.67%,相比于QF 溶液有一定的缓释效应。
3 讨论
以富马酸喹硫平的包封率为指标,采用单因素和正交试验设计,从处方配比中可发现,立方液晶的形成与GMO/F127 的比例及水含量相关,含水量低于40%较难形成立方液晶,且存在一定的层状液晶及非液晶形态;当水含量超过70%时,基本可形成立方液晶体系。另外,GMO 质量比重与立方液晶的形成有关,因为构成立方液晶的整体骨架主要是甘油单油酸酯,F127 的作用则是嵌入骨架缝隙的稳定剂,因此引入过多的稳定剂F127 会干扰立方液晶的形态。
在选取影响包封率的4 个因素中,分散相用量和GMO 与F127 质量比均有统计学差异,表明该因素对包封率有显著影响,符合立方液晶的晶体特性[12-14]。
制剂通过超声、均质后制备的纳米颗粒能显著提高药物的包封率。目前,制备立方液晶多采用纳米均质法,可实现低温下水浴循环制备纳米粒,制备过程中能保证粒子结构的稳定性。故本试验中选用均质机制备立方液晶纳米粒,对QF-LCNP 制备过程中的影响因素进行考察。均值压力和均质次数在一定范围内可影响药物的包封率和粒径,由于在均质过程中增加均质压力和均质次数可能会导致仪器温度升高,破坏立方液晶结构,故在试验前加入循环恒温引流水,保证均质管内的温度恒温。均质压力超过1 500 bar 时,药物的包封率有所降低,可能是过高的能量破坏了立方液晶结构或导致立方液晶晶型的转变。
体外药物释放是考察缓释制剂体外释放速率的有效方法。本试验中采用透析法、高效液相色谱法测定药物释放量,结果显示,QF-LCNP 具有明显的缓释作用。此外,文献[15]的研究表明,立方液晶能明显提高药物脑部吸收,为QF-LCNP 的体内试验提供了一定依据。本试验中最后优化得到的处方各项指标均在正常范围内,确定了富马酸喹硫平脂质立方液晶制备工艺的可行性,可为QF-LCNP 的深入研究提供参考。

