溶胶-凝胶法制备烯肟菌胺分子印迹聚合物及性能研究
王岩松,贺明睿,王冬妍,姜鑫,罗景阳,袁帅
(1.沈阳市食品药品检验所,辽宁 沈阳 110124;2.沈阳化工大学,辽宁 沈阳 110142;3.辽宁省药品检验检测院,辽宁 沈阳 110036)
溶胶-凝胶分子印迹技术是采用溶胶-凝胶法将模板分子引入无机网络结构中制备分子印迹聚合物(Molecular Imprinted Polymer,MIP)的一项技术,是溶胶-凝胶法和分子印迹技术的结合体[1-3]。模板分子在聚合物基体中以共价键,非共价键,氢键等形成具有“记忆”功能的识别位点。模板分子脱离聚合物后留下与其结构相匹配的立体空腔,通过立体空腔与识别位点对模板分子表现出特异的识别性[4-5]。目前分子印迹聚合物已广泛应用于分离技术、传感技术、环境检测、食品检测等领域,展现了良好的性能和应用前景[6-7]。
烯肟菌胺作为模板分子,均匀的镶嵌在钛酸丁酯的聚合物中,依靠烯肟菌胺分子构型和物理吸附在聚合物中形成与之相匹配立体空间结构,通过索氏提取洗脱模板分子后,保留具有特异吸附性能的空腔,空腔的比例和识别位点的分布直接影响着印迹聚合物的吸附性和特异性。优化模板分子与功能单体的比例,聚合过程中酸的加入量,温度的控制等实现烯肟菌胺分子印迹聚合物的最佳吸附性能。
1 实验部分
1.1 仪器与试剂
串联质谱仪(API 4000,美国应用生物系统公司);液相色谱仪(LC 20A,日本岛津公司);电子天平(BS244S,赛多利斯科学仪器有限公司);电热鼓风干燥箱(101-2,余姚市远东数控仪器厂);集热式恒温加热磁力搅拌器(DF-101S,巩义市英峪予华仪器制造厂);台式离心机(800-1,金坛区西城区新瑞仪器厂);恒温水浴振荡器(SHA-B,国华企业);电子万用炉(DL-1,北京市永光明医疗仪器有限公司);数控超声波清洗器(KQ5200DE,昆山市超声仪器有限公司)。
烯肟菌胺(质量分数98%,沈阳化工研究院);氟吗啉(质量分数95%,沈阳化工研究院);烯酰吗啉(质量分数98%,德国的Sigma公司);无水乙醇(分析纯,天津市大茂化学试剂厂);钛酸丁酯(分析纯,天津市风船化学试剂科技有限公司);盐酸(分析纯,国药有限公司);冰乙酸(分析纯,天津市大茂化学试剂厂);甲醇、乙腈(色谱纯,美国Fisher公司)。
1.2 MIP的制备
准确称取0.382 4 g烯肟菌胺于250 mL三角瓶中,加入60 mL无水乙醇搅拌至完全溶解。逐滴加入一定量的钛酸丁酯,充分混匀后缓慢加入一定体积的盐酸(1 mol·L-1),再加入1 mL 去离子水,在一定温度的水浴中搅拌5 h得到透明溶胶。取出三角瓶置于40℃烘箱中保温48 h形成凝胶,升高温度至60℃干燥24 h,充分研磨后置于索氏提取器中,60 mL无水乙醇-乙酸(体积比为8∶2)提取6 h,反复多次用甲醇-水(体积比为1∶1)超声洗脱至洗脱液为中性后用甲醇洗脱,LC-MS/MS检测不到烯肟菌胺分子为止,将聚合物置于60℃烘箱中烘干后得到烯肟菌胺分子印迹聚合物,置于干燥器中备用。
非分子印迹聚合物(NIP)的制备步骤除不添加烯肟菌胺,与MIP 制备方法一致。
1.3 MIP的性能表征
1.3.1 LC-MS/MS检测的条件
Symmetry C18色谱柱(150 mm×2.1 mm,3.5 µm);流动相A为水,B为甲醇,分别添加质量分数为0.1%的甲酸;线性梯度洗脱程序:0~1 min为10%B,1~5 min由10%B变为95%B,5~7 min由80%B变为95%B,7~7.5 min由95%B变为10%B,7.5~10 min 保持10%B。流速:0.3 mL·min-1。柱温:35℃。进样体积10 µL。
电喷雾离子源(electron spray ionization,ESI),正离子扫描;多反应监测(multiple reaction monitoring,MRM);电喷雾电压(ionspray voltage IS):5 500 V;雾化气压力:65 psi (448.16 kPa);气帘气压力:15 psi(103.42 kPa);辅助气压力:65 psi(448.16 kPa);离子源温度:550℃;定性离子对、定量离子对、碰撞气能量(collision energy,CE)及去簇电压(declustering potential,DP)见表1。

表1 烯肟菌胺、氟吗啉和烯酰吗啉的质谱参数
1.3.2 吸附动力学实验
准确称取20 mg MIP和NIP各7份,分别置于10 mL塑料离心管中,加入5 mL烯肟菌胺水溶液(10 mg·L-1)30℃恒温水浴震荡,不同时间间隔同时取出MIP和NIP各1份,离心后取上清液100 μL置于100 mL容量瓶中,蒸馏水定容至刻度,取1 mL溶液过0.22滤膜,供LC-MS/MS测定。10、20、30、40、50、60、80 min吸附量Q与吸附时间t作图,绘制吸附动力学曲线。吸附量计算见式(1)。
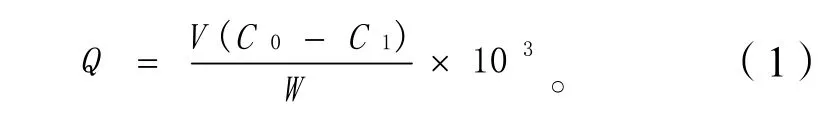
式中:Q—吸附量,μg·g-1;
V—烯肟菌胺标准溶液的体积,mL;
C0—烯肟菌胺的初始质量浓度,ng·mL-1;
C1—吸附后烯肟菌胺的质量浓度,ng·mL-1;
W—聚合物的质量,mg。
1.3.3 静态平衡吸附实验
准确称取20 mg MIP和NIP各6份,置于10 mL塑料离心管中,分别加入2、4、6、8、10和12 μg·mL-1的烯肟菌胺标准溶液5 mL,在30℃下恒温震荡60 min后离心,取上清液100 μL置于100 mL容量瓶中,蒸馏水定容至刻度,取1 mL溶液过0.22滤膜,供LC-MS/MS测定。吸附量Q与烯肟菌胺浓度C作图,绘制等温吸附曲线。
1.3.4 MIP选择性吸附实验
取20 mg MIP各3份置于10 mL塑料离心管中,分别加入5 mL质量浓度为10 μg·mL-1的烯肟菌胺、氟吗啉和烯酰吗啉水溶液,恒温震荡一定时间,供LC-MS/MS测定。比较MIP 对3种化合物的吸附性能。
2 结果与讨论
2.1 不同制备条件对MIP吸附性能的影响
2.1.1 印迹分子与交联剂的摩尔比对MIP吸附量的影响
通过改变烯肟菌胺与钛酸丁酯的摩尔比,考察其成胶效果和对MIP吸附性能的影响,制备过程中其他条件保持不变。
比较了烯肟菌胺与钛酸丁酯摩尔比为1∶10、1∶15、1∶20时,随着钛酸丁酯的量的增大成胶时间缩短,在摩尔比为1∶20时,胶体浑浊并出现乳白色悬浮颗粒。准确称取不同摩尔比的MIP各20 mg,置于10 mL质量浓度为10 μg·mL-1的烯肟菌胺水溶液中,室温下震荡吸附60 min,之后离心,上清液供LC-MS/MS测定。计算吸附量Q,分别为375、1 110和720 μg·g-1。推测在钛酸丁酯比例较低时,模板分子在聚合物中没有形成独立的空腔,特异识别位点较少,导致吸附性能较差。随着钛酸丁酯比例的增加,模板分子在聚合物中均匀的分散,形成完整独立的空腔和与模板分子相匹配的识别位点,因此吸附性能较强。但是随着钛酸丁酯比例的继续增加,模板分子在聚合物中形成空腔和识别位点的数量相对下降,同时部分模板分子被包裹在聚合物中无法脱离,导致MIP的吸附性能下降。因此实验选择烯肟菌胺与钛酸丁酯的摩尔比为1∶15。
2.1.2 酸的用量对MIP吸附量的影响
在聚合反应中,不改变其他聚合反应条件的同时,尝试不同酸的加入量考察对MIP吸附量的影响。
在5组聚合反应中分别加入浓度为1 mol·L-1的盐酸0.5、1.2、1.5、1.7、2.5 mL,盐酸的加入量为0.5和2.5 mL时,溶液未形成胶体状态,加入量为1.2、1.5和1.7 mL时,形成了透明的胶体,随着酸加入量的增加,成胶速度加快。当酸的加入量为1.5 mL时,MIP的吸附量最大为1 170 μg·g-1,减少和加大盐酸的加入量,吸附量都会相应地下降。因为钛酸丁酯带有电负性,少量H离子存在中和了电负性,提高分子间碰撞的概率,催化聚合反应。但是过量的H离子的存在,使得聚合反应过快,在短时间形成了较大的胶粒,模板分子被完全封锁在聚合物中间无法洗脱出来,降低了MIP应有的特异吸附性。因此综合以上实验,选择酸的加入量为1.5 mL。
2.1.3 反应温度对MIP吸附量的影响
温度是聚合反应速率的重要因素,实验比较了35、40、45、50℃条件下对聚合反应的影响。在35℃聚合时,10 h 未形成胶体。在40和45℃聚合时,分别在5和4.5 h形成无色透明溶胶状态,在50℃时3后溶液出现黏稠状,很快出现白色悬浮颗粒。对40和45℃制备的MIP进行了吸附量的测定,45℃制备的MIP吸附量1 170 μg·g-1略高于40℃制备的MIP吸附量1 085 μg·g-1,因此实验选择聚合反应温度为45℃。
2.2 MIP吸附性能实验
2.2.1 吸附动力学实验
聚合物的吸附动力学实验是为了考察吸附量随着吸附时间的增加的变化情况,MIP和NIP吸附量随着吸附时间的变化曲线见图1。如图所示,在30 min内MIP吸附量迅速增大,30到60 min加大缓慢,60到80 min处于平衡状态,NIP 在20 min后趋于平衡,在吸附曲线平衡阶段MIP的吸附量明显高于NIP。因为吸附开始阶段,溶液中模板分子浓度较大与聚合物接触频率较大,模板分子迅速与聚合物表面形成物理吸附,NIP 在20 min附近达到了饱和吸附;30 min前MIP在表面吸附同时模板分子进入“记忆”空腔,随着空腔和识别位点被占据增大了模板分子进入深层次空腔的阻力,吸附速率下降。在超声震荡的作用下,60 min后MIP达到了饱和吸附。
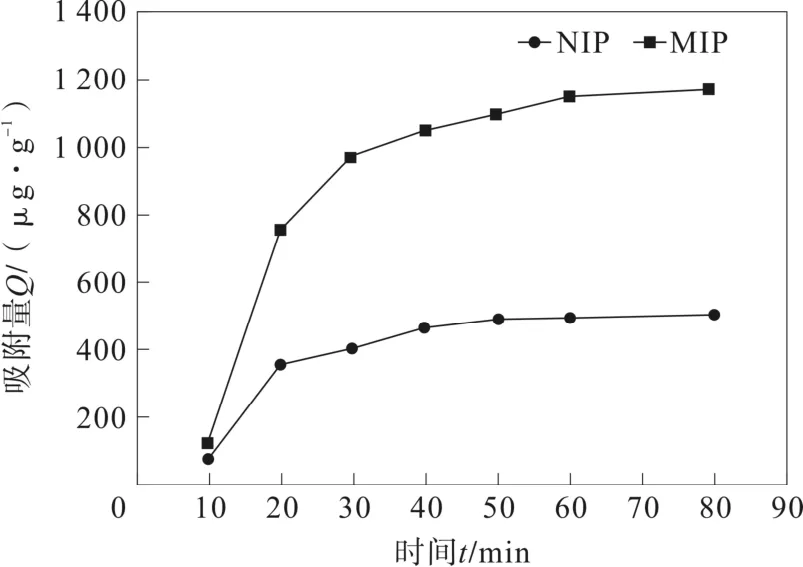
图1 MIP和NIP对烯肟菌胺的吸附动力学曲线
2.2.2 静态吸附实验
采用静态吸附法,考察在一定的条件下MIP和NIP对不同浓度的烯肟菌胺的吸附量。根据不同浓度下吸附量的变化,以不同溶液中烯肟菌胺浓度为横坐标,吸附量Q为纵坐标,作MIP和NIP的等温吸附曲线,吸附时间为60 min,见图2。

图2 聚合物的静态吸附曲线
如图2所示,MIP和NIP都表现出随着吸附烯肟菌胺浓度的升高吸附量变大的趋势,NIP的吸附曲线比较平稳,MIP曲线在4到8 μg·mL-1出现了突越,MIP结构中印迹空腔和识别位点与烯肟菌胺浓度相匹配,烯肟菌胺分子在MIP中迅速占位,在质量浓度达到10 μg·mL-1时吸附行为达到终点,最大吸附量为1 170 μg·g-1。NIP依靠自身的缝隙和疏松的结构也存在一定的吸附行为,饱和吸附量为520 μg·g-1。
2.2.3 MIP选择性的考察
在相同的实验条件下,比较了MIP对烯肟菌胺、氟吗啉和烯酰吗啉的吸附能力,实验结果MIP对烯肟菌胺的吸附量明显高于氟吗啉和烯酰吗啉,为1 170 μg·g-1。对氟吗啉和烯酰吗啉的吸附量分别为545和560 μg·g-1,略高于NIP。氟吗啉和烯酰吗啉的结构比较相近,吸附量也变化不大,再次证明MIP结构中形成的记忆空腔和识别位点只与烯肟菌胺分子相匹配,与氟吗啉和烯酰吗啉的分子结构不具有识别功能。
3 结 论
以烯肟菌胺为模板分子,采用溶胶-凝胶法制备了分子印迹聚合物,摸索出事宜的制备条件,通过吸附性能实验证明了MIP具有较强的吸附性,能够选择性吸附烯肟菌胺分子。实验将利用MIP的特异选择性吸附应用食品中烯肟菌胺残留的固相萃取。

