浩源核酸检测系统的性能确认
王艺芳,葛文超,李俊英,吕永磊,方建华
(河南省红十字血液中心,河南 郑州450012)
按照《血站实验室质量管理规范》[1]和《血站技术操作规程(2015 版)》[2]的要求,检测设备在正式投入使用之前应经过确认,核酸检测(nucleic acid test, NAT)设备还应进行分析灵敏度验证,实验室应建立血液检测试剂的评价、选择和确认程序。 因此,在核酸检测设备投入使用前,需要通过性能确认了解其性能,确认是否达到预期,满足实验室日常检测需要。 浩源核酸检测系统于2018 年7 月份引进本实验室,笔者通过通量测试、压力测试、灵敏度验证和平行试验等方面,完成对浩源核酸检测系统性能的评估,为其他实验室的核酸检测系统性能确认工作提供借鉴。
1 材料与方法
1.1 标本来源 选取2018 年08 月本中心采集的无偿献血者标本。 献血者均符合国家《献血者健康检查要求》中的相关要求。 采集每人份血液同时留取酶联免疫吸附试验(Enzyme Linked Immunosorbent Assay,ELISA)样管和NAT 样管,其中NAT 标本在采样后4h 内于2~8 ℃1760g 离心20 min,2~8℃保存,24h 内上机进行检测。
1.2 主要试剂、 仪器和NAT 试剂厂家 乙型肝炎病毒丙型肝炎病毒人类免疫缺陷病毒(1 型)核酸检测试剂盒(上海浩源生物科技有限公司, 批号:MF2 0180101);乙型肝炎病毒丙型肝炎病毒人类免疫缺陷病毒(1+2 型)核酸检测试剂盒(苏州华益美生物科技有限公司,批号:MA20180403 等)。 配套耗材均由试剂公司提供,均在有效期内使用。 核酸检测使用:ChiTaSBSS1200 核酸提取系统(美国PE公司),Hamilton Star 全自动混样仪(瑞士HAMILTON 公司),ABI 7500 实时荧光定量PCR 仪(美国ABI 公司),低温大容量离心机KUBOTA 8730(日本KUB OTA 公司)。
1.3 血清盘 北京康彻斯坦核酸系列血清评价盘(系统性能验证盘), 有36 份编号为P 系列样本,其中包括HIV-1 RNA、HCV RNA 和HBV DNA 及阴性的样本,见表1,进行8 人份混样检测。北京康彻斯坦核酸系列血清评价盘(分析灵敏度), 分别由WHO HBV DNA 标准品(10/26 4)稀释至9 IU/ml(6 个)、6 IU/ml(20 个)、3 IU/ml(6 个),WHO HCV RNA 标准品(06/102)稀释至36 IU/ml(6 个)、24 IU/ml(20 个)、12 IU/ml(6 个),WHO HIV RNA-1标准品(10/152)稀释至72 IU/ml(6 个)、48 IU/ml(20 个)、24 IU/ml(6 个),进行单人份检测。
1.4 方法
1.4.1 通量测试 14h 内连续进行两个批次的8 混检模式检测,每个批次均是满负荷,含质控品和样本。 所用样本为实验室当日检测过的样本,以验证在满负荷连续运行14h 内的检测量。
1.4.2 压力测试 使用浩源核酸检测系统进行8 混检模式检测,连续运行检测3d,共计检测样本2 232份(未包含质控品),观察并记录检测系统的满负荷的运行状况以验证在长时间运行时的系统稳定性。
1.4.3 分析灵敏度验证 使用浩源核酸检测系统对分析灵敏度血清评价盘进行单检模式检测,将HBV、HCV 和HIV-1 3 种病毒标准品随机分布进行检测, 并用IBM SPSS Statistics 19 分别分析其95%检出限。
1.4.4 平行试验 使用2018 年8 月6 日-11 日华益美检测过的样本进行检测。
1.4.5 抗交叉污染 使用13 个阴性血浆样本和53个阳性血浆样本 (含HBV、HCV、HIV 强阳性或弱阳性样本),交替放置8 混检模式检测。
1.4.6 检测能力验证 采用浩源核酸检测系统对康彻斯坦血清盘进行8 混检模式进行检测。
2 结果
2.1 通量测试 1 台浩源核酸检测系统在14h 内可以完成1 488 份样本的混样模式检测,运行过程中无故障发生。
2.2 压力测试 每天进行744 份样本混样模式检测,连续3d,模拟实际运行过程中最大的检测压力,在满负荷状态下连续运行3d,无故障和无效结果。
2.3 分析灵敏度验证 分析灵敏度验证的结果见表2,单人份检测HBV DNA 95%检出限为6.00 IU/ml,HCV RNA 95%检 出 限 为24.00 IU/ml,HIV RNA-1 95%检出限为48.00 IU/ml。
2.4 平行试验 使用华益美检测过的样本进行检测,有1 个pool 浩源混检阳性而华益美混检阴性,拆分阴性,其他结果均一致。
2.5 抗交叉污染 66 个样本试验,53 个阳性样本均检测为有反应性,13 个阴性样本均为无反应性。阳性孔均未对邻近孔位造成交叉污染。
2.6 检测能力验证 对康彻斯坦血清盘进行8 混检模式进行检测,检测结果与血清盘说明书参考结果符合度100%。 见表1。
3 讨论
病毒核酸检测技术是直接检测病原体核酸的一系列技术的总称。 相比酶联免疫检测方法,血液病毒核酸检测技术可以有效缩短抗原抗体免疫检测的“窗口期”,从而大大降低经输血传播病毒的风险[3-6]。 目前全国血站核酸检测工作已逐步在各地区普及[7],更多的实验室关注核酸检测的质量更加注重核酸检测系统性能确认工作。 国际输血协会(International Society Blood Transfusion,ISBT)指出安装确认(IQ)、运行确认(OQ)、性能确认(PQ)是设备确认的3 个连续阶段,并对具体操作进行了说明[8]。 本实验室在实施性能确认前对安装调试完毕的浩源核酸系统的设备已进行评估,确保设备硬件和软件的正确安装,设备在可要求的范围内正确运行。 目前,全自动NAT 仪器这样的大型仪器IQ和OQ 通常由厂商的工程技术人员进行,而PQ 则需实验室的设备使用人员来完成[9]。
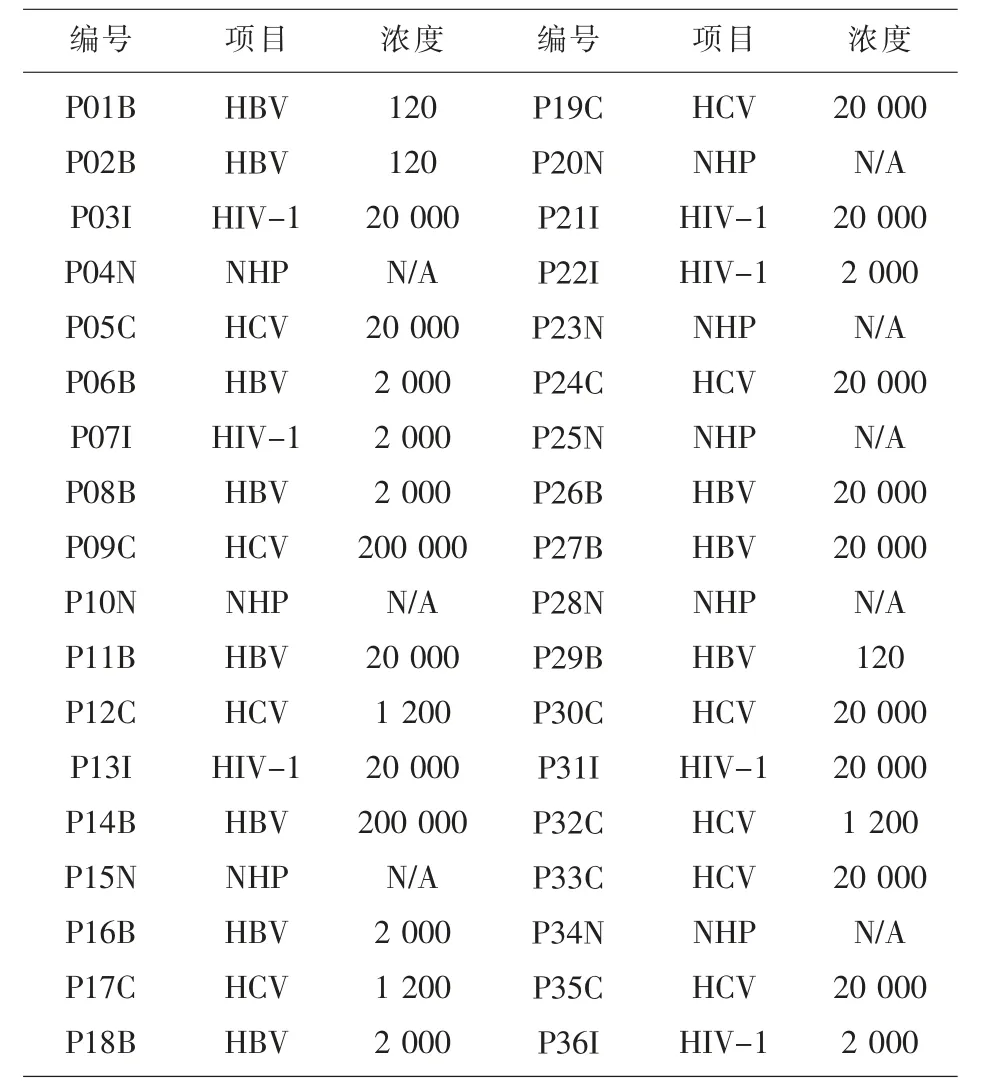
表1 36 份编号为P 系列样本背景清单
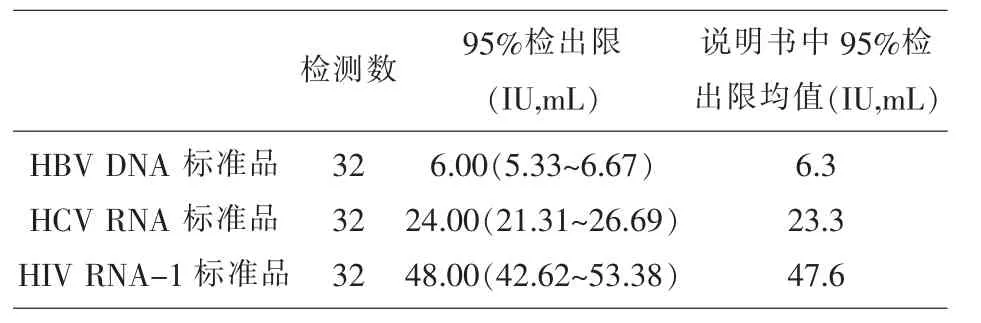
表2 浩源核酸检测系统对WHO 标准品分析灵敏度的验证结果
通过验证操作性能(通量测试和压力测试)和检测性能(灵敏度验证、平行试验、抗交叉污染和检测能力)两个方面[10],设计确认方案完成对浩源核酸检测系统性能的评估。 通量测试是实验室对浩源核酸检测系统检测量和检测时间有一个预估计,14h 内可完成1 488 份样本的8 混检模式检测,为今后日常检测合理安排工作提供依据。 使用浩源核酸检测系统进行8 混检模式检测,由于平常实验室检测量较大,在压力测试测评价中模拟实际运行过程中最大的检测压力,并连续检测,以此验证了检测系统的满负荷运行状况以在长时间运行时的系统稳定性。 灵敏度验证方面,参考ELISA 弱阳性质控品来监控试验的有效性和稳定性[11],监控系统的趋势变化。按照规程要求,结合NAT 自身特点和灵敏度血清盘结果, 笔者认为选择最低检测限0.5~2 倍检出限的NAT 标准品作为分析灵敏度验证的阳性样本,其病毒含量明确,一致性较好,相对于日常检测的血液样本,更适用于新仪器的灵敏度检测确认。 由表2 可知,分析灵敏度验证HBV DN A、HCV RNA 和HIV RNA-1 95%检出限为分别为6.00 IU/ml、24.00 IU/ml、48.00 IU/ml, 这与试剂说明书基本相符。 平行试验评价采用另外一套系统当日检测过的样本进行检测, 仅有1 个pool 混检阳性,经拆分后为阴性,并在前一套系统内重复检测,均为阴性。 分析原因:可能由于检测方案、灵敏度的不同,出现了检测结果的差异。由于NAT 防污染是必须重视的1 个问题[12],实验室在进行抗交叉污染评价之前,首先进行了防污染监控确认,确保实验室环境、设备无污染。 其次将阳性(含HBV、HCV、HIV 强阳性或弱阳性样本) 和阴性样本混合交叉排列进行交叉污染的评估,可以有效的验证仪器在汇集、 提取和扩增过程中对待测样本的处理是否存在交叉污染[13],便于日后出现多孔位反应性时,排除系统原因,分析污染原因。 系统性能验证血清盘是一组含有阴性、强阳性、弱阳性样本以及常见基因型样本,通过混样检测,对检测系统的准确性、基因型覆盖面、弱阳性样本的检测能力、防交叉污染能力等方面进行综合评价, 其检测性能符合实验室日常检测要求。
通过性能确认,我们对浩源核酸检测系统的综合性能有了全面的了解,其操作性能和检测性能基本符合实验室日常检测要求。 同时,根据实验室日常的检测量和检测成本,在设计核酸检测系统的确认方案时,除考虑满足法律法规外,还应参加NAT室间质评实验室能力评价活动,作为性能确认工作的补充,并对这一系列确认活动形成确认报告。

