超高效液相色谱-串联质谱法同时测定环境水体中3种典型“三高”药物残留
陈泽雄 周志洪 巫陪山 马艳芳
(1.广州市环境监测中心站,广州,510030;2.广东省科学院,中国广州分析测试中心,广东省化学危害应急检测技术重点实验室,广州,510070)
近年来,随着生活水平的提高,我国居民慢性疾病高血压、高血糖、高血脂(俗称“三高”)的发病率也呈增长趋势。最新的《中国心血管病报告2018》显示,中国成人高血压、血脂异常和糖尿病标化患病率分别为27.9%、40.4%和10.9%;治疗率分别为45.8%、19.5%和32.2%[1]。这3种疾病构成了代谢综合征的主体,其患病率随着患者年龄增长而升高[2]。“三高”人群往往需要根据自身病情,选用合适的药物,并长期服用以维持病情稳定,其中,硝苯地平、格列吡嗪和吉非罗齐作为降压药、降糖药和降脂药使用广泛[3,4]。药物使用以后不能完全被人体吸收,一部分随患者排泄物进入污水处理系统,从而进入环境水体[5],并对各级水生生物造成生物毒性效应[6]。研究表明,硝苯地平(10 μM)可诱导欧洲湖蛙(Pelophylax ridibundus)体内氧自由基产生,增加谷胱甘肽和氧化谷胱甘肽浓度,并导致超氧化歧化酶活性升高[7];吉非罗齐对大型蚤(Daphnia magna)的无效应观察浓度为30 μM[8],环境相关浓度的吉非罗齐(1.5 μg/L)能对鲷鱼(Sparus aurata)造成明显的基因损伤[9]。
环境水体来源广泛,组成复杂,包含多种药物活性物质,前期研究表明,环境水体中的多种药物活性成分协同作用下,往往对水生生物存在更强的毒性效应[10,11]。前期有学者分别调查了硝苯地平、格列吡嗪和吉非罗齐在环境水体中的含量,结果表明,硝苯地平在地表水和污水处理厂污水中均有检出[12,13];格列吡嗪在中国胶州湾海水中广泛检出,检出率达58%[14];吉非罗齐在地表水、污水处理厂污水中均广泛检出,含量可达45.2 μg/L[15-17]。然而,同时监测环境水体中3种典型“三高”药物硝苯地平、格列吡嗪和吉非罗齐含量的研究鲜有报道。“三高”症状人群需要长期同时服用降压药、降糖药和降脂药以控制病情,其中,一部分未被患者完全吸收代谢的药物能够随生活污水持续排入环境中。此外,药物代谢物的转化产物以及制药厂出水中未处理完全的药物均可通过城市污水管网进入受纳环境。由于环境水体中药物残留来源广泛,并对生态环境造成持续影响。因此,有必要开发灵敏、可靠的分析方法,用于同步筛查环境水体中典型“三高”药物硝苯地平、格列吡嗪和吉非罗齐的含量,为评估其环境生态风险提供方法保证。
1 实验方法
1.1 仪器、试剂与材料
安捷伦1290系列超高效液相色谱-6470系列三重四级杆串联质谱联用仪(UPLC-MS/MS,美国,Agilent);EFAA-DC24-RT系列24孔平行氮吹仪(中国,安谱);SBEQ-CG1824系列固相萃取装置(中国,安谱)。
ENVI-Carb固相萃取柱(500 mg,6 mL)、MCX固相萃取柱(500 mg,6 mL)、MAX固相萃取柱(500 mg,6 mL)、HLB固相萃取柱(500 mg,6 mL)购自美国Waters公司;GF/F玻璃纤维滤膜(0.7 μm)购自英国Whatman公司;有机相滤头购自中国安谱公司。
硝苯地平标准品购自加拿大TRC公司;格列吡嗪标准品购自中国源叶公司;吉非罗齐标准品购自德国Dr.Ehrenstorfer公司;同位素标记标准品奈韦拉平-d3、苯扎贝特-d4、吉非罗齐-d6购自加拿大TRC公司,其纯度均高于95%。色谱纯乙腈、乙酸乙酯、二氯甲烷、甲醇、正己烷购自德国Merk公司;色谱纯乙酸铵、甲酸购自德国CNW公司;分析纯硫酸、氨水购自中国科密欧公司;实验用水为屈臣氏蒸馏水。所有标准品均采用甲醇配制成100 mg/L的标准储备溶液,通过逐级稀释标准储备溶液获得不同浓度的标准工作溶液,标准储备溶液及标准工作溶液均置于-20 ℃避光保存。
1.2 样品采集
地表水样品从流溪河水库采集,流溪河水库位于广州市从化区东北部(23°45′N,113°46′E),水库水面面积约为13 km2,整个流域水土状况保持良好,人类活动影响小。污水处理厂样品从广州市南沙污水厂采集,南沙污水厂服务人口30万,日进水量约8万吨。地表水和污水处理厂污水均采用1 L棕色玻璃瓶采集,样品采集后立即加入50 mL甲醇抑制微生物活动,采用冷藏恒温箱尽快运回实验室,并于48 h内完成样品前处理。
1.3 样品前处理
采用GF/F玻璃纤维滤膜(0.7 μm)过滤以去除水样中的悬浮颗粒物,然后向水样中加入100 ng(1 mg/L,100 μL)的混合同位素标记标准品作为内标,并混合均匀。采用HLB固相萃取柱(500 mg,6 mL),通过固相萃取法提取3种目标药物。首先,依次采用10 mL甲醇、10 mL超纯水活化HLB小柱,随后以5~10 mL/min的流速加载水样,并始终保持液面高于HLB小柱填料表面。样品加载完毕后,用20 mL甲醇/水溶液(v/v=5∶95)润洗样品瓶2次,并过柱。
抽真空2 h以去除小柱中残留的水分。小柱干燥后,分别用4 mL甲醇、3 mL二氯甲烷和3 mL乙酸乙酯洗脱富集在小柱填料上的目标药物,收集洗脱液,采用氮气缓慢地将洗脱液浓缩至近干,用1 mL甲醇定容浓缩液,并转移到1 mL棕色进样小瓶,置于-20 ℃冰箱避光保存用于后续分析。分析前,取100 μL待测样品溶液,用氮气缓慢浓缩至近干,用含5 mmol/L乙酸铵的甲酸(体积分数0.2%)水溶液与甲醇的混合溶液(v/v=1∶4)重新溶解,定容至100 μL,待测。
1.4 仪器分析
样品提取液采用UPLC-MS/MS进行分析,色谱柱为Agilent ZORBAX Eclipse Plus C18柱(50 mm×2.1 mm,1.8 μm),色谱柱前端接0.22 μm在线过滤器,用于去除流动相和样品中的微小颗粒物。色谱分离后,样品通过电喷雾离子源(ESI)雾化,随后进入质谱检测器,进样量为2 μL。目标药物均在多重反应模式(MRM)下进行分析。
硝苯地平和格列吡嗪采用ESI+模式监测,柱温箱温度为40 ℃;流动相为缓冲溶液A(含5 mmol/L乙酸铵和0.2%甲酸的水溶液)和B甲醇,流动相流速为0.3 mL/min,总运行时间6.5 min;梯度洗脱程序为:0 min,20% B;0.5 min,25% B;1.5 min,35% B;2.5 min,45% B;3 min,55% B;6.5 min,85% B。干燥气流速为8 L/min,温度为350℃;雾化器压力为45 psi;鞘气温度为350 ℃,流速为12 L/min;喷嘴电压为500 V;毛细管电压为3500 V。
吉非罗齐采用ESI-模式监测,柱温箱温度为35 ℃;流动相为A纯水溶液和B甲醇,流动相流速为0.32 mL/min,总运行时间5 min。梯度洗脱程序为:0 min,10% B;1.5 min,55% B;2.5 min,70% B;3.8 min,88% B;4.8 min,93% B;5 min,97% B。干燥气流速为11 L/min,温度为280 ℃;雾化器压力为50 psi;鞘气温度为350 ℃,流速为11 L/min;喷嘴电压为2000 V;毛细管电压为3500 V。3种目标药物的UPLC-MS/MS分析参数如表1所示。
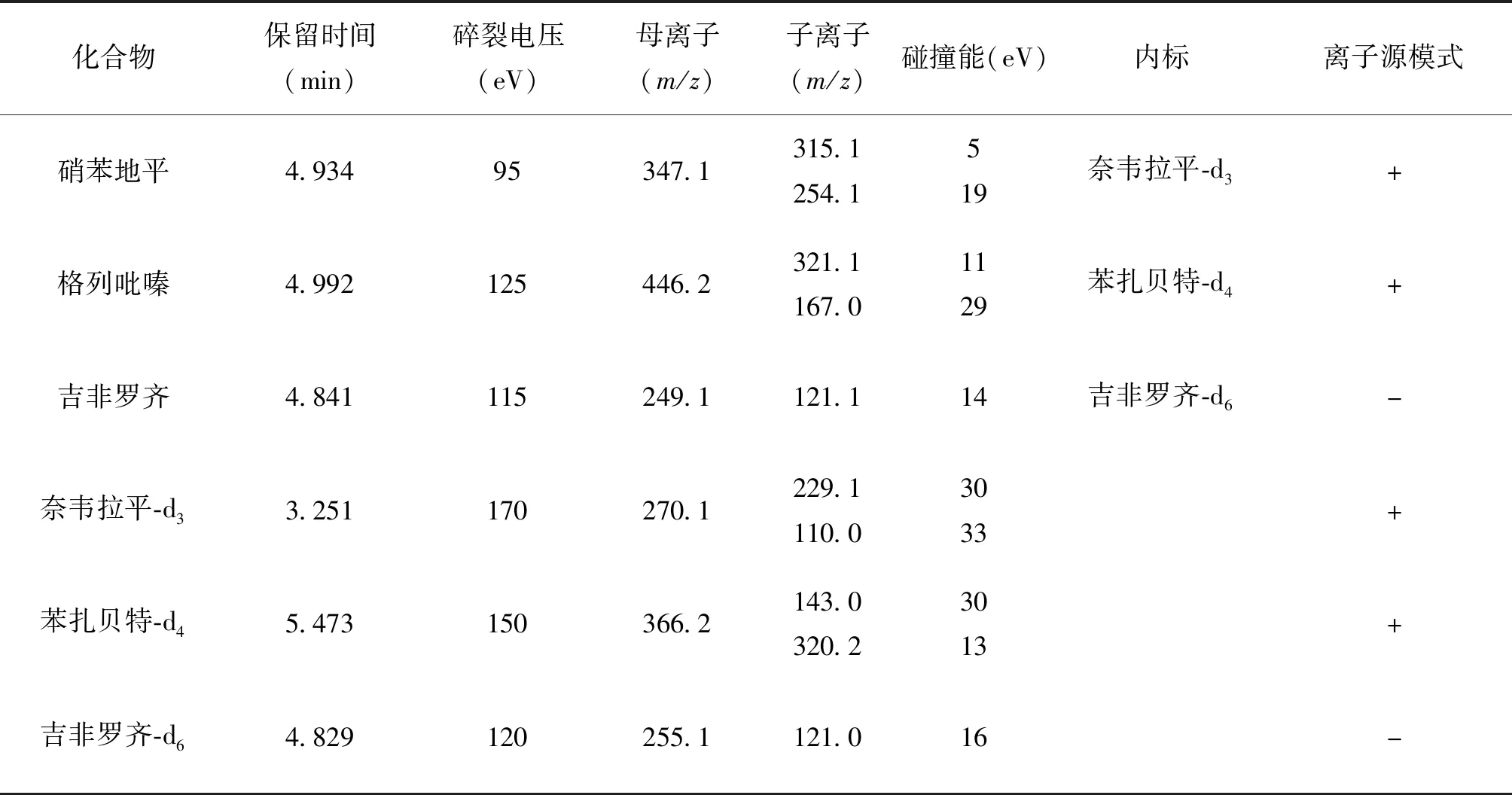
表1 3种目标药物的超高效液相色谱-质谱分析参数
2 结果与讨论
2.1 前处理方法优化
2.1.1固相萃取柱选择
为了获得最佳的富集和净化效果,需要根据目标化合物性质选择合适的固相萃取小柱类型。本研究考察了4种不同填料的固相萃取小柱对3种目标药物回收率的影响:a)石墨化炭黑吸附柱ENVI-Carb;b)阳离子交换柱MCX;c)阴离子交换柱MAX;d)聚合物反相柱HLB。其中,ENVI-Carb柱无键合相,常用于极性和非极性化合物的吸附萃取[18];MCX柱是弱阳离子交换柱,常用于提取弱碱性化合物[19];MAX柱是弱阴离子交换柱,常用于提取弱酸性化合物[20];HLB柱由亲脂性二乙烯苯和亲水性N-乙烯基吡咯烷酮聚合而成,对酸碱性和极性不同的化合物均有较好的提取效果[19]。4种不同填料固相萃取小柱对目标药物的提取效率如图1所示,3种目标药物在ENVI-Carb柱、MCX柱、MAX柱和HLB柱中的加标回收率范围分别为2%~153%、76%~122%、75%~165%和91%~133%。总体而言,MCX柱和HLB柱对3种目标药物均表现出较好的提取效果。硝苯地平在ENVI-Carb柱中的保留效果很差,其加标回收率低至2%。格列吡嗪在ENVI-Carb柱和MAX柱中的加标回收率均高于120%,这与其内标化合物Benzafibrate-d4的提取效率偏低有关。由于MCX柱的价格较昂贵,综合考虑目标化合物提取效率和固相萃取小柱价格因素,最终选择采用HLB柱提取目标药物。
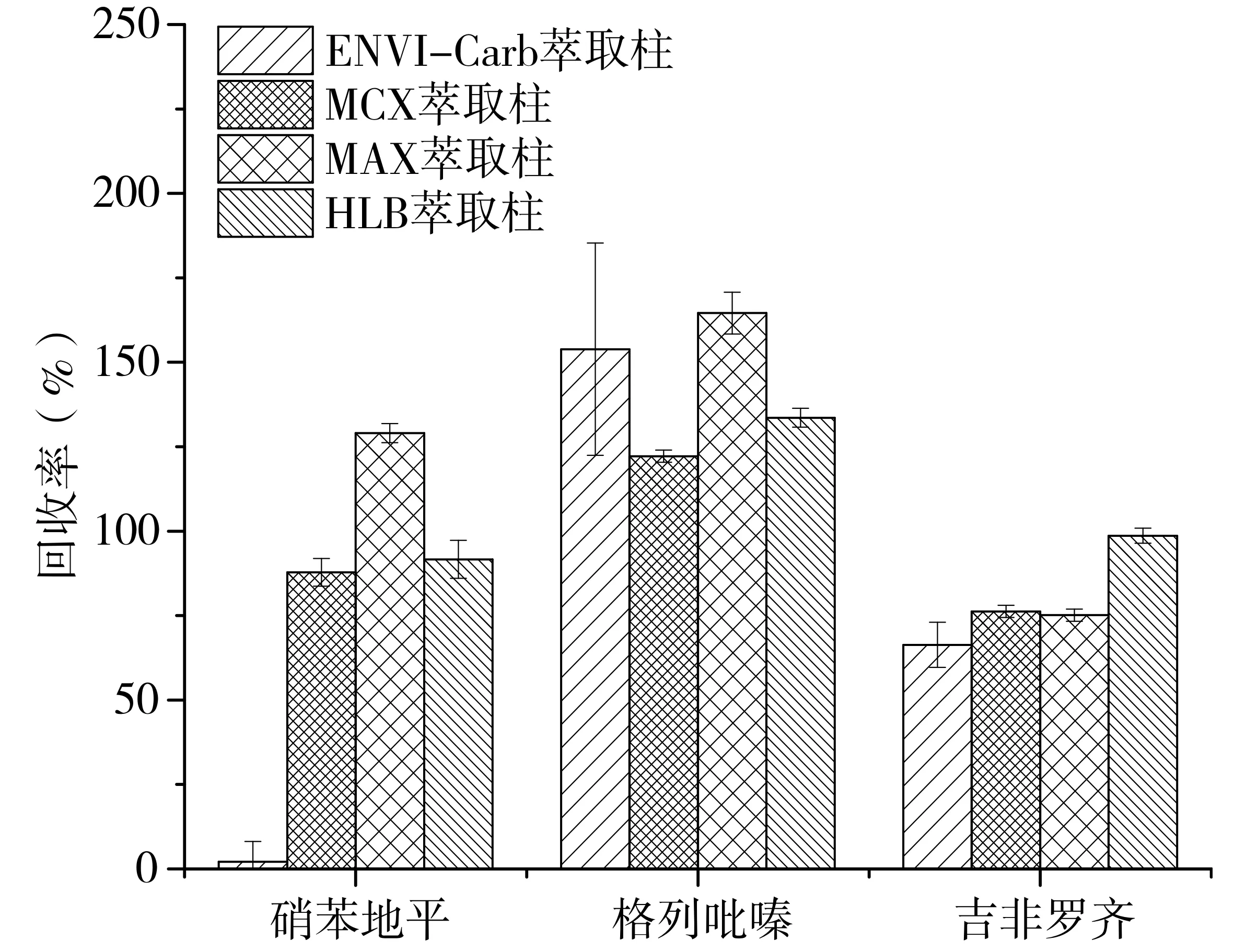
图1 不同固相萃取小柱对3种目标药物回收率的影响
2.1.2样品pH条件选择
样品pH条件能够影响化合物在水中的存在形态,从而影响化合物的萃取效率[21]。通过调研文献可知,3种目标药物硝苯地平、格列吡嗪和吉非罗齐的酸解离常数(pKa值)分别为3.93、5.2和4.75[22-24]。采集的环境水体样品pH值为6.8,本实验通过向样品中分别加入硫酸溶液(4 mol/L)和氨水溶液(5%)调节样品pH值,研究了酸性(pH=3)、中性(pH=6.8)和碱性(pH=10)条件下,HLB柱对目标药物的提取效率(图2)。如图所示,酸性(pH=3)、中性(pH=6.8)和碱性(pH=10)条件下,3种目标药物的加标回收率范围分别为88%~191%、84%~128%和79%~124%。总体而言,中性条件(pH=6.8)和碱性条件(pH=10)下,HLB柱对3种目标药物均表现出较好的萃取效果;酸性条件(pH=3)下,由于格列吡嗪的内标化合物Benzafibrate-d4回收率较低,导致格列吡嗪的回收率过高。由结果可知,相比保持样品中性pH条件,将样品pH值调为碱性对3种目标药物的回收率没有明显提高,为了减少实验操作步骤,最终选择中性条件(pH=6.8)下萃取目标药物。

图2 不同pH值对3种目标药物回收率的影响
2.1.3洗脱溶剂选择
硝苯地平、格列吡嗪和吉非罗齐在固相萃取过程中的洗脱溶剂一般为甲醇和乙腈[25-27],本研究考察了不同极性有机溶剂乙腈、甲醇、乙酸乙酯、二氯甲烷和正己烷对目标药物的洗脱效果,结果如图3所示。由图可知,4种不同溶剂洗脱条件下,目标药物均具有较好的洗脱效果,其加标回收率范围分别为79%~113%、78%~113%、75%~115%和79%~110%,说明洗脱溶剂极性对3种目标药物的洗脱效果影响较小。最终,选择逐步加入甲醇、二氯甲烷、乙酸乙酯洗脱目标药物。
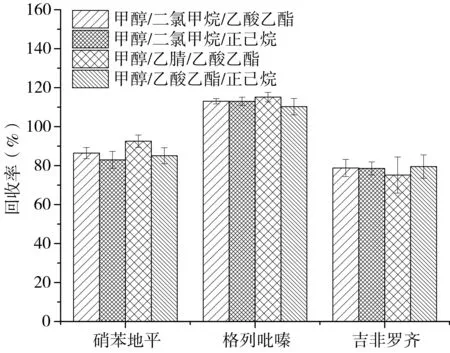
图3 不同提取溶剂对3种目标药物回收率的影响
2.2 方法验证
2.2.1加标回收率及相对标准偏差
采用优化后的提取方法,分别向流溪河水库的地表水样品和南沙污水处理厂的污水样品中加入低、中、高3个浓度的标准溶液,每个浓度平行测定3次,对优化后的方法进行评价。结果如表2所示.加标浓度为5 ng/L、20 ng/L和200 ng/L的地表水样品中,硝苯地平、格列吡嗪和吉非罗齐的回收率范围分别为95%~103%、111%~126%和91%~98%,平行样相对标准偏差(RSD)范围为1%~26%;加标浓度为100 ng/L、500 ng/L和1000 ng/L的污水样品中,硝苯地平、格列吡嗪和吉非罗齐的回收率范围分别为71%~80%、87%~113%和105%~112%,RSD范围为1%~28%。总体而言,目标药物在不同加标浓度的样品基质中回收率均在70%~130%范围,RSD均<30%,所建立的方法能满足环境样品中3种目标药物的分析要求。

表2 3种目标药物的加标回收率和相对标准偏差(RSD)(n=3)
2.2.2线性范围、基质效应及定量下限
采用优化后的提取方法分别提取流溪河水库地表水样品和南沙污水处理厂污水样品,获得2种样品基质提取液,分别向2种基质提取液和空白甲醇/水(含5 mmol/L乙酸铵和0.2%甲酸)(v/v=1∶4)溶液中加入3种目标药物的混合标准溶液,获得系列浓度分别为2 μg/L、5 μg/L、10 μg/L、50 μg/L、100 μg/L、200 μg/L、500 μg/L和2000 μg/L的混合基质标准曲线和空白标准曲线(内标浓度均为100 μg/L)。系列曲线溶液在选定的色谱分离和质谱检测参数下,采用UPLC-MS/MS进行检测,使用分析仪器匹配的MassHunter软件进行分析,以目标药物的归一化相对响应值(Y)为纵坐标,归一化相对浓度(X)为横坐标,得到3种目标药物的线性方程及相关系数(表3)。由表可知,在环境基质样品提取液及空白溶液中,3种目标药物在2 μg/L~2000 μg/L的浓度范围内均具有良好的线性关系,线性相关系数r2为0.9989~0.9999。
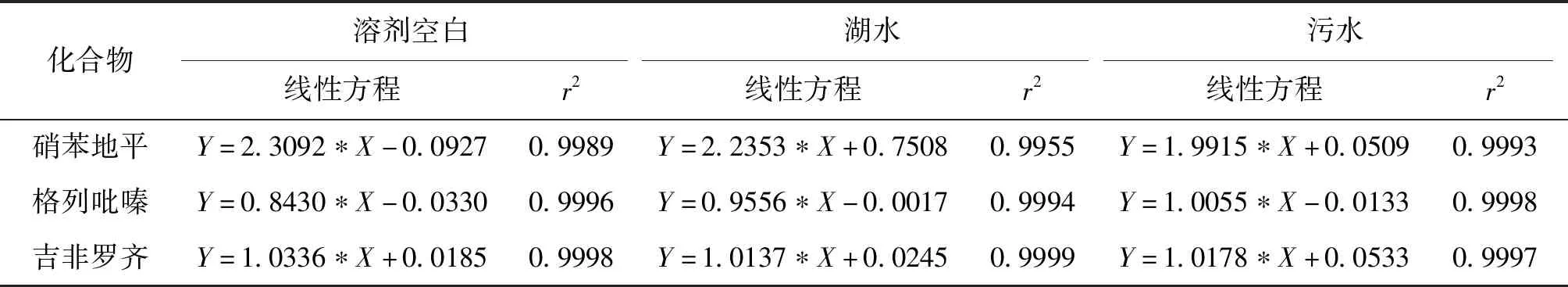
表3 3种目标药物在不同标准溶液曲线中的线性方程和相关系数
根据基质标准曲线和空白标准曲线的线性方程斜率,可进一步计算目标药物在地表水和污水样品中的基质效应,计算公式为[28]:
其中,α值为基质效应(%);Smatrix为基质标准曲线线性方程斜率;Sblank为空白标准曲线线性方程斜率,α>0,说明存在基质增强效应;α<0,说明存在基质抑制效应;α绝对值越大,说明基质效应越明显[28, 29]。如表4所示,硝苯地平和吉非罗齐在地表水和污水处理厂污水中主要存在基质抑制效应,格列吡嗪在地表水和污水处理厂污水中主要存在基质增强效应。总体上,3种目标药物在水库地表水和污水处理厂污水中的基质效应在±20%范围内,其基质效应范围分别为-3.2%~13%和-14%~19%。相比水库地表水,目标药物在污水处理厂样品中受基质效应影响更大,这可能与污水处理厂污水成分复杂有关[30]。
向水库地表水和污水处理厂污水样品中分别添加目标物浓度为5 ng/L和100 ng/L的混合标准溶液,按照色谱峰高信噪比大于3(S/N>3)计算获得物质检出限(MDLs),按照色谱峰高信噪比大于10(S/N>10)计算获得物质检测限(MQLs)。如表4所示,水库地表水中3种目标药物的MDLs范围为0.04ng/L~0.24ng/L,MQLs范围为0.13ng/L~0.79 ng/L;污水处理厂污水中3种目标药物的MDLs范围为1.00 ng/L ~1.89 ng/L,MQLs范围为3.35ng/L ~6.32ng/L,相比地表水,污水来源广泛,成分复杂,目标物在污水中的检测限较高。总体上,3种目标药物在地表水的MQLs均<1 ng/L,其中,硝苯地平的MQLs低于Varga等人报道的15 ng/L[31];吉非罗齐的MQLs与Tran等人报道的0.4 ng/L相当[32]。3种目标药物在污水处理厂污水中MQLs均<10 ng/L。硝苯地平的MQLs低于王钊等人报道的107 μg/L[25];吉非罗齐的MQLs低于Abou-Elwafa Abdallah和王钊等人报道的14.5 ng/L和52.7 μg/L[25, 33]。
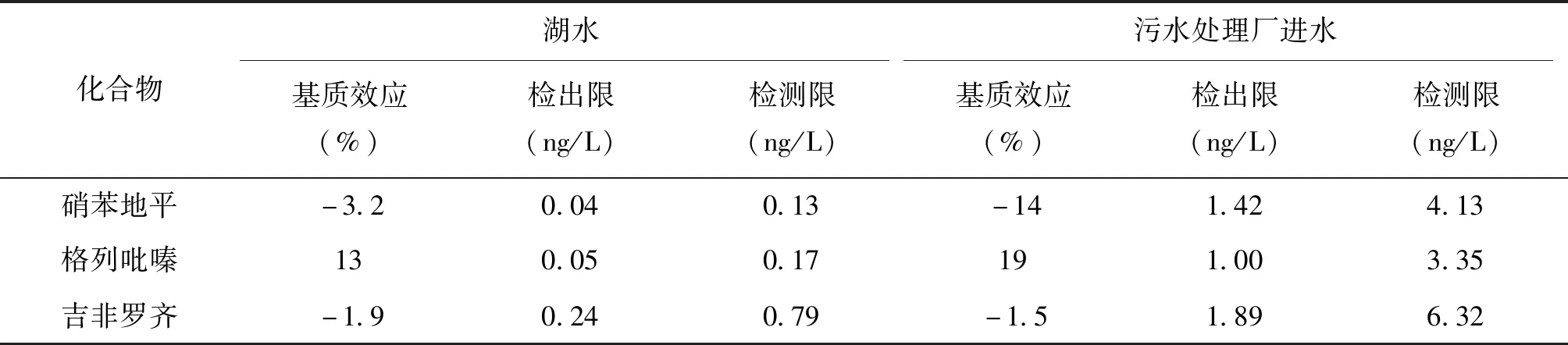
表4 3种目标药物在环境样品中的基质效应,检出限及检测限
2.3 方法应用
采用本实验建立的提取-分析方法,对来源于流溪河水库的地表水和南沙污水处理厂的污水进行检测,每种环境样品做3个份平行样。结果显示,目标药物硝苯地平、格列吡嗪和吉非罗齐在3份地表水平行样中均未检出,说明该水库受人类活动影响较小;硝苯地平在3份污水平行样中均有检出,其平均浓度为8.7 ng/L;格列吡嗪和吉非罗齐在污水中未检出,这可能与硝苯地平作为降血压药使用量较大有关。
3 结论
建立了环境水体中典型“三高”药物硝苯地平、格列吡嗪和吉非罗齐的提取、分析方法,通过探讨固相萃取条件对“三高”药物提取效率的影响,优化了提取方法,并对方法准确度、灵敏度及基质效应进行了验证。所开发的方法用于检测环境水体中典型“三高”药物硝苯地平、格列吡嗪和吉非罗齐具有良好的回收率(70%~130%)、较弱的基质效应(±20%)和较低的检测限(<10 ng/L)。本方法灵敏可靠,可同时筛查和检测环境水体中痕量的典型“三高”药物。

