症状型与非症状型腹主动脉瘤形态学数据的分析
苏志向,郭建明,郭连瑞,崔世军,吴英锋,佟铸,刘一人,魏立春,张建,谷涌泉
(首都医科大学宣武医院血管外科 首都医科大学血管外科研究所,北京 100053)
腹主动脉瘤(abdominal aortic aneurysm,AAA)在人群中的发病率约为5%,当瘤体破裂时具有生命危险[1]。依据其是否有相关的症状表现,主要指动脉瘤相关的腹痛及背部疼痛,可分为症状型腹主动脉瘤(symptomatic abdominal aortic aneurysm,sAAA)和非症状型腹主动脉瘤(asymptomatic abdominal aortic aneurysm,aAAA),其中症状型腹主动脉瘤较为少见,约占5%~22%[2],通常,伴有症状是腹主动脉瘤破裂的先兆,常需急诊修复[3],相对于非症状型腹主动脉瘤来说,症状型腹主动脉瘤病人的短期及长期生存期都相对较短[4]。对于男性病人来说瘤体直径大于5.5 cm,而女性瘤体的最大直径大于5.0 cm是具有手术干预的指征[5],因此以腹主动脉瘤瘤体的最大直径对于判定动脉瘤的破裂风险是有一定意义的,然而在临床中有一些瘤体直径较小的AAA也存在破裂的情况,而一些瘤体直径较大的AAA却能保持相对稳定的情况[6-7],可见单以AAA的最大直径去判定AAA的破裂风险是相对局限的,目前临床上术前对于AAA的评估主要依据腹部CT血管造影(CTA),获得直观的形态学表现,主要的形态学数据为瘤体的最大直径、瘤颈的长度、瘤颈的角度等相关数据,为了更好地对AAA的破裂风险进行评估,本研究旨在探究sAAA与aAAA形态学相关数据的差异性及相关的联系。
资料与方法
一、临床资料
于我中心2013年1月至2019年1月被诊断为肾下型腹主动脉瘤的病人纳入该研究,主要依据腹部CTA进行诊断。破裂型腹主动脉瘤,感染性腹主动脉瘤被排除在外。伴有腹部和(或)背部疼痛的的病人,且排除由动脉瘤继发性血栓,动脉内膜撕裂及其他原因引起的,可定义为sAAA,若不伴有腹部或者背部疼痛的病人可定义为aAAA。数据收集来源于我中心数据库,主要收集病人的一般资料,既往病史(高血压、糖尿病、心血管病、脑血管病),吸烟史,主要形态学数据,包括腹主动脉瘤最大直径,瘤颈长度,瘤颈角度,瘤体形态,术前的CTA图像对病人进行了二维的处理和三维的重建,瘤颈的测量是瘤体近端与较低肾动脉的距离,瘤颈角度的测量是瘤颈角度的中轴线与腹主动脉主干中轴线的夹角,3人测量后取平均值(主要来源于我中心腹部CTA)。
二、统计学方法
结 果
共有107例病人纳入研究,sAAA组27例,aAAA组80例,两组病人的临床基线资料:年龄、性别、既往病史、吸烟史等方面差异无统计学意义(表1)。
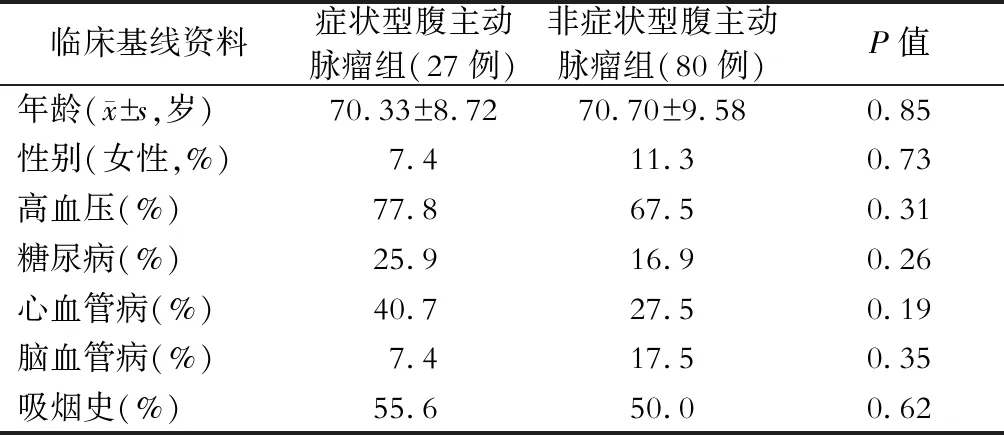
表1 病人的临床基线资料
通过统计分析,sAAA组的瘤体最大直径大于aAAA组,且差异有统计学意义;瘤颈长度及瘤颈角度,两组之间差异无统计学意义。偏心性动脉瘤在sAAA组的比例相对较高,且差异有统计学意义(51.9%比30.0%,P=0.040)(表2)。通过绘制散点图,可直观发现瘤颈长度与瘤体最大直径存在负相关关系,而瘤颈角度与瘤体最大直径存在正相关关系(图1、图2)。通过Spearman相关分析,结果显示瘤颈长度与瘤体的最大直径存在负相关关系(r=-0.36,P<0.01),瘤颈的角度与瘤体的最大直径之间存在正相关关系(r=0.258,P=0.007)(表3)。
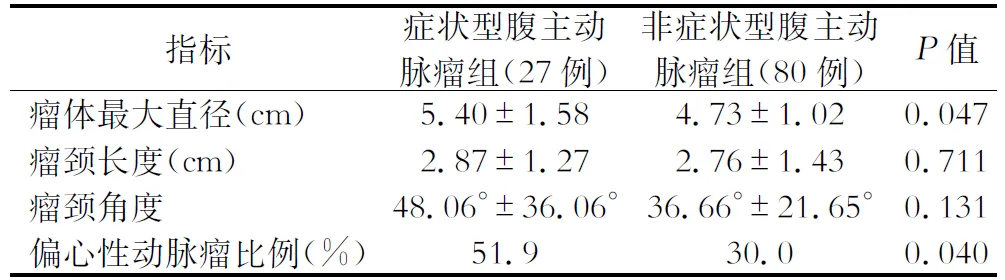
表2 形态学数据

表3 瘤颈长度及瘤颈角度与瘤体最大直径的相关关系
讨 论
sAAA常会表现出腹部或背部疼痛的症状,而这些症状的出现常与腹主动脉瘤的破裂风险有关,目前来说,在临床上腹主动脉瘤的最大直径常被用来判断腹主动脉瘤的破裂风险,一般来说,最大直径为4.0~5.5 cm的小动脉瘤相对安全,而对于最大直径大于5.5 cm的腹主动脉瘤以及快速扩张的腹主动脉瘤(半年来扩张超过0.5 cm或1年来扩张超过1.0 cm),是具有破裂的风险的[6]。通常,腹主动脉瘤的最大直径大于5.5 cm是需要行手术干预的,然而有证据表明,有最大直径小于5.5 cm的腹主动脉瘤仍会出现破裂[8],表明腹主动脉瘤的破裂风险不能只依据腹主动脉瘤的最大直径来判断。本研究也证实部分sAAA的瘤体最大直径小于5.5 cm,也存在aAAA的病人的瘤体最大直径大于5.5 cm,但sAAA与aAAA的瘤体最大直径差异有统计学意义 [(5.40±1.58) cm 比(4.73±1.02) cm,P=0.047],可见瘤体的最大直径对预测腹主动脉瘤的破裂风险有一定意义,但不是唯一指标。
近年来,有报道通过生物动力学分析的方法来预测腹主动脉瘤的破裂风险,即采用限定元分析的方法(finite elements analysis,FEA),其最初是用于工程学及建筑学领域,近年来逐渐用于医学领域,其主要利用CTA的数据进行腹主动脉瘤的三维几何图形的重建,结合来自生物动力学试验的数据来计算每个腹主动脉瘤的血管壁压力,从而获取血管壁峰值压力(peak wall stress, PWS)这样的生物动力学数据,亦可获取关于腹主动脉瘤腔、腔内血栓、直径、体积等相关的几何变量的数据[9]。在较早期就有研究PWS在预测腹主动脉瘤破裂风险的价值,发现PWS值在破裂或者sAAA中明显高于aAAA[10]。Soto等[11]研究表明,当腹主动脉瘤的PWS值大于305.15 kPa时有较高的破裂风险,当其小于305.15 kPa时,其破裂的风险较小,但是在临床上用该值去预测腹主动脉瘤的风险还需要更加深入的研究,一方面需要对aAAA进行长期随访,观测其发展为sAAA后PWS的变化,另一方面需要加大样本量使研究更加可信。除了PWS这样的血流动力学的数据,也有研究指出PWS与瘤体最大直径的比值,即直径标准化的血管峰值压力(diameter normalised PWS,dnPWS)这样的生物力学数据才能更好地区分症状型及非症状型腹主动脉瘤,特别是在腹主动脉瘤的最大直径大于6.5 cm时[12]。
血流动力学数据的产生与腹主动脉瘤的几何学结构是密切相关的,有研究表明短瘤颈的腹主动脉瘤具有较高的破裂风险[13],较短瘤颈的腹主动脉瘤相对腔内血栓的体积(腔内血栓的体积与动脉瘤总体积的比值)较大[14],因为腔内血栓的存在影响了腹主动脉瘤壁血流动力学的活动及瘤壁压力的分布,这会影响腹主动脉瘤的破裂风险[15]。国内也有研究指出腹主动脉瘤的不同形态会对瘤体的血流动力学产生影响,特别是瘤体的内流场特征[16]。在本研究中,腹主动脉瘤的瘤颈长度和腹主动脉瘤的瘤体最大直径呈负相关,瘤颈角度与腹主动脉瘤最大直径呈正相关,因而腹主动脉瘤形态学变量之间也是彼此联系,相互影响的,而早期国内有研究也得出相同的结论[17-18]。为了更好地对腹主动脉瘤破裂风险进行预测,有研究就利用计算机算法(machine learning algorithms,MLA) 对腹主动脉瘤的风险预测,其主要结合病人的人口学数据、瘤体的几何数据、瘤体的血流动力学数据进行分析,使对腹主动脉瘤破裂风险的预测更加准确,而关于MLA的模型有多种,其最好的准确率可达87%,是目前较高的预测方法[19]。
除了从血流动力学的方向分析腹主动脉瘤破裂风险,也可以从病理生理学的角度分析腹主动脉瘤的进一步发展。炎性反应、氧化应激在腹主动脉瘤的发病过程中具有重要的作用[20]。腹主动脉瘤的血管壁主要以内侧血管的新生、炎性细胞(主要为巨噬细胞和淋巴细胞)的渗透,以及细胞外基质的胶原蛋和弹力蛋白的纤维断裂为主要特点。而炎症细胞在腹主动脉瘤的进展过程中具有重要的作用,并且有研究应用PET-CT的核素显像技术证实动脉瘤发生时白细胞在动脉外膜的聚集及C反应蛋白的循环[21]。但对于腹主动脉瘤中较高水平核素聚集的是否对应较大的PWS值,目前仍有较多争论[22],有研究通过带有超微超顺磁性氧化铁的核磁共振去判定腹主动脉瘤的炎性反应,发现瘤壁的压力值与超微超顺磁性氧化铁的摄取程度(代表炎性反应程度)无明显关系,其认为瘤壁的炎性反应和血管壁的压力可能在腹主动脉瘤的进展过程中代表不同但相互补充的阶段[23]。因而对于sAAA与aAAA破裂风险的预测及区分,除了临床上常用的几何学数据,还应从血流动力学的角度以及病理生理学的角度去分析。
在该研究中,在sAAA与aAAA的瘤体最大直径、瘤颈长度、瘤颈角度的几何学变量比较中,瘤体最大直径差异具有统计学意义,sAAA组中偏心性动脉瘤的比例相对较高,为临床上积极处理sAAA提供了支持。瘤颈长度与瘤体最大直径存在负相关关系,而瘤颈角度与瘤体最大直径存在正相关关系,腹主动脉瘤形态学变量之间也是彼此联系、相互影响的,但不能单以瘤体的最大直径来预测腹主动脉瘤破裂风险,还应从血流动力学的角度以及病理生理学的角度去分析,这样会使预测及判定更加科学。

